介紹 鄰基因組成的DNA片段,其中結構基因的表達受到操縱基因的調控。主要見於
原核生物 ,在
真核生物 中少見。
操縱子 原核生物 原核生物 大多數
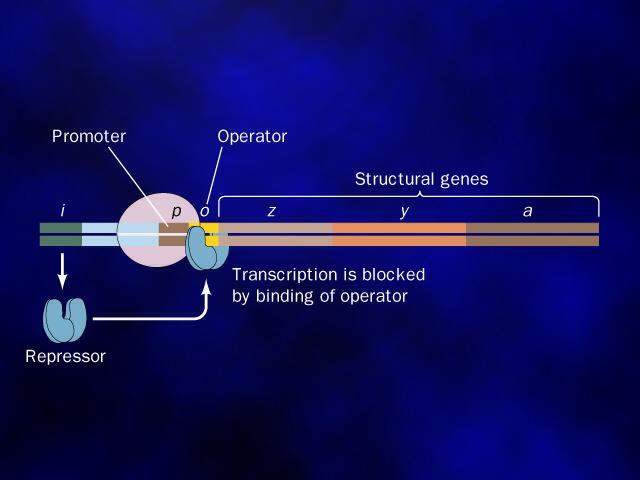
基因表達調控 是通過操縱子機制實現的。操縱子通常由 2個以上的編碼序列與啟動序列、操縱序列以及其他調節序列在基因組中成簇串聯組成。啟動序列是
RNA聚合酶 結合併啟動
轉錄 的特異DNA序列。多種原核基因啟動序列特定區域內,通常在轉錄起始點上游-10及-35區域存在一些相似序列,稱為
共有序列 。大腸桿菌及一些細菌啟動序列的共有序列在-10區域是TATAAT,又稱Pribnow盒(PribnowBox),在-35區域為 TTGACA。這些共有序列中的任一鹼基突變或變異都會影響RNA聚合酶與啟動序列的結合及轉錄起始。因此,與
共有序列 的一致度決定啟動序列的轉錄活性大小。操縱序列是原核
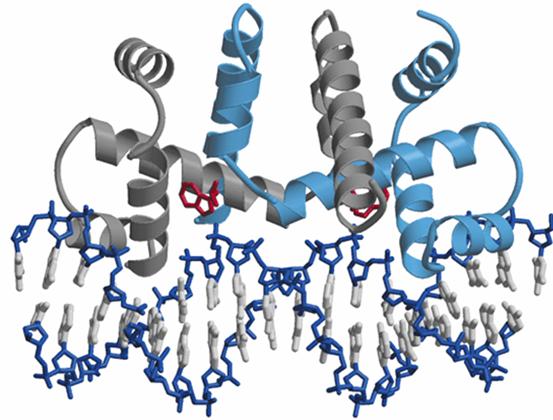
阻遏蛋白 的結合位點。當操縱序列結合阻遏蛋白時會阻礙RNA聚合酶與啟動序列的結合,或使RNA聚合酶不能沿DNA向前移動,阻遏轉錄,介導負性調節。原核操縱子調節序列中還有一種特異DNA序列可結合激活蛋白,使轉錄激活,介導正性調節。
操縱子 阿拉伯糖 阿拉伯糖操縱子 ara operon
結構和功能 阿拉伯糖的代謝是由araB、araA和araD基因所編碼的三種酶的催化的。其特點是:
⑴AraC蛋白是雙功能的,單純的araC蛋白結合於araO1(-100~-144)(操縱基因),起到阻遏的作用;當araC蛋白和
誘導物 Ara結合形成的複合體是Cind(CinducedPro.誘導型araC蛋白),它結合於araI區(-40~-78)使RNA Pol(RNA聚合酶)結合於PBAD位點(+140),
轉錄 araB、araA、araD三個基因;
⑵C蛋白結合araO1時也反饋性地阻遏了其本身的表達;
⑶araC蛋白的兩種狀態(Cind和Crep)功能不同,結合的位點也不同Cind結合於araI
Crep(Crepressionprotein阻遏型araC蛋白)可結合於araO1和araO2;
⑷ara操縱子的araC蛋白還可以調節分散的基因araE和araF,因此,
轉錄單位 也稱
調節子 (regulon);
⑹Pc啟動子和araO1重疊。
調控 當Glu(葡萄糖)和Ara(阿拉伯糖)都存在時,araC蛋白基因
轉錄 ,產生少量的C蛋白,結合於araO1(-106~-144),使RNA聚酶不能結合PC啟動子,使araC的轉錄受到阻遏。
當有Ara存在,而沒有Glu時,Ara可作為糖源。此時Ara和少量的araC蛋白結合形成了誘導型的araC蛋白—Cind,它作為
正調控 因子結合於araI,促進了araPBAD的轉錄,產生了araB、araA、araD 3種酶,促使Ara分解;
當Ara不存在或者用過完了,過量的araC蛋白可以結合則araO1上,阻礙RNA聚合酶在此區域結合,從而關閉了操縱子;或者結合到araI(-40~-78)和araO2上,彼此相互作用形成了環,阻遏了PBAD和PC的啟動。
乳糖 乳糖操縱子(lac操縱子)
大腸桿菌的lac操縱子受到兩方面的調控:一是對RNA聚合酶結合到啟動子上的調控(
正調控 );二是對操縱基因的調控(
負調控 )。
在含葡萄糖的
培養基 中大腸桿菌不能利用乳糖,只有改用乳糖時才能利用乳糖,這一現象的調控機理是:當在培養基中只有乳糖時由於乳糖的代謝產物異乳糖是lac操縱子的
誘導物 ,它可以結合在
阻遏蛋白 的變構位點上,使構象發生改變,破壞了阻遏蛋白與
操縱基因 的親和力,不能與操縱基因結合,於是RNA聚合酶結合於
啟動子 ,並順利地通過操縱基因,進行
結構基因 的
轉錄 ,產生大量分解乳糖的酶,這就是當大腸桿菌的培養基中只有乳糖時利用乳糖的原因。
操縱子 在含乳糖的培養基中加入葡萄糖時,不能利用乳糖的原因是:在lac操縱子的調控中,有
降解物基因活化蛋白 (CAP),當它特異地結合在啟動子上時,能促進RNA聚合酶與啟動子結合,促進轉錄(由於CAP的
結合能 促進轉錄,稱為陽性調控方式)。但游離的CAP不能與啟動子結合,必須在細胞內有足夠的cAMP時,CAP首先與cAMP形成複合物,此複合物才能與啟動子相結合。葡萄糖的
降解產物 能降低細胞內cAMP的含量,當向乳糖培養基中加入葡萄糖時,造成cAMP濃度降低,CAP便不能結合在
啟動子 上。此時即使有乳糖存在,RNA聚合酶不能與啟動子結合,雖已解除了對
操縱基因 的阻遏,也不能進行
轉錄 ,所以仍不能利用乳糖。
色氨酸 色氨酸操縱子的基本結構
大腸桿菌色氨酸操縱子結構較簡單,也是研究得最清楚的操縱子,
結構基因 依次排列為trpE,trpD,trpC,trpB,trpA,其中trpG與trpD 和trpC與trpF分別發生
基因融合 。trpE和trpG編碼
鄰氨基苯甲酸 合酶,trpD編碼鄰氨基苯甲酸磷酸核糖
轉移酶 ,trpC編碼
吲哚甘油磷酸合酶 ,trpF編碼
異構酶 ,trpA和trpB分別編碼色氨酸合酶的α和β亞基。trpE的上游為調控區,由
啟動子 、
操縱基因 和162bp 的
前導序列 組成。5 個結構基因全長約6800bp,trpD遠側還有一個二級啟動子,在
細胞生長 需要過量Trp時發揮作用。
一些G+菌,如
枯草桿菌 色氨酸操縱子 的結構有所不同,7 個
結構基因 中的6 個依次排列為trpE,trpD,trpC,trpF,trpB,trpA,存在於含有12個結構基因的
芳香族胺基酸 超操縱子 ( aro operon ),第7 個結構
基因 ,trpG存在於葉酸合成操縱子中,該酶參與Trp 和葉酸的合成。有2個啟動子參與調控,一個位於aro operon的起始位置,另一個則位於trpE 上游約200 bp處。
色氨酸操縱子的調控作用途徑
阻遏作用
trp操縱子 轉錄起始 的調控是通過
阻遏蛋白 實現的。產生阻遏蛋白的
基因 是trpR,該基因距trp operon
基因簇 很遠。它結合於trp
操縱基因 特異序列,阻止轉錄起始。但阻遏蛋白的DNA結合活性受Trp調控,Trp起著一個效應分子的作用,Trp與之結合的動力學常數為1~2 ×10- 5mol·L - 1。在有高濃度Trp存在時,阻遏蛋白-
色氨酸 複合物形成一個同源二聚體,並且與色氨酸操縱子緊密結合,因此可以阻止
轉錄 。阻遏蛋白- 色氨酸複合物與基因特異位點結合的能力很強,動力學常數為2 ×10- 10mol·L - 1,因此細胞內阻遏蛋白數量僅有20~30分子已可充分發揮作用。當Trp 水平低時,
阻遏蛋白 以一種非活性形式存在,不能結合DNA。在這樣的條件下,trp操縱子被RNA聚合酶轉錄,同時Trp
生物合成 途徑被激活。
弱化作用
trp操縱子 轉錄終止 的調控是通過
弱化作用 ( attenuation)實現的。在大腸桿菌trp operon,
前導區 的鹼基序列包括4個分別以1、2、3和4表示的片段,能以兩種不同的方式進行
鹼基配對 ,1 - 2和3 -4配對,或2 - 3配對,3 - 4配對區正好位於
終止密碼子 的識別區。
前導序列 有相鄰的兩個色氨酸
密碼子 ,當培養基中Trp 濃度很低時,負載有Trp 的tRNATrp也就少,這樣翻譯通過兩個相鄰色氨酸密碼子的速度就會很慢,當4區被
轉錄 完成時,核糖體滯留1區,這時的前導區結構是2 - 3配對,不形成3 - 4配對的終止結構,所以轉錄可繼續進行。反之,核糖體可順利通過兩個相鄰的色氨酸密碼子,在4區被轉錄之前,核糖體就到達2區,這樣使2 - 3不能配對,3 - 4 區可以配對形成
終止子 結構,轉錄停止。
枯草桿菌 的
弱化作用 機制另有特點。因其
色氨酸操縱子 結構的特殊性,
轉錄起始 的調節似乎不如
轉錄終止 的調節更具重要性。枯草桿菌色氨酸操縱子表達主要受到色氨酸激活
RNA結合蛋白 ( Trp -activated RNA - binding p rotein,TRAP)的調節。該蛋白與色氨酸結合被激活後,可與trpE上游
轉錄 產物結合,導致轉錄終止。當色氨酸濃度較低時,TRAP失活,轉錄可以繼續,
結構基因 得以表達。另外枯草桿菌對未負荷色氨酸的tRNATrp也很敏感,後者大量堆積,會誘導合成抗TRAP 蛋白( anti -TRAP,AT)。AT與Trp激活的TRAP結合,可以取消其轉錄終止活性。trpG表達也受TRAP調控,活化的TRAP與和trpG相重疊的S - D 序列結合,阻礙核糖體的結合,抑制trpG轉錄。
反饋抑制作用
由於基因表達必然消耗一定的能源和前體物,相對於阻遏和
弱化作用 ,反饋抑制作用更為經濟和高效。終產物Trp對催化分支途徑幾步反應的酶具有反饋抑制作用,其50%抑制濃度分別為:
鄰氨基苯甲酸 合酶 ,0. 0015 mmol·L - 1 ;鄰氨基苯甲酸磷酸核糖
轉移酶 ,0. 15 mmol·L - 1 ;
色氨酸合成酶 ,7. 7mmol·L - 1。對於普通野生
菌株 ,鄰氨基苯甲酸合酶對Trp合成起到關鍵調控作用,常被稱為瓶頸酶;但對高產Trp工程菌而言,上述任何一種酶的
反饋抑制 都會直接影響Trp產量。研究發現
酶蛋白 某些特殊位點突變可以導致對反饋抑制作用敏感性顯著下降,如鄰氨基苯甲酸合酶38位的絲氨酸被
精氨酸 取代,抗反饋抑制能力顯著提高,當環境中Trp濃度為10 mmol·L - 1時酶活性不受影響,而相同條件下野生型酶活性不到1%。鄰氨基苯甲酸磷酸核糖
轉移酶 162位
纈氨酸 被
谷氨酸 取代,抗反饋抑制能力也有顯著提高,當環境中含有0. 83 mmol·L - 1色氨酸或0. 32 mmol·L - 1 5 - 甲基- 色氨酸時,酶活性分別為野生菌的3. 6倍和2. 4倍。
陳小芳 等報導一株谷氨酸棒桿菌
鄰氨基苯甲酸 合酶
基因 7個鹼基突變導致6個
胺基酸 殘基改變,抗反饋抑制能力顯著增強,環境中Trp 濃度達到15 mmol·L - 1時,鄰氨基苯甲酸合酶活性幾乎沒有變化。
色氨酸操縱子遺傳改造
由於
色氨酸操縱子 的調控作用,自然界不可能存在高產Trp
菌株 ,為了獲得高產Trp菌株,就必須對色氨酸操縱子進行改造,解除其調節作用。早期的研究策略主要依靠傳統誘變方法,經過長期努力,獲得了一些有價值的研究結果,如獲得了TrpR - 菌株,通過缺失某些片斷解除了
弱化作用 ,得到了一些抗反饋抑制的酶。許多Trp生產菌株都是通過隨機的誘變技術篩選得到的,如
王健 等通過硫酸二乙酯誘變,Trp 類似物篩選等方法從
谷氨酸 棒桿菌中培育出一株trp 高產菌株,搖瓶發酵64 h,產trp達到7. 28 g·L - 1。
傳統誘變的方法儘管有效,但其缺陷點也是顯而易見的,如工作量大,效率低,
突變株 的菌體生長、對環境的耐受性以及遺傳穩定性等都比
野生型 菌株差等。
基因工程技術 的建立和發展對
色氨酸操縱子 改造提供了新的技術平台。1979年Tribe等人採用
DNA重組技術 對大腸桿菌進行改造,擴增trp 操縱子,發酵12 h,產酸1 g·L - 1,產酸量儘管不是很高,但是其意義卻十分重大,由此開創了
基因 工程技術在Trp
生物合成 套用的先河。隨後,Aiba等將帶有色氨酸操縱子的質粒引入大腸桿菌,發酵27 h,並補充
鄰氨基苯甲酸 ,得到trp 6. 2 g·L - 1。Ikeda等通過構建穩定質粒,擴增分支途徑
限速酶 並改造中心
代謝途徑 ,獲得產Trp 達58 mg ·L - 1 的
菌株 。除了擴增表達操縱子基因,對其進行理性設計和改造也開始引起關注。已知酶分子某些特殊位點突變可以導致對反饋抑制作用敏感性下降,因此可以考慮利用
基因工程技術 對
色氨酸操縱子 結構基因 進行理性改造降低其對反饋抑制的敏感性,但是Z至今尚缺乏成功的範例,主要原因在於現有酶分子反饋抑制結構與功能關係資料不足,不能滿足需要。
代謝工程理論與色氨酸操縱子調控研究
1991年,Bailey用代謝工程描述利用DNA重組技術對細胞的酶反應、物質運輸以及調控功能的
遺傳操作 ,進而改良細胞生物活性的過程,標誌著代謝工程向一門系統學科發展的轉折點。代謝工程亦稱
途徑工程 ,以區別於傳統的單基因表達(第一代基因工程)和基因定向突變(
第二代基因工程 ),是有目的地對細胞
生化反應 的
代謝網路 進行修飾的技術,在多基因水平上設計修飾細胞固有的
代謝途徑 和遺傳性狀,並賦予細胞更為優越甚至嶄新的產物生產品質。代謝工程在提高
宿主細胞 原有
代謝物 的產量、產生新物質、擴展和構建新代謝途徑、生產代謝產物如
胺基酸 、抗生素、維生素以及降解
環境污染物 等諸多方面顯示出廣闊的套用前景。從理論上提高Trp產率是代謝工程的首要任務,這需要對Trp
生物合成 和對細胞內控制Trp 代謝的異化途徑有很好的了解,同時還要有一個在較寬的微生物代謝網路內描述這些途徑的有效的數學模型。早期的模型主要考慮
色氨酸操縱子 動力學的某個方面,僅有少數研究模型,綜合考慮了色氨酸操縱子的三種作用機制。
修志龍 等將代謝工程理論引入trp代謝分析領域,建立了適宜的數學模型,發現在代謝穩定的條件下,阻遏水平和酶的
反饋抑制 強度嚴重地影響了目標變數,即trp 濃度。Santillan等人提出的動力模型採用Second Lyapunov’s method分析,通過對野生菌株和幾株改良菌株(
鄰氨基苯甲酸 合成酶 反饋抑制和
弱化作用 分別解除)的性能進行比較、驗證,得出結論認為酶的反饋抑制對於系統穩定性具有重要作用,而弱化作用影響較小,主要在Trp營養發生改變時發生作用。這兩個模型有一定的代表性,它們考慮了酶的反饋抑制,對於Trp
生物合成 具有一定指導意義;但其不足也很明顯,僅僅考慮了鄰氨基苯甲酸合成酶的反饋抑制作用,對其它酶未作考慮,另外一個不足是缺乏高產色氨酸菌株來加以驗證。
 操縱子
操縱子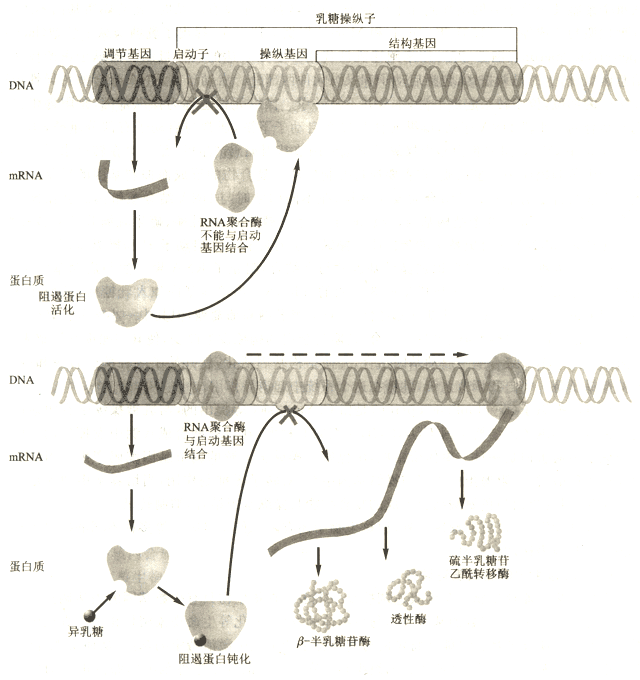 操縱子
操縱子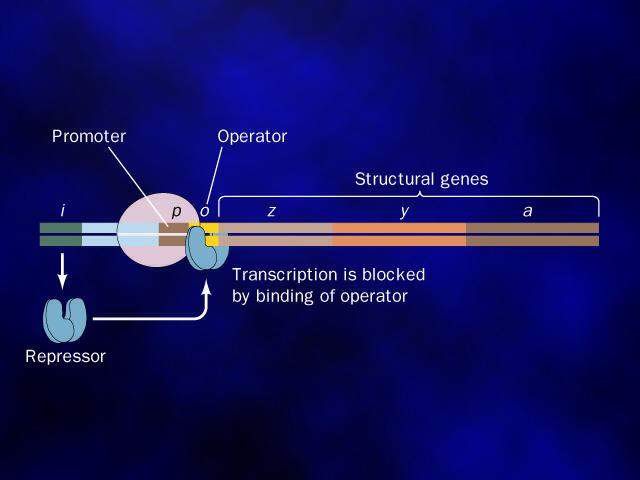
 操縱子
操縱子