基本介紹
- 中文名:恆沸點
- 外文名:azeotropic point
- 分類:最高恆沸點和最低恆沸點
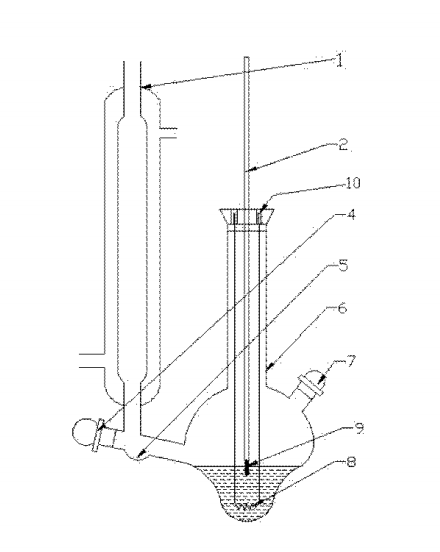
到達恆沸點時體系的自由度為0,即體系的各強度性質都皆為常數。可以用恆沸點測定儀來測量恆沸點。基本概念在某些二組分氣液平衡溫度-組成(T~x)圖中,會出現一個最高或最低點,這一點能同時表示呈平衡的氣、液兩相所處的狀態,表示...
恆沸物是指多種相溶液體組成的混合物,在出現蒸汽壓正偏差和負偏差時,所對應的固定組成的混合物,其特點的泡點溫度和蒸發組成依照液相組成變化,只有在恆沸點組成下的液體混合物才會按照恆沸點對應的比例蒸發。而共沸物是指多種不溶或微溶的物質(固體之間或液體之間)組成的混合物,其組成無論如何變化,其沸點是...
恆沸液,也叫恆沸溶液或恆沸混合物。在一定條件下,當某溶液的組成與其處於平衡狀態的蒸汽組成相同時,其沸點保持恆定不變。許多物質與水組成的液體如氫鹵酸、HNO3、H2SO4、酒精的溶液等都有一種在一定溫度下沸騰而其組成不變的溶液。這種在恆壓下組成保持一定的沸點的溶液即稱為恆沸液。當壓力改變時,它的...
反應結束後,先利用乙醇與水共沸(共沸點78.1℃)的特點共沸蒸出乙醇和水,再加入正庚烷共沸精餾,餾出物為正庚烷與水(恆沸點88~98℃)、正庚烷和乙二胺(恆沸點87~97℃)及正庚烷-乙二胺-水的三元共沸物(共沸點88~97℃)。餾出物分層後,分去水層,正庚烷返回釜內,直到水全部蒸出、再將乙二胺與正...
硫酸的沸點及粘度較高,是因為其分子內部的氫鍵較強的緣故。由於硫酸的介電常數較高,因此它是電解質的良好溶劑,而作為非電解質的溶劑則不太理想。硫酸的熔點是10.371℃,加水或加三氧化硫均會使凝固點下降。濃度的差異 儘管可以制出濃純淨的硫酸,並且室溫下是無限穩定的(所謂的分解成恆沸物的反應發生在接近...
恆沸精餾法 以正戊烷為恆沸劑,正戊烷和異戊二烯形成恆沸物(恆沸點33.8℃,恆沸組成含正戊烷28%),由於恆沸點和其他C5烴的沸點相近,需要塔板數多、回流比大才能由裂解C5餾分中分離出正戊烷和異戊二烯的恆沸物。該法只適用於C5餾分中含正戊烷較多,產品異戊二烯的再加工是以正戊烷為溶劑或正戊烷的存在不影響...
共沸屬於一種多相體系,兩種(或幾種)液體形成的具有恆沸點的混合物稱為共沸混合物。三種組分形成的具有恆定沸點的叫做三元共沸物。三元共沸物相圖特點 ① 三個性質相同的二組分共沸物→形成一個三元共沸物。② 兩個性質相同的二組分共沸物→P面→脊or谷 。③ 一個正(負)偏差共沸物與一個不參加此二元共沸物...
azeotropic,英語單詞,主要用作形容詞,作形容詞時譯為“共沸點的;恆沸點的”。短語搭配 azeotropic mixture[化學] 共沸混合物 ; 共沸點混合物 ; 恆沸點混合物 ; 氣液混合物 azeotropic point[化學] 共沸點 ; 恆沸點 ; 恆比點 ; 翻譯 azeotropic process 共沸過程 ; 翻譯 ; 共沸蒸餾過程 ; 共沸蒸餾過程...
當泡點與液相組成的關係中,出現極小值或極大值時,這極值溫度相應稱為最低恆沸點或最高恆沸點,這時,汽相與液相組成相同,相應的混合物稱為恆沸混合物。汽液平衡時,液相的泡點即為汽相的露點。由液相組成計算一定壓力下的泡點和汽相組成,稱為泡點計算,基本公式為(見圖一)式中m為組分數;xi、yi和Ki分別...
在共沸蒸餾中,第三種溶劑(稱作共沸劑)被加到初始共沸混合物中,它可與原來混合物中的一種組分形成恆沸點混合物,由此產生的沸點變化經常大到足以引起沸點接近的物質的進一步分離,原共沸混合物中的一種成分的定量移去依賴於加入的共沸劑過量的情況,第二個要求是共沸劑必須容易用簡單蒸餾方法除去。無水乙醇可通過...
苯能與水恆沸,沸點69.25 ℃,含苯91.2%,在有水生成的反應中常加苯蒸餾,以將水餾出。10~1500 mmHg間的飽和蒸氣壓可以根據安托萬方程計算:P單位為mmHg,t單位為℃,A=6.91210,B=1214.645,C=221.205。化學性質 苯參加的化學反應大致有3種:一種是其他基團和苯環上的氫原子之間發生的取代反應;一...
(1)聚甲醛與乙二醇在三氯化鐵催化劑作用下,在90~110℃下反應,然後常壓蒸餾,製得共沸物,為了突破恆沸點,可採用諸如分子篩等脫水劑,脫除恆沸物中的一部分水,再精餾精製而得;(2)乙二醇與甲醛反應可得;(3)環氧乙烷與甲醛在路易斯酸催化劑存在下反應可得。其他信息 與水形成共沸物,共沸點70~73℃,含...
《跨越精餾區間和精餾邊界的分離的研究》是依託西安交通大學,由劉桂蓮擔任項目負責人的專項基金項目。中文摘要 恆沸精餾是化學工程領域極為重要的化工單元操作。但由於恆沸點的存在,恆沸精餾系統的組成空間通常被分為多個精餾區間和精餾單元。而要實現分離,通常需要跨越精餾區間或跨越精餾單元。因此,研究恆沸精餾系統中...
對於正偏差很大的系統,存在最低恆沸點。屬於這類系統的有:水和乙醇、甲醇和苯、乙醇和苯等。對於負偏差很大的系統,存在最高恆沸點。屬於這類系統的有:水和硝酸、氯化氫和二甲醚、水和氯化氫等。部分互溶的雙液系 這種體系按照會溶溫度(即部分互溶變為互溶的溫度)的不同可以分為以下四類:具有最高會溶...
但實際上,非理想液態混合物更為常見。對於非理想液態混合物,它們的行為與Raoult定律存在一定的偏差。對於正偏差很大的系統,存在最低恆沸點。屬於這類系統的有:水和乙醇、甲醇和苯、乙醇和苯等。對於負偏差很大的系統,存在最高恆沸點。屬於這類系統的有:水和硝酸、氯化氫和二甲醚、水和氯化氫等。
萃取精餾和恆沸精餾相似,也是向原料液中加入第三組分(稱為萃取劑或溶劑),以改變原有組分間的相對揮發度而得以分離。不同的是,要求萃取劑的沸點較原料液中各組分的沸點高很多,且不與組分形成恆沸液。萃取精餾常用於分離各組分沸點( 揮發度) 差別很小的溶液。例如,在常壓下苯的沸點為80.1℃,環己烷的沸點為...
萃取蒸飽是指一種特殊的精餾方法,用以分離恆沸點混合物或組分揮發度相近的液體混合物。通常是在精餾時加入某種較難揮發的物質,以增大液體混合物中各組分的揮發度的差異,使揮發度相對地變大的組分可由精餾塔頂餾出,揮發度相對地變小的組分則與加入的物質聚集於塔底而取出。用於不能或難於用普通精餾方法進行分離...
在蒸汽張力曲線存在最大值的系統中,壓力增高,蒸發能耗高的組分在恆沸混合物中的濃度增加。相反,壓力降低時,蒸發能耗低的組分在恆沸混合物中的濃度增加。低濃度的酒精—水溶液,壓力增高,氣相中的酒精濃度增加;相反,高濃度的酒精水溶液,壓力增高,氣相中的水分增高。據此進行減壓蒸餾,可將恆沸點往增加酒精濃度...
下面以製取無水酒精為例,說明共沸精餾的過程,水和酒精能形成具有恆沸點的混合物,所以用普通的精餾方法不能獲得純度超過96%(體積)的乙醇,若在酒精和水的溶液中加入共沸組分--苯,則可構成各種恆沸混合物,但以酒精、苯和水所組成的三組分共沸混合物的沸點為最低(64.84℃)。當精餾溫度在64.85℃時,酒精...
共沸乾燥 共沸乾燥兩種(或幾種)液體形成的恆沸點混合物。共沸混合物用途: 比如說有些有機化合物能與水形成共沸混合物,可以利用該特性,在待乾燥的有機物中加入共沸組成中某一有機物,因共沸混合物的沸點通常低於待乾燥的有機物的沸點,所以蒸餾時可將水帶出來,從而達到乾燥的目的。
完全互溶雙液體系 完全互溶雙液體系是指兩個純液體可按任意比例互溶,每個組分都服從拉烏爾定律,也稱理想的液體混合物。通常雙液系可分為三類:(1)無恆沸點雙液系(2)有最低恆沸點雙液系,如圖1(3)有最高恆沸點雙液系
基於兩種同位素分子的揮發性(沸點)的差異,藉助於加熱液態同位素混合物來實現同位素分離的方法.當同位素混合物被加熱並同時存在於氣液兩相時,易揮發的同位素分子又較多地存在於氣相內,而難揮發的同位素分子則較多地存在於液相內.這樣,在氣相中就濃集了易揮發的同位素,而在液相中濃集了較難揮發的同位素.例如,輕水(H20...
蒸餾是一種熱力學的分離工藝,它利用混合液體或液-固體系中各組分沸點不同,使低沸點組分蒸發,再冷凝以分離整個組分的單元操作過程,是蒸發和冷凝兩種單元操作的聯合。與其它的分離手段,如萃取、過濾結晶等相比,它的優點在於不需使用系統組分以外的其它溶劑,從而保證不會引入新的雜質。詞語解釋 1. [distill]∶...
負偏差溶液 負偏差溶液: 異分子間的吸引力大,使得溶液的兩個組分的平衡分壓都比拉烏爾定律所預計的低.負偏差嚴重時形成具有最高恆沸點的溶液.
正偏差溶液 正偏差溶液,即異分子間的排斥傾向起了主導作用,使溶液的兩個組分的平衡分壓都比拉烏爾定律所預計的高,正偏差嚴重時形成具有最低恆沸點的溶液。
