基本信息
化學式
化學式:SnCl4
式量:260.50
編號系統
CAS號:7646-78-8
 四氯化錫試劑
四氯化錫試劑MDL號:MFCD00011242
InChI:1S/4ClH.Sn/h4*1H;/q;;;;+4/p-4
物化性質
四氯化錫工業品為無色或淡黃色的液體,暴露於空氣中與空氣中水分反應生成白煙,有強烈的刺激性,遇水分解,生成鹽酸及正錫酸。
遇潮濕空氣,起水解反應生成
錫和
氯化氫,發生白煙,有腐蝕性。與計算量的水形成五水合物,白色半透明單斜晶體,在空氣中潮解。溶於冷水並放出大量的熱,溶於
乙醇、
乙醚、
苯、
甲苯、
四氯化碳。遇熱水則分解。在濕空氣中吸水生成為三水物。進一步加水,生成5、8、9等不同數量的結晶水的化合物。無水氯化錫在低溫下能吸收大量的氯氣,同時體積形成膨脹和冰點下降;能與氨反應生成復鹽;與鹼金屬作用生成錫酸鹽。遇水強烈水解,因此在潮濕的空氣中發煙;可溶於有機溶劑如乙醇、四氯化碳、苯、
丙酮等。
鹽酸可抑制其水解作用。在19~56℃範圍內,鹽酸可使四氯化錫從濃溶液中以無色的水合晶體SnCl4·5H2O析出。
計算化學數據
1、疏水參數計算參考值(XlogP):無可用
2、氫鍵供體數量:0
3、氫鍵受體數量:0
4、可旋轉化學鍵數量:0
5、拓撲分子極性表面積(TPSA):0
6、重原子數量:5
7、表面電荷:0
8、複雜度:19.1
9、同位素原子數量:0
10、確定原子立構中心數量:0
11、不確定原子立構中心數量:0
12、確定化學鍵立構中心數量:0
13、不確定化學鍵立構中心數量:0
14、共價鍵單元數量:1
製備方法
①金屬錫氯化法:將金屬錫熔融,然後潑入冷水,激成錫花,加入反應器中,通入乾燥
氯氣進行反應,生成四氯化錫。由於產物中有過量的
游離氯而呈黃色。可加入幾片錫薄片,加熱蒸餾,用乾燥容器接收105~120℃的
餾分,製得無水氯化錫成品。其反應方程式為:
Sn+2Cl2→SnCl4
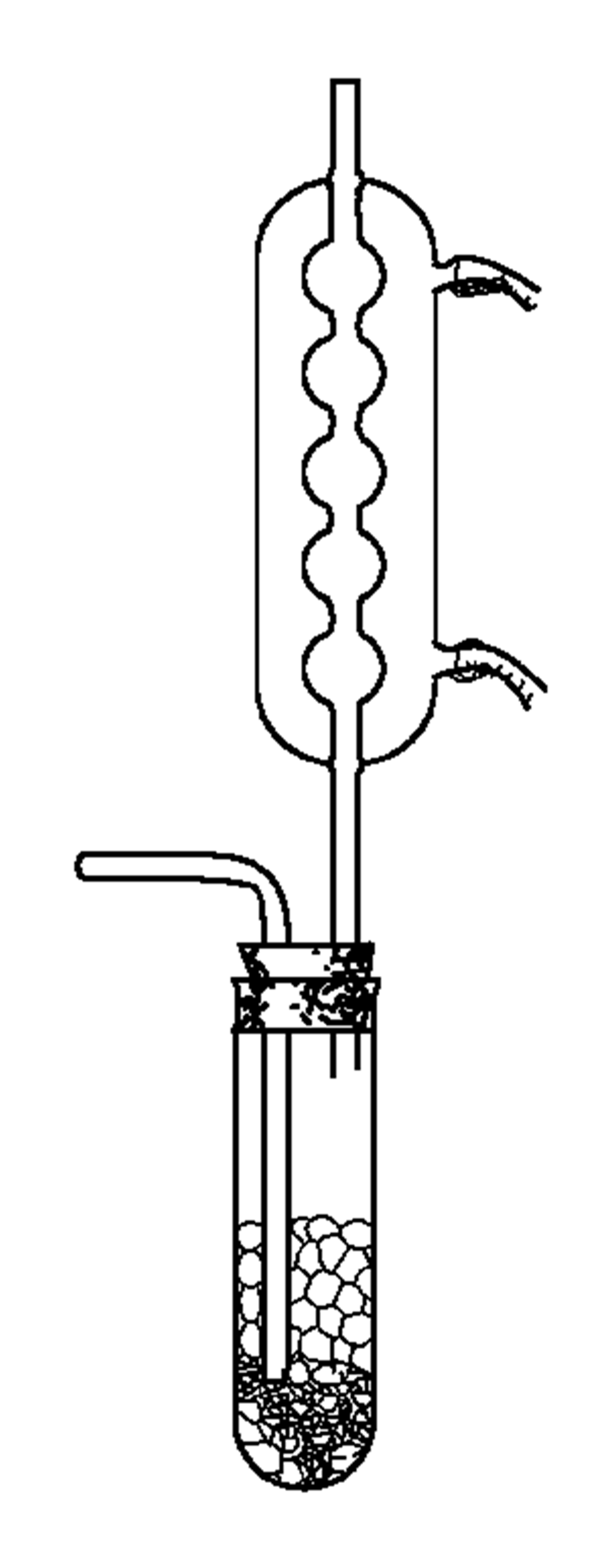 製備四氯化錫的裝置
製備四氯化錫的裝置在
通風櫥內按圖裝配好儀器。大試管內裝入錫粒至其體積的
。開始從導氣管中緩慢地通入乾燥的氯氣,氣流速度應使氯氣能與錫充分反應為宜。反應很激烈,當試管底部聚集的SnCl
4液層明顯增厚時,適當提高導氣管,但末端仍應沒入溶液中。反應結束後將SnCl
4傾入玻璃瓶中,加入少許錫粒用以與游離的氯作用,將此瓶密閉靜置1h。蒸餾,收集112~114℃間的餾分,為防濕氣侵入,接受器上應安裝
CaCl2乾燥管。如果原料錫中含有鐵,蒸餾不宜進行到底。所得SnCl
4裝入帶玻璃塞或軟木塞的玻璃瓶中。
 製備四氯化錫的“雙聯式”裝置
製備四氯化錫的“雙聯式”裝置圖為製備氯化錫的裝置圖製備氯化錫的“雙聯式”裝置
1,2—試管;3,4—支管;5—氯氣導管;6—連線管;7—球形冷凝器
若大量製取(每天3kg)SnCl4,可採用如圖的裝置。當試管1中幾乎充滿SnCl4時,停止通氯氣。在管5下面放一乾燥的玻璃瓶,用橡皮球從冷凝管7上口向裝置內吹氣,則SnCl4被排入管5下面的玻璃瓶中。然後經支管向試管中再填裝錫粒以繼續反應。所接收的SnCl4的處置和提純操作同上。產率可達90%~95%。
主要用途
製造藍曬紙和感光紙、潤滑油添加劑,玻璃表面處理以形成導電塗層和提高抗磨性。
用作有機合成中氯化的催化劑和糖漂白劑等;還可用於導電性塗層和鍍錫。
氯化錫的蒸氣與
氨及水汽混合,生成
氫氧化錫及
氯化銨之微粒而呈濃煙狀,軍事上用以製作煙幕彈。反應式:SnCl
4+4NH
3+4H
2O→Sn(OH)
4+4NH
4Cl.
用於製作FTO導電玻璃, FTO玻璃可以做為ITO導電玻璃的替換用品,廣泛用於液晶顯示屏,光催化,
薄膜太陽能電池基底等方面,市場需求極大。反應式為:SnCl
4+2H
2O=SnO
2+4HCl.
用作分析試劑、有機合成脫水劑。也用於電鍍工業。
醇酸酯化反應:由於酸醇醋化反應傳統的生產工藝是以濃硫酸為催化劑製備, 具有生產周期長, 副產品多, 設備腐蝕嚴重, 反應後處理複雜, 廢酸污染環境等缺點,因此人們一直致力於新型催化劑的研究, 以簡化生產工藝, 降低生產成本, 四氯化錫作為高效醋化催化劑, 是一種價廉易得的化工產品, 因此, 引起人們的廣泛關注, 在這方面的研究也日益增多。四氯化錫取代傳統的濃硫酸催化劑作為醋化催化劑, 在酸醇醋化方面的研究最多, 研究涉及無水四氯化錫或五水四氯化錫的催化醋化、氯乙酸和醇的催化醋化、固載形式的催化醋
縮酮反應:王建平用SnCl
4.5H2O為催化劑以
環己酮、
乙二醇為原料合成了環己酮縮乙二醇。
雙烯合成
脫水反應利用SnCl4.5H2O作催化劑進行脫水反應的研究不多, 尚待更進一步的研究。
環境影響
健康危害
侵入途徑:吸入、食入。
健康危害:對眼睛、皮膚、黏膜和呼吸道有強烈的刺激作用。吸入、攝入或經皮膚吸收對身體有害。吸入可能由於咽喉、支氣管的痙攣、水腫、炎症,化學性肺炎、肺水腫而致死。中毒表現有燒灼感、咳嗽、喘息、喉炎、氣短、頭痛、噁心和嘔吐。
毒理學資料
毒性:屬低毒類。
危險特性:受高熱分解產生有毒的腐蝕性氣體。遇
氰化物能產生劇毒的氰化氫氣體。
燃燒(分解)產物:氯化物。
生態學資料
對環境有危害,應特別注意對水體的污染。
環境標準
美國(1974)職業安全及衛生管理局標準:空氣:時間加權平均值2mg/m3[Sn]。
監測方法
空氣中:樣品用濾器收集,再用原子吸收光譜法測定(NIOSH法)。
應急處理
泄漏處理
疏散泄漏污染區人員至安全區,禁止無關人員進入污染區,建議應急處理人員戴自給式呼吸器,穿化學防護服。不要直接接觸泄漏物,勿使泄漏物與可燃物質(木材、紙、油等)接觸,在確保全全情況下堵漏。噴水霧減慢揮發(或擴散),但不要對泄漏物或泄漏點直接噴水。將地面灑上蘇打灰,然後用大量水沖洗,經稀釋的洗水放入廢水系統。如果大量泄漏,最好不用水處理,在技術人員指導下清除。
廢棄物處置方法:廢料倒在碳酸氫鈉上,用
氨水噴淋,同時加碎冰,反應停止後用水沖入下水道。
防護措施
呼吸系統防護:可能接觸其蒸氣時,應該佩帶防毒口罩。
眼睛防護:戴化學安全防護眼鏡。
防護服:穿工作服(防腐材料製作)。
手防護:戴橡皮手套。
其它:工作後,淋浴更衣。單獨存放被
毒物污染的衣服,洗後再用。保持良好的衛生習慣。
急救措施
皮膚接觸:立即脫去污染的衣著,用大量流動清水徹底沖洗。若有灼傷,就醫治療。
眼睛接觸:立即提起眼瞼,用流動清水沖洗10分鐘或用2%碳酸氫鈉溶液沖洗。
吸入:迅速脫離現場至空氣新鮮處。注意保暖,保持呼吸道通暢。必要時進行人工呼吸。就醫。
食入:患者清醒時立即漱口,給飲牛奶或蛋清。立即就醫。
滅火方法:砂土、二氧化碳。禁止用水。
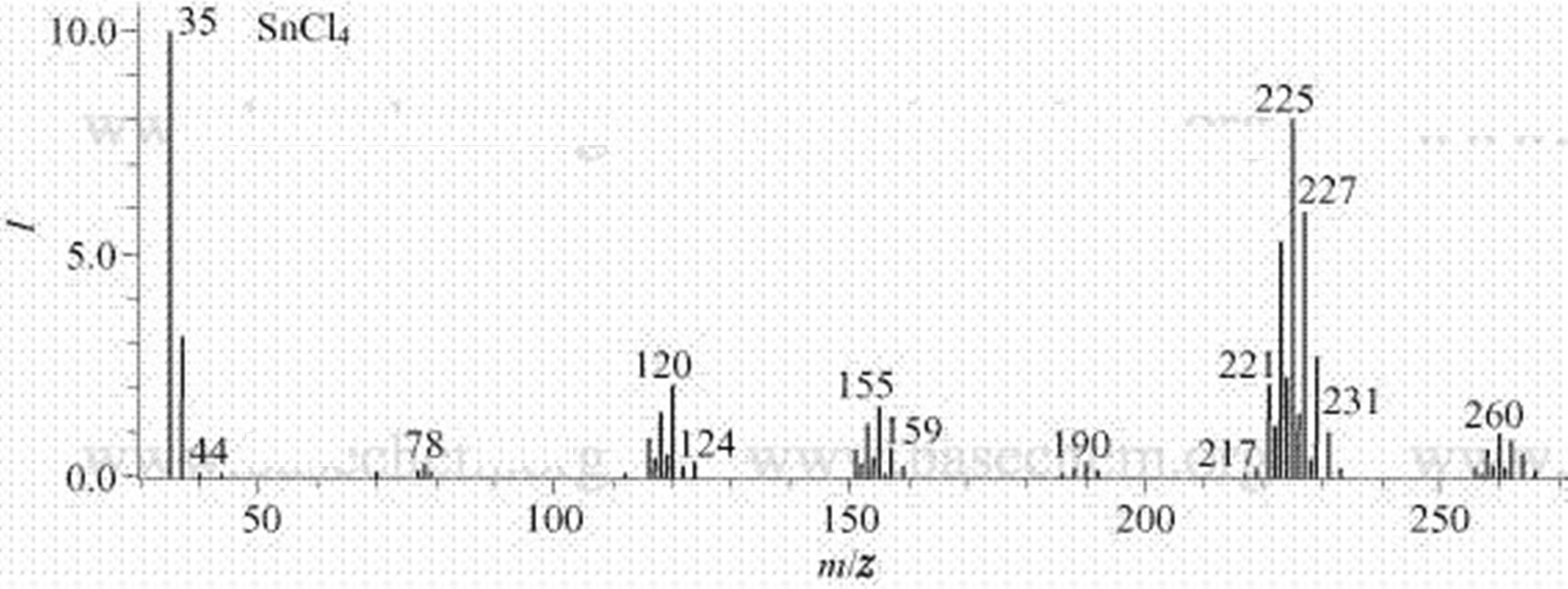 四氯化錫質譜(MS)
四氯化錫質譜(MS)貯存方法
儲存於陰涼、乾燥、通風良好的庫房。遠離火種、熱源。庫溫不超過30℃,相對濕度不超過75%。包裝必須密封,切勿受潮。應與易(可)燃物、鹼類、醇類等分開存放,切忌混儲。儲區應備有泄漏應急處理設備和合適的收容材料。
安全信息
危險運輸編碼
UN 1827 8/PG 2
危險品標誌
腐蝕
 腐蝕
腐蝕安全說明
S26:萬一接觸眼睛,立即使用大量清水沖洗並送醫診治。
S45:出現意外或者感到不適,立刻到醫生那裡尋求幫助(最好帶去產品容器標籤)。
S61:避免排放到環境中。參考專門的說明/安全數據表。
危險類別碼
R34:引起灼傷。
R52/53:對水生生物有害,可能在水生環境中造成長期不利影響。
五水合四氯化錫
CAS號:10026-06-9
物化性質
五水合四氯化錫,白色或微黃色結晶或熔塊。微有鹽酸氣味。吸濕性強。易溶於水,溶於乙醇。
計算化學數據
1、疏水參數計算參考值(XlogP):未確定
2、氫鍵供體數量:5
3、氫鍵受體數量:5
4、可旋轉化學鍵數量:0
5、拓撲分子極性表面積(TPSA):5
6、重原子數量:10
7、表面電荷:0
8、複雜度:19.5
9、同位素原子數量:0
10、確定原子立構中心數量:0
11、不確定原子立構中心數量:0
12、確定化學鍵立構中心數量:0
13、不確定化學鍵立構中心數量:0
14、共價鍵單元數量:6
製備方法
由無水四氯化錫緩慢地加入到水中,得到的熱溶液在攪拌下冷卻結晶製得。或者將氯氣通入二氯化錫溶液中至飽和,加熱蒸發,再冷卻結晶,分離製得。
向33mL水中分次少量地逐漸加入100g無水氯化錫,溶解時劇烈放熱,所得透明液體在攪拌和冷卻下即可全部結晶。產量100~103g,產率約85%。
將乾燥的氯氣通到裝有金屬錫粒的帶有冷凝器的容器底部,進行反應:
Sn+2Cl2=SnCl4
反應比較激烈,放出的熱量使四氯化錫發進入冷凝器,待反應結束後,將四氯化錫倒回反應器,密封靜置1h,讓過量錫與游離氯結合,然後將溶液蒸餾,收集112~114℃餾分,得無水四氯化錫。在攪拌下將所得四氯化錫溶解到適當蒸餾水中 (100g四氯化錫用33ml水) ,溶解時大量放熱,待透明熱溶液冷卻至完全結晶,即為結晶四氯化錫。
 四氯化錫試劑
四氯化錫試劑 製備四氯化錫的裝置
製備四氯化錫的裝置 四氯化錫質譜(MS)
四氯化錫質譜(MS) 腐蝕
腐蝕

 製備四氯化錫的“雙聯式”裝置
製備四氯化錫的“雙聯式”裝置