基本介紹
簡介
總反應
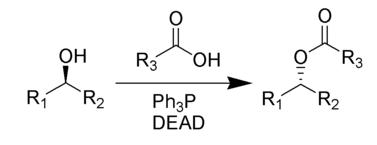 反應圖片一
反應圖片一反應機理
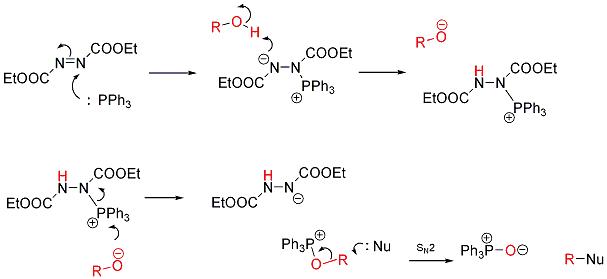 反應圖片二
反應圖片二用途
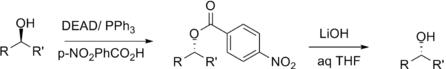 反應圖片三
反應圖片三重要合成反應中的作用
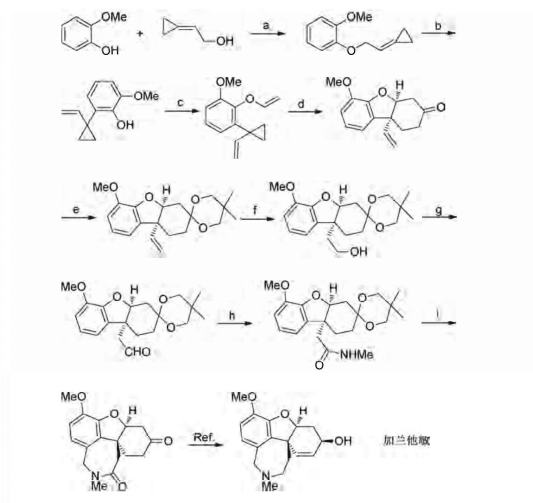 銠催化體系合成反應
銠催化體系合成反應
 反應圖片一
反應圖片一 反應圖片二
反應圖片二 反應圖片三
反應圖片三 銠催化體系合成反應
銠催化體系合成反應光延反應是一種雙分子親核取代反應(SN2反應)。由日本化學家光延旺洋(Mitsunobu, O) 等人於1967年發現,是現代有機合成中常用的反應。...
1921年,狄爾斯和其研究生巴克(Back)研究偶氮二羧酸乙酯(半個世紀後因光延反應而在有機合成中大放光芒的試劑)與胺發生的酯變胺的反應,當他們用2-萘胺做反應的...
狄爾斯和其研究生巴克(Back)研究偶氮二羧酸二乙酯(半個世紀後因光延反應而在有機合成中大放光芒的試劑)與胺發生的酯變胺的反應,當他們用2-萘胺做反應的時候,...
1921年,狄爾斯和其研究生巴克(Back)研究偶氮二羧酸乙酯(半個世紀後因光延反應而在有機合成中大放光芒的試劑)與胺發生的酯變胺的反應,當他們用2-萘胺做反應的...
反應中不生成碳正離子,速率控制步驟是上述的協同步驟,反應速率與兩種物質的濃度成正比,因此稱為雙分子親核取代反應。 [1] 瓦爾登反轉光延反應 ...
典型的 SN2 反應和光延反應都伴有瓦爾登翻轉。它可以形象地與雨傘在大風作用下從裡向外翻轉的過程類比。Walden轉化意義 編輯 證實旋光性發生了反轉。...
1 DEAD 和三苯基膦是Mitsunobu反應(光延反應)中的試劑,其中 DEAD 是活性試劑,用作氫的接受體,而三苯基膦則為氧的接受體,反應後生成鍵能高的P=O 鍵。...
1921年,狄爾斯和其研究生巴克(Back)研究偶氮二羧酸乙酯(半個世紀後因光延反應而在有機合成中大放光芒的試劑)與胺發生的酯變胺的反應,當他們用2-萘胺做反應的...
1921年,狄爾斯和其研究生巴克(Back)研究偶氮二羧酸乙酯(半個世紀後因光延反應而在有機合成中大放光芒的試劑)與胺發生的酯變胺的反應,當他們用2-萘胺做反應的...
1921年,狄爾斯和其研究生巴克(Back)研究偶氮二羧酸乙酯(半個世紀後因光延反應而在有機合成中大放光芒的試劑)與胺發生的酯變胺的反應,當他們用2-萘胺做反應的...
1921年,狄爾斯和其研究生巴克(Back)研究偶氮二羧酸乙酯(半個世紀後因光延反應而在有機合成中大放光芒的試劑)與胺發生的酯變胺的反應,當他們用2-萘胺做反應的...
有機合成中很多反應,如Wittig、Staudinger和光延反應都會產生Ph3PO副產物,Ph3PCl2在轉化醇為氯代烴也會產生三苯基氧化膦:Ph3PCl2 + ROH → Ph3PO + HCl + ...
1921年,狄爾斯和其研究生巴克(Back)研究偶氮二羧酸乙酯(半個世紀後因光延反應而在有機合成中大放光芒的試劑)與胺發生的酯變胺的反應,當他們用2-萘胺做反應的...
1921年,狄爾斯和其研究生巴克(Back)研究偶氮二羧酸乙酯(半個世紀後因光延反應而在有機合成中大放光芒的試劑)與胺發生的酯變胺的反應,當他們用2-萘胺做反應的...
1 DEAD 和三苯基膦是Mitsunobu反應(光延反應)中的試劑,其中 DEAD 是活性試劑,用作氫的接受體,而三苯基膦則為氧的接受體,反應後生成鍵能高的P=O 鍵。 [1...
立體專一性,立體化學術語。當一個反應中,互為立體異構體的反應物分別生成立體特徵不同的產物時,此反應具有立體專一性。SN2反應和光延反應是典型的立體專一反應。...
1921年,狄爾斯和其研究生巴克(Back)研究偶氮二羧酸乙酯(半個世紀後因光延反應而在有機合成中大放光芒的試劑)與胺發生的酯變胺的反應,當他們用2-萘胺做反應的...
