基本介紹
- 中文名:乙醇解
- 外文名:ethanolysis
- 反應類型:親核取代反應
- 特點:乙醇既是溶劑又是反應試劑
釋義
鹵代烷的乙醇解反應
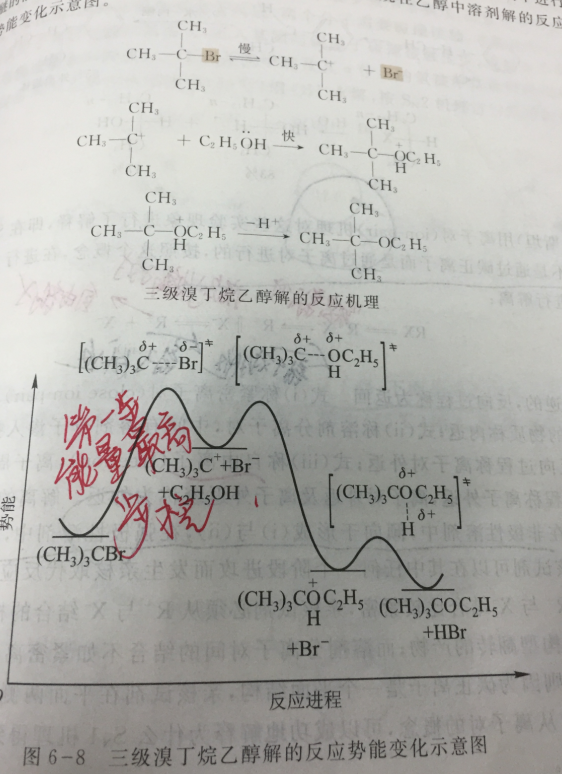
羧酸衍生物的乙醇解反應
乙腈為底物
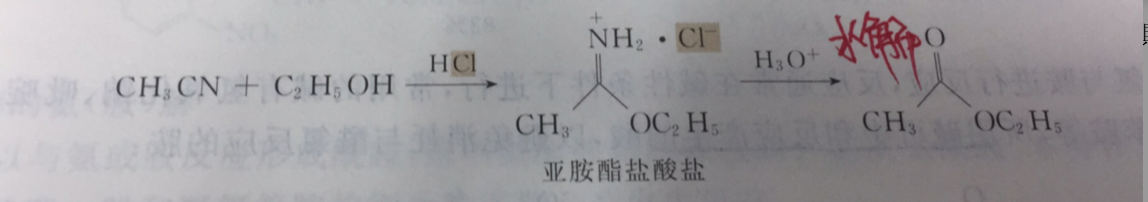
醯胺為底物
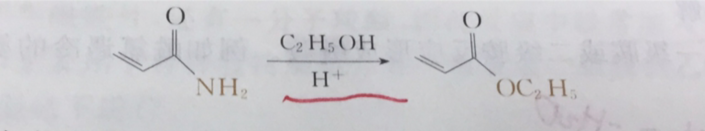
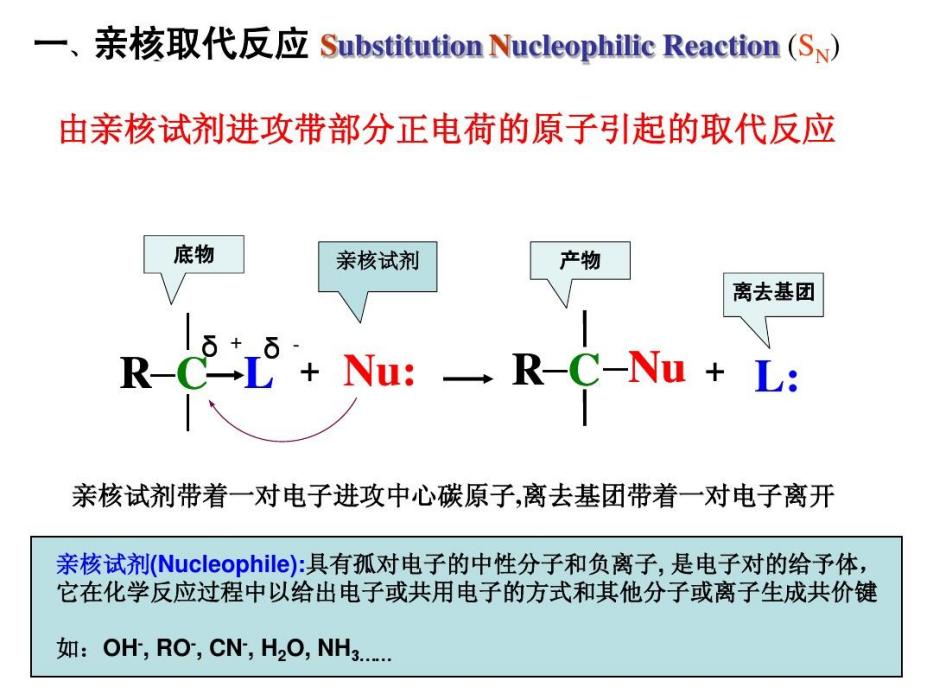



乙醇解隸屬於溶劑解反應的範疇。如果在反應體系中只有底物和溶劑,沒有另外加試劑,那么底物就將與溶劑發生反應,溶劑就成了試劑,這樣的反應稱為溶劑解反應,包括SN1、SN2反應。簡單的我們可以把乙醇解反應理解成溶劑乙醇作為親核...
乙醇的工業化生產從19世紀末開始發展起來,到第二次世界大戰期間發酵法生產乙醇達到了高峰。發酵法是經典的乙醇生產方法,在相當長的時期里是乙醇的主要來源。但是發酵法受到原料來源和成本高的限制,因此合成法逐漸興起。間接水合法制乙醇早...
大量實驗結果表明,用血液乙醇濃度BAC (Blood Alchol Concentration)來’表示中毒程度更為確切,並將酒精中毒稱之為酩酊,其中毒症狀的輕重大體與血液中所含乙醇濃度成正比,嚴重中毒時血醇濃度一般為200一350毫克/100毫升,中毒致死者血醇...
2-(2-丁氧基乙氧基)乙醇是一種化學品。物性數據 1. 性狀:無色液體,微有香味。2. 密度(g/mL,20/20ºC):0.9536 3. 熔點(ºC):-68 4. 沸點(ºC,常壓):231 5. 折射率(20ºC):1.4316 6. 黏度...
乙醇提取法是指利用乙醇的溶解性,將乙醇作為溶劑對物質進行分離提純的方法。在化學實驗、化工提純、化學製藥和中醫藥劑的製取等廣泛套用。發展歷史 2023年5月17日,據江南大學官方訊息,該校化學與材料工程學院劉小浩教授團隊創新性地採用...
2-(2-己氧基乙氧基)乙醇是一種化學品。物性數據 1. 性狀:無色液體。2. 密度(g/mL,20℃):0.932 3. 相對密度(20℃,4℃):0.9364 4. 熔點(ºC):-40.2 5. 沸點(ºC,常壓):249.1 6. 沸點(ºC,...
乙醇,俗稱酒精,套用最廣泛的一類醇。乙二醇,是最簡單和重要的二元醇,為帶有甜味的黏稠狀無色液體。丙三醇,俗稱甘油,是無色具有甜味的黏稠性液體,能與水混合,不溶於有機溶劑,有強烈的吸水性。正丁醇,為無色油狀液體,是重要...
工業酒精,即工業上使用的酒精,也稱變性酒精、工業火酒。工業酒精的純度一般為95%和99%。主要有合成和釀造(原煤或石油)兩種方式生產,合成的一般成本很低,乙醇含量高,釀造的工業酒精一般乙醇含量大於或等於95%,甲醇含量低於1%。成分 ...
酒精過敏其實是體內缺少乙醛轉化酶導致的一種外在皮膚過敏症狀反應。酒精過敏的兩個必要條件是過敏體質和酒精,過敏體質大多體內缺少乙醛轉化酶。酒精,也就是乙醇,在體內轉化成乙醛,因為體內缺少乙醛轉化酶,不能再轉化為乙酸排到體外,...
乙醇即我們平常所說的酒精,為無色芳香易揮發性液體,廣泛套用與工業、醫藥、家用製劑或酒類飲料。急性乙醇/酒精中毒多見於一次飲酒過多,即酗酒,由於一些社會原因,近年發病率有上升趨勢,而且由於不法分子用工業酒精兌制假酒,工業酒精...
無水乙醇(Ethanol absolute),是指純度較高的乙醇水溶液,是乙醇和水的混合物。一般情況下稱濃度99.5%的乙醇溶液為無水乙醇。成分 乙醇和水的混合物,一般為99.5%的乙醇溶液。乙醇的基本信息 中文名:乙醇;酒精;火酒 英文名:...
《乙醇的消去反應》是茂名市第一中學學校提供的微課課程,主講教師為鄧金鳳。 課程簡介 通過視頻驗證乙醇可以發生消去反應。設計思路 先介紹消去反應的定義,了解到乙醇可發生消去反應,再通過實驗視頻驗證,探究式講法學習乙醇的消去反應。
急性乙醇中毒乙醇又稱酒精,為無色易揮發易燃液體,成人LD50為5~8g/kg,易溶於水,能與大多數有機溶劑相溶。一次飲入過量酒精,可引起以神經精神症狀為主的疾病即為急性乙醇中毒或急性酒精中毒。臨床上分興奮期、共濟失調期、昏迷期...
燃料酒精是一種新能源,其優勢在於屬於可再生能源。 乙醇不僅是優良的燃料,它還是優良的燃油品改善劑。其優良特性表現為:乙醇是燃油的增氧劑,使汽油增加內氧,充分燃燒,達到節能和環保的目的;乙醇還可以經濟有效的降低芳烴、烯烴含量...
乙醇溶液,適應症為外用消毒。作用類別 本品為皮膚科用藥類非處方藥藥品。適應症 外用消毒。規格 75%(容量/容量)用法用量 用消毒棉球蘸取適量塗擦於需消毒的皮膚。不良反應 對皮膚有輕微刺激性。注意事項 1.不得用於皮膚破潰處。2...
乙醇發酵的主要代表菌為酵母菌,工業上主要用於釀酒和酒精生產。某些細菌,如運動發酵單胞菌也可以進行乙醇發酵。反應介紹 糖酵解途徑又稱EMP(Embden-Meyerhof Parnas)途徑,過一系列步驟,降解成三碳化合物(即丙酮酸,2 CH₃COCOOH)...
解酒(dispel the effects of alcohol),顧名思義,就是“醒酒”,使人從醉酒的狀態中醒過來,恢復意識或恢復自制力。通常不是自然清醒,而是採用酒前飲用解酒物質解酒,加速乙醛轉化,促進酒精分解,起到節約時間的目的、減小乙醇對人體...
靈芝用於解酒,目前是比較安全的。《本草綱目》記載靈芝有解百毒的作用。現代臨床研究,靈芝可以清除血中毒素,對受損的 肝臟細胞起修復營養的作用。研究發現,靈芝能幫助人體快速分解出乙醇脫氫酶和乙醛脫氫酶,可以快速分解人體內的酒精。
甲醇很輕、揮發性強、無色、易燃,並有與乙醇(飲用酒)非常相似的氣味。但不同於乙醇,甲醇毒性大,不可以飲用。通常用作溶劑、防凍劑、燃料或乙醇變性劑,亦可用於經過酯交換反應生產生物柴油。歷史 古埃及人在遺體保存技術防腐的過程...
意思是說,極性溶劑能夠溶解離子化合物以及能離解的共價化合物,而非極性溶劑則只能夠溶解非極性的共價化合物。比如,食鹽,是一種離子化合物,它能在水中溶解,卻不能在乙醇中溶解。在有機化學中一般會用到的溶劑有丙酮、乙醇、水和...
葛根可改善酒精導致的新陳代謝的異常。葛根有明顯的抗癌作用。常飲葛根製品能調節人體機能,增強和提高機體抗病能力,抗衰延年,永葆青春活力。山楂:現代科學研究證明,含山楂酸等多種有機酸,味酸甘,並含解脂酶,入胃後,能增強酶的...
微溶於冷水、己烷,溶於熱水、乙醇、乙醚、氯仿、苯、二硫化碳和松節油等。苯甲酸以游離酸、酯或其衍生物的形式廣泛存在於自然界中。主要用於製備苯甲酸鈉防腐劑,並用於合成藥物、染料,還用於制增塑劑、媒染劑、殺菌劑和香料等。可由...
《本草綱目》記載靈芝有解百毒的作用。現代臨床研究,靈芝可以清除血中毒素,對受損的 肝臟細胞起修復營養的作用。研究發現,靈芝能幫助人體快速分解出乙醇脫氫酶和乙醛脫氫酶,可以快速分解人體內的酒精,能使人從醉酒的狀態中,快速的醒...
alcohol thermometer[儀]酒精溫度計 ; 酒精溫度表 ; 火酒溫度計 雙語例句 1Wine contains about 10% alcohol.葡萄酒含有約10%的酒精。《牛津詞典》2He gave up the crutch of alcohol.他不再依賴酒精。《柯林斯英漢雙解大詞典》3...
