CRISPR-Cas9,一種基因治療法,這種方法能夠通過DNA剪下技術治療多種疾病。
2017年3月,英國《自然·通訊》雜誌發表一項遺傳學重要研究成果,利用CRISPR-Cas9系統可拯救失明小鼠。
基本介紹
- 外文名:CRISPR-Cas9
- 屬性:基因治療法
- 作用:治療多種疾病
- 原理:DNA剪下技術
研製經過

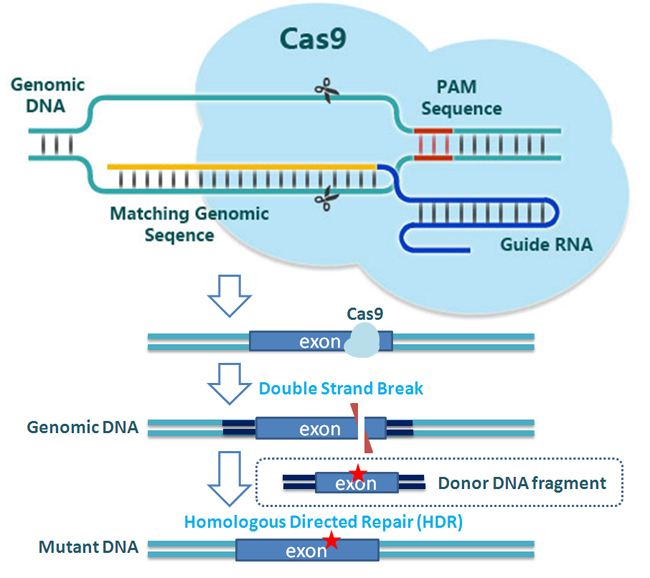
crispr/cas9一般指本詞條
CRISPR-Cas9,一種基因治療法,這種方法能夠通過DNA剪下技術治療多種疾病。
2017年3月,英國《自然·通訊》雜誌發表一項遺傳學重要研究成果,利用CRISPR-Cas9系統可拯救失明小鼠。

CRISPR(/'krɪspər/,Clustered regularly interspaced short palindromic repeats)是原核生物基因組內的一段重複序列,是生命進化歷史上,細菌和病毒進行鬥爭產生的...
CRISPR-Cas9,一種基因治療法,這種方法能夠通過DNA剪下技術治療多種疾病。2017年3月,英國《自然·通訊》雜誌發表一項遺傳學重要研究成果,利用CRISPR-Cas9系統可拯救...
CRISPR/Cas9 是細菌和古細菌在長期演化過程中形成的一種適應性免疫防禦,可用來對抗入侵的病毒及外源DNA。CRISPR/Cas9 系統通過將入侵噬菌體和質粒 DNA 的片段整合到...
(clustered regularly interspaced short palindromic repeat sequences,即CRISPR序列,這就是二十多年前日本科學家發現的那個序列)和CRISPR相關基因(CRISPR-associated ...
CRISPR/Cas系統,全名為常間回文重複序列叢集/常間回文重複序列叢集關聯蛋白系統(clustered regularly interspaced palindromic repeats/CRISPR-associated proteins),為目前...
CRISPR靶向特異性是由兩部分決定的,一部分是RNA嵌合體和靶DNA之間的鹼基配對,另一部分是Cas9蛋白和一個短DNA序列,這個短的DNA序列通常在靶DNA的3'末端作用,被稱...
張鋒,男,1982年出生於河北石家莊,史丹福大學化學及生物工程博士,是當今最為人所關注的華人生物學家之一。他最著名的工作是基因修飾技術CRISPR-Cas9的發展和套用,率先...
賀建奎擁有多學科交叉的背景,並在基因測序儀研究, CRISPR基因編輯,生物信息學等多個領域取得研究突破。他的實驗室將高通量測序套用到免疫細胞受體庫的多樣性研究。201...
基因編輯技術指能夠讓人類對目標基因進行“編輯”,實現對特定DNA片段的敲除、加入等的一項技術。而CRISPR/Cas9技術自問世以來,就有著其它基因編輯技術無可比擬的優勢...
有專家評論,儘管這種技術尚處於初期階段,但其潛力有望超過近來被看作諾貝爾獎熱門的CRISPR-Cas9技術。 [1] 2016年11月,《自然-生物技術》就韓春雨論文爭議發表了...
2016 CRISPR/Cas技術在植物基因組編輯上的套用研究 馮爭艷 中國科學院大學 博士 2016 CRISPR/Cas9技術在植物中的套用與發展 陸鈺明 中國科學院大學 博士後 2016 diR...
2016年8月,盧鈾領導一個中國科學家團隊將開展全球首例對人體使用革命性基因編輯技術CRISPR的試驗。該團隊計畫於今年8月開始在肺癌患者身上測試經過CRISPR技術編輯的細胞...
Synthego的旗艦產品CRISPRevolution是合成RNA系列產品,用於CRISPR基因編輯和研究設計實驗中,旨在提高基因編輯實驗效率、降低實驗成本。2016年8月,真格基金投資了這家美國...
1、研究TALEN和CRISPR基因編輯技術的特性,提高其效率和特異性。2、在造血幹細胞和T細胞中建立和最佳化基因編輯技術,開發新型疾病治療方法。...
林帥亮,北京大學、清華大學和北京生命科學研究所聯合培養項目博士生。 2016年8月,一封來自張峰實驗室前工作人員林帥亮倒戈的郵件被公開,讓CRISPR的專利之爭升級。這是...
