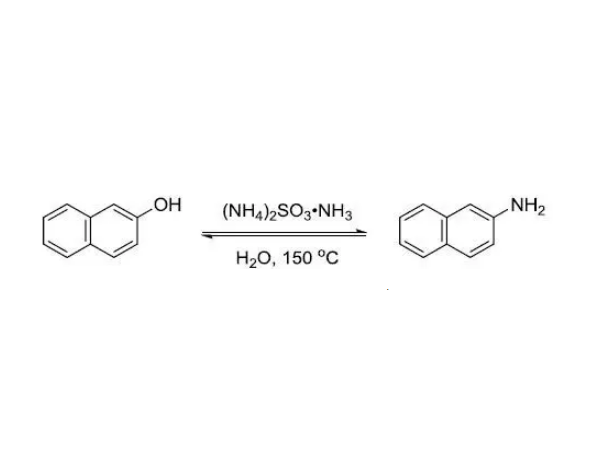
Bucherer反應的機理為加成消除過程。
在間苯二酚、萘酚和萘胺以及它們的衍生物的合成中,Bucherer反應舉足輕重,隨著染料及醫藥領域對萘胺、苯胺的需求不斷增加,氨解、烷基化反應成為Bucherer反應及它的延伸反應的熱點。
基本介紹
- 中文名:Bucherer反應
- 機理:加成消除
- 主要產品:萘酚,萘胺及衍生物
- 主要領域:染料及醫藥
反應機理,套用實例,
反應機理
本反應機理是加成消除反應 ,反應分為4步,以萘酚為例。
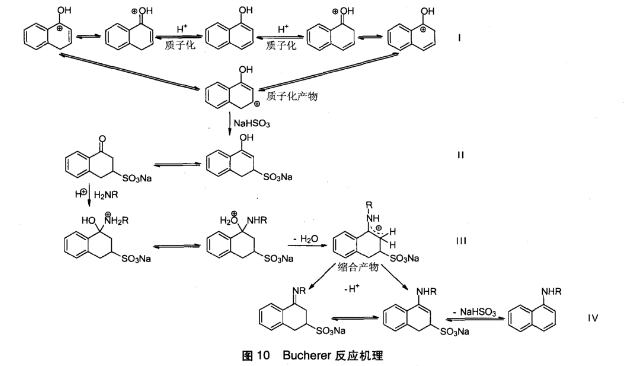 反應機理
反應機理(I)質子化效應:一個質子與萘酚電子云密 度較強的C-2或C-4相結合,質子化後有五種共振式產物,再通過環脫芳構化得到更穩定的酮式,;(II)烯醇一酮互變異構過程:一個亞硫酸氫根離子加到質 子化產物的C-3上,經烯醇一酮互變異構得到更為穩定的四氫萘酮-3-磺酸鈉;(III)羰基一胺縮合反應:四氫萘酮-3-磺酸鈉與胺按照羰基化合物一胺縮合反應,發生羰基親核加成並失水,得到受共振穩定的正離子型縮合產物;(IV)去質子化效應:正 離子型縮合產物去質子化得到烯胺及亞胺,最後烯胺消除亞硫酸氫鈉,重新芳構化,生成萘胺。
套用實例
1、氧化石墨烯(GO)的選擇性氨解
Hu和Ho等在NaHSO3水溶液中通入氨氣,控制溫度150-240℃,反應5-24h。反應為一步氨解反應,反應簡單、容易控制,是現在石墨烯氨化的主要製備方法。
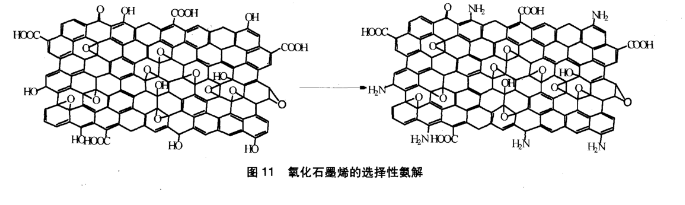 氧化石墨烯(GO)的選擇性氨解
氧化石墨烯(GO)的選擇性氨解2、萘酚衍生物的合成
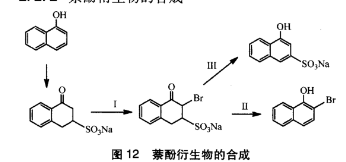 萘酚衍生物的合成
萘酚衍生物的合成其中,萘酚在NaHSO3中先進行烯醇-酮互變形成穩定的四氫萘酮-3-磺酸鈉,在(I)溴化後形成2-溴-1-四氫萘酮-3-磺酸鈉;在強鹼環境中通 過(II)過程失去-分子NaHSO 得到2-溴-α-萘酮;在少量的有機鹼存在時,可以通過(IlI)過程消去一分子HBr得到1-羥基-萘酮-3-磺酸鈉。這些萘酚的衍生物在染料、醫藥中有廣泛的用途。