在氧化還原反應中,氧化劑與還原產物、還原劑與氧化產物各自組成共軛的氧化還原體系,這種共軛的氧化還原體系,我們稱之為氧化還原電對,簡稱電對。
基本介紹
- 中文名:氧化還原電對
- 外文名:Redox pair
- 簡稱:電對
概念解釋
在氧化還原反應中,氧化劑在反應過程中氧化數降低,其產物具有較低的氧化數,具有弱還原型,是一個弱還原劑;還原劑在反應過程中氧化數升高,其產物具有較高的氧化數,具有弱氧化性,是一個弱氧化劑。氧化劑與還原產物、還原劑與氧化產物各自組成的兩個共軛的氧化還原體系,這種共軛的氧化還原體系,我們稱之為氧化還原電對,簡稱電對。
例如:鋅與銅離子反應生成鋅離子和銅單質的反應中,鋅離子與鋅組成一個電對,銅離子與銅組成一個電對。
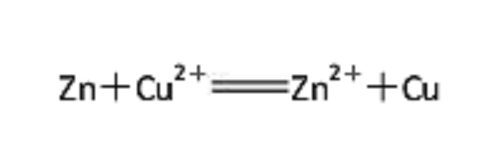
電對通常寫成如下形式:
氧化劑/還原產物 或 氧化產物/還原劑
在氧化還原電對中,氧化數高的物質叫做氧化型物質,氧化數低的物質叫做還原型物質。例如上面反應式中銅離子的氧化數較高,為氧化劑,而鋅作為還原劑。
此外,我們可以說:氧化還原反應是兩個(或兩個以上)氧化還原電對共同作用的結果。
在對某些劇烈與水反應而不能直接測定的電極,可通過熱力學數據用間接方法來計算標準電極電勢。而標準電極電勢是表示在標準條件下。所謂標準條件,則要求之一為:電對的[氧化型]/[還原型]=1或[Mn+]=1mol·dm-3等
