基本介紹
- 中文名:阿倫尼烏斯方程
- 外文名:Arrhenius equation
- 又稱:阿龍尼烏斯方程
- 提出者:瑞典化學家阿倫尼烏斯
- 形式:k=A·exp(-Ea/RT)(指數式)
提出
形式
微分形式

定積分形式



指數形式

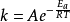
適用性


精確性








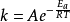




阿累尼烏斯方程又稱為阿倫尼烏斯方程,是化學動力學的重要公式,由瑞典的阿倫尼烏斯所創立的化學反應速率常數隨溫度變化關係的經驗公式。該公式具有三種不同的表達式,即:...
阿倫尼烏斯公式(Arrhenius equation )是由瑞典的阿倫尼烏斯所創立的化學反應速率常數隨溫度變化關係的經驗公式。 公式寫作 k=Ae-Ea/RT (指數式)。k為速率常數,R為...
學術成果,解釋溶液中的元素是如何被電解分離的現象,研究過溫度對化學反應速度的影響,得出著名的阿倫尼烏斯公式。還提出了等氫離子現象理論、分子活化理論和鹽的水解...
提出了電解質在水溶液中電離的阿倫尼烏斯理論,研究了溫度對化學反應速率的影響,得出阿倫尼烏斯方程。由於在物理化學方面的傑出貢獻,被授予1903年諾貝爾化學獎。 尼烏斯...
它是物理和化學之間的一座橋樑(見阿倫尼烏斯電離理論)。 阿倫尼烏斯的研究領域廣泛。1889年提出活化分子和活化熱概念,導出化學反應速率公式(阿倫尼烏斯方程)。他還研究...
它是物理和化學之間的一座橋樑(見阿倫尼烏斯電離理論)。阿倫尼烏斯的研究領域廣泛。1889年提出活化分子和活化熱概念,導出化學反應速率公式(阿倫尼烏斯方程)。他還研究...
表示這一反應的速率常數,與溫度、離子活度、光照、固體反應物的接觸面積、反應活化能等因素有關,通常可通過阿累尼烏斯方程計算出來,也可通過實驗測定。指數 、 為反...
提出了電解質在水溶液中電離的阿倫尼烏斯理論,研究了溫度對化學反應速率的影響,得出阿倫尼烏斯方程。由於在物理化學方面的傑出貢獻,被授予1903年諾貝爾化學獎。...
阿倫尼烏斯公式k=A·exp(-Ea/RT)中,k、R、T、Ea分別是化學反應速率常數、摩爾氣體常數、反應溫度及活化能,式中的A稱為指前因子。它是一個只由反應本性決定...
(阿倫尼烏斯公式中的活化能區別於由動力學推導出來的活化能,又稱阿倫尼烏斯活化能或經驗活化能)活化分子的平均能量與反應物分子平均能量的差值即為活化能。...
非活化分子轉變為活化分子所需吸收的能量為活化能的計算可用阿倫尼烏斯方程求解。阿倫尼烏斯方程反應了化學反應速率常數K隨溫度變化的關係。在多數情況下,其定量規律可...
1.阿侖尼烏斯方程微分式:指數式:積分式:式中,A稱為指前因子或表觀頻率因子,其單位與k相同;Ea稱為阿累尼烏斯活化能(簡稱活化能),其單位為kJmol-1。上述三...
相對反應速率是假定100°C(373°K)時的反應速率為1,按阿累尼烏斯方程計算得到的不同溫度下的相對反應速率K:lnK=B-A/TK=ln^-1(43.2-16113/T)按照蒸煮曲線...
阿累尼烏斯方程及計算(活化能的概念與計算;速率常數的計算;溫度對速率常數影響的計算等)。活化能與反應熱的關係。反應機理一般概念。推求速率方程。催化劑對反應影響...
一級反應(的積分式)的有關計算(速率常數、半衰期、C-14法推斷年代等);阿累尼烏斯方程及其有關計算(阿累尼烏斯活化能的概念與計算;速率常數的計算;溫度對速率常數...
活化能/阿累尼烏斯電離理論/阿累尼烏斯方程/反應熱 1904年度 威廉·拉姆塞 稀有氣體/氦、氖、氬、氯、氙、氡的發現 1905年度 阿道夫·馮·拜耳 酚酞/染料...
▪ 阿累尼烏斯方程 ▪ 氨 ▪ 螯合劑 ▪ 螯合物 ▪ 螯合物 ▪ 半反應 ▪ 半微量分析 ▪ 苯 ▪ 比色分析 ▪ 變異係數 ▪ 標定 ▪ ...
均勻化處理過程是熱激活過程,所以原子擴散係數遵循阿累尼烏斯方程的規律:D=Doexp(一Q/RT)。因此,為加速均勻制過程,應儘可能提高均勻化處理溫度。通常採用的均勻化...
阿累尼烏斯方程及計算(活化能的概念與計算;速率常數的計算;溫度對速率常數影響的計算等)。活化能與反應熱的關係。反應機理一般概念。推求速率方程。催化劑對反應影響...
對指數函式可取其對數作圖,則仍為線性關係,例如,反應速率常數k與活化能Ea的關係式(阿累尼烏斯公式)k=Aexp(-Ea/RT)若根據不同溫度T下的k值,作1nk對1/T的圖...
