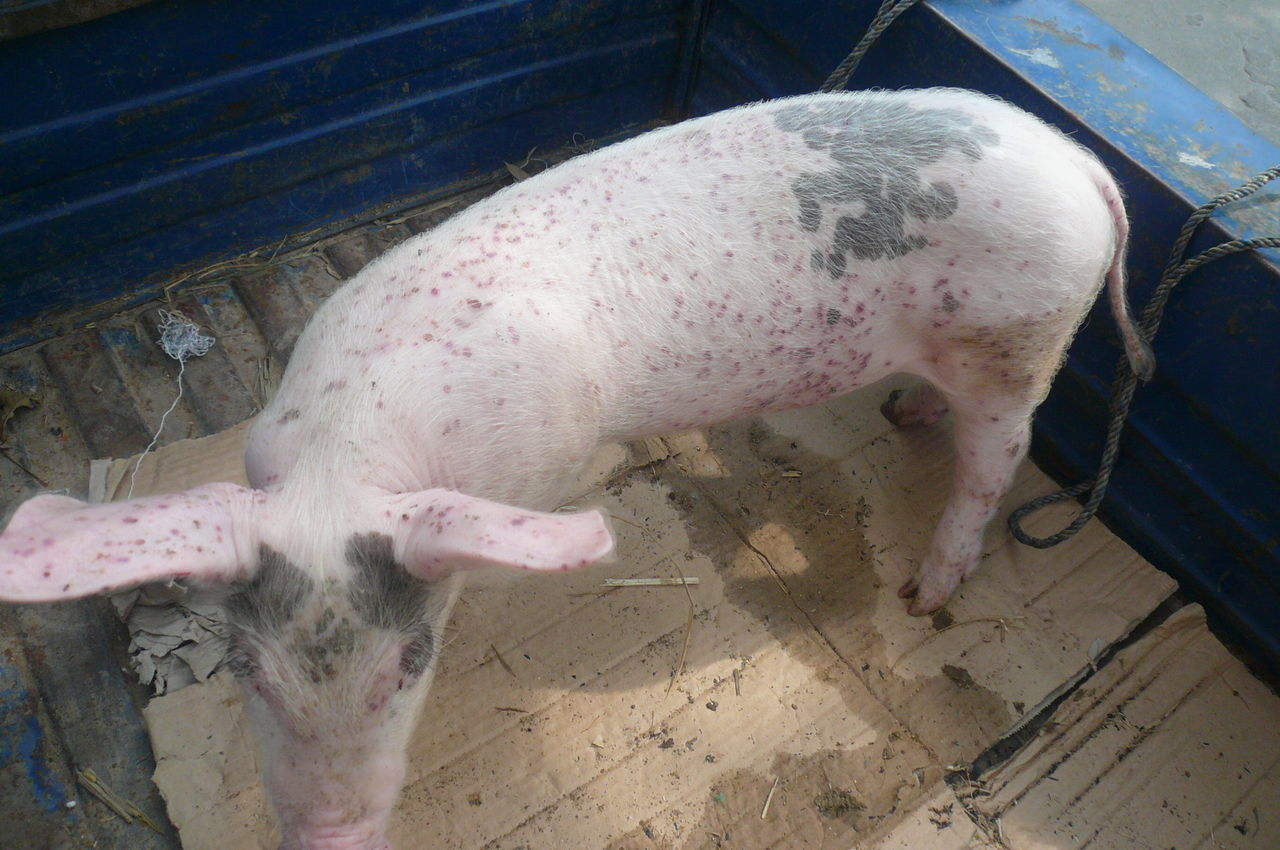
形態與理化特性
豬圓環病毒(Porcine circovirus,縮寫:PCV)是迄今發現的一種最小的動物病毒。現已知PCV有兩個血清型,即PCV1和PCV2。PCV1為非致病性的病毒。PCV2為致病性的病毒,它是斷奶仔豬多系統衰竭綜合徵(Postweaning Multisystemic Wasting Syndrome,PMWS)的主要病原。本病最早發現於
加拿大(1991),很快在歐美及亞洲一些國家包括我國發生和流行,除PMWS外,PDNS(豬皮炎與腎病綜合徵)、PNP(增生性壞死性肺炎)、PRDC(
豬呼吸道疾病綜合徵)、繁殖障礙、先天性顫抖、腸炎等疾病亦與PCV2感染有重要關聯。PCV2及其相關的豬病,死亡率10%~30%不等,較嚴重的豬場在暴發本病時死淘率高達40%,給養豬業造成嚴重的經濟損失。現已被世界各國的獸醫與養豬業者公認為是繼
豬繁殖與呼吸綜合徵(PRRS)之後新發現的引起豬免疫障礙的重要傳染病。
1974年,
德國人Tischer發現,豬圓環病毒(PCV)為二十面體對稱、無囊膜、單股環狀DNA病毒。病毒粒子直徑為17 nm,是目前發現的最小的動物病毒。
PCV對外界的抵抗力較強,在pH 3的酸性環境中很長時間不被滅活。該病毒對氯仿不敏感,在56 ℃或70 ℃處理一段時間不被滅活。在高溫環境也能存活一段時間。不凝集牛、羊、豬、雞等多種動物和人的紅細胞。
發病機制
在病豬鼻黏膜、
支氣管、
肺臟、
扁桃體、腎臟、脾臟和小腸中有PCV粒子存在。胸腺、脾、
腸系膜、支氣管等處的
淋巴組織中均有該病毒,其中肺臟及淋巴結中
檢出率較高。表明PCV嚴重侵害豬的免疫系統:病毒與巨噬細胞/
單核細胞、組織細胞和胸腺巨噬細胞相伴隨,導致患豬體況下降,形成
免疫抑制。由於
免疫抑制而導致
免疫缺陷,其臨床表現為:對低致病性或減弱疫苗的微生物可以引發疾病;重複發病對治療無應答性;對
疫苗接種沒有充分免疫應答;在一窩豬中有一頭以上發生無法解釋的出生期發病和死亡;豬群中同時有多種疾病綜合徵發生。這些特徵在PMWS的豬群中基本上都有不同程度的發生。
淋巴細胞缺失和
淋巴組織的巨噬細胞浸潤,是PMWS病豬的獨特性病理損害和基本特徵。而且此特徵與血液循環中B及T細胞減少和
淋巴器官中這類細胞的減少呈高度相關;與周圍血液和
淋巴組織中巨噬細胞/單核細胞譜系細胞的增加呈高度相關。另外已證實
淋巴組織、相關免疫細胞和血液中的細胞存在大量的PCV2抗原。
流行病學
PMWS是最早被認識和確認的由PCV2感染所致的疾病。常見的PMWS主要發生在5~16
周齡的豬,最常見於6~8周齡的豬,極少感染乳豬。一般於斷奶後2~3天或1周開始發病,急性發病豬群中,病死率可達10%,耐過豬後期發育明顯受阻。但常常由於並發或繼發細菌或病毒感染而使死亡率大大增加,病死率可達25%以上。血清學調查表明,PCV在世界範圍內流行。在
德國和
加拿大,豬群中PCV抗體陽性率分別高達95%和55%,在
英國和愛爾蘭,豬群中PCV抗體陽性率分別高達86%和92%,但不一定表現PMWS症狀。在我國對部分省市豬群檢測,20日齡未斷奶仔豬陽性率為0,1~2月斷奶仔豬陽性率為16.5%,後備母豬陽性率為42.3%,經產母豬陽性率為85.6%,肥育豬陽性率為51%,總陽性率為42.9%。臨床症狀可能在幾個月內持續存在,在6~12個月達到高峰,接著下降;一群與另一群之間的感染有很大差別,因為乳豬體內母源的PCV抗體在其出生後8~9
周齡時消失,而小豬轉移到育肥圈時(11~13周齡)又接觸了PCV,PCV抗體又出現了。
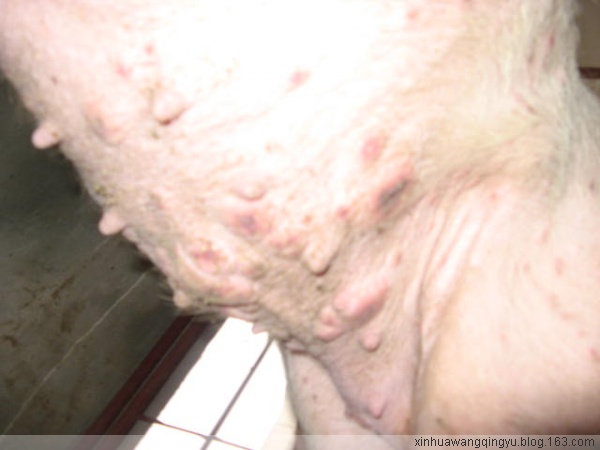 豬圓環病毒病
豬圓環病毒病傳播途徑
豬對PCV2具有較強的易感性,感染豬可自鼻液、糞便等廢物中排出病毒,經口腔、呼吸道途徑感染不同年齡的豬。懷孕母豬感染PCV2後,可經胎盤垂直傳播感染仔豬。人工感染PCV2血清陰性的公豬後精液中含有PCV2的DNA,說明精液可能是另一種傳播途徑。用PCV2人工感染試驗豬後,其他未接種豬的同居
感染率是100%,這說明該病毒可水平傳播。豬在不同豬群間的移動是該病毒的主要傳播途徑,也可通過被污染的衣服和設備進行傳播。
工廠化養殖方式可能與本病有關,飼養管理不善、惡劣的斷奶環境、不同來源及年齡的豬混群、飼養密度過高及刺激仔豬免疫系統均為誘發本病的重要危險因素,但豬場的大小並不重要。
PCV感染試驗動物,發現只有豬產生特異性抗體,而兔、鼠、牛,甚至人均為血清學陰性。
PCV1對豬無致病性,但能產生
血清抗體,並且在調查的豬群中普遍存在。
PCV2可引起斷奶仔豬多系統衰竭綜合徵(PMWS),並多發於5~16
周齡的豬。
PCV能水平傳播,接觸病毒後一周, 血清中能檢出抗體,隨後滴度不斷升高。
臨床症狀
與PCV2感染有關的疾病主要有如下幾種。
PMWS的臨床症狀
最常見的是豬只漸進性消瘦或生長遲緩,這也是診斷PMWS所必需的臨床依據,其他症狀有厭食、精神沉鬱、行動遲緩、皮膚蒼白、被毛蓬亂、呼吸困難,咳嗽為特徵的呼吸障礙。較少發現的症狀為腹瀉和
中樞神經系統紊亂。發病率一般很低而病死率都很高。體表淺淋巴結腫大,腫脹的淋巴結有時可被觸摸到,特別是腹股溝淺淋巴結;貧血和可視黏膜黃疸。在一頭豬可能見不到上述所有臨床症狀,但在發病豬群可見到所有的症狀。
胃潰瘍、嗜睡、
中樞神經系統障礙和突然死亡較為少見。絕大多數PCV2是亞臨床感染。一般臨床症狀可能與繼發感染有關,或者完全是由繼發感染所引起的。在通風不良、過分擁擠、空氣污濁、混養以及感染其他病原等因素時,病情明顯加重,一般病死率為10%~30%。
先天性顫抖的症狀
顫抖由輕微到嚴重不等,一窩豬中感染的數目也變化較大。嚴重顫抖的病仔豬常在出生後1周內因不能吮乳而飢餓致死。耐過1周的乳豬能存活,3
周齡時康復。顫抖是兩側性的,乳豬躺臥或睡眠時顫抖停止。外部刺激如突然聲響或寒冷等能引發或增強顫抖。有些豬一直不能完全康復,整個生長期和育肥期繼續顫抖。發病窩豬常為新引入的年輕種豬所生,這表明這些血清學陰性種豬在懷孕的關鍵期接觸了PCV。
常見的混合感染
PCV感染可引起豬的
免疫抑制,從而使機體更易感染其他病原,這也是圓環病毒與豬的許多疾病混合感染有關的原因。最常見的混合感染有PRRSV、PRV(偽
狂犬病毒)、PPV(
細小病毒)、
肺炎支原體、多殺性巴氏桿菌、PEDV(流行性腹瀉病毒)、SIV(
豬流感病毒),有的呈二重感染或三重感染,其病豬的病死率也將大大提高,有的可達25%~40%。
病理變化
剖檢病變
本病主要的病理變化為患豬消瘦,貧血,皮膚蒼白,黃疸(疑似PMWS的豬有20%出現);淋巴結異常腫脹,內臟和外周淋巴結腫大到正常體積的3~4倍,切面為均勻的白色;肺部有灰褐色炎症和腫脹,呈瀰漫性病變,比重增加,堅硬似橡皮樣;肝臟發暗,呈淺黃到橘黃色外觀,萎縮,肝小葉間結締組織增生;腎臟水腫(有的可達正常的5倍),蒼白,被膜下有壞死灶;脾臟輕度腫大,質地如肉;胰、小腸和結腸也常有腫大及壞死病變。
組織學病變
病變廣泛分布於全身器官、組織,廣泛性的病理 損傷。肺有輕度多灶性或高度瀰漫性間質性肺炎;肝臟有以
肝細胞的單細胞壞死為特徵的肝炎;腎臟有輕度至重度的多灶性間質性腎炎;心臟有多灶性心肌炎。在
淋巴結、脾、扁桃體和胸腺常出現多樣性
肉芽腫炎症。PMWS病豬主要的病理組織學變化是淋巴細胞缺失。
診斷
本病的診斷必須將臨床症狀、病理變化和實驗室的病原或抗體檢測相結合才能得到可靠的結論。最可靠的方法為病毒分離與鑑定。
病理學檢查
此法在病豬死後極有診斷價值。當發現病死豬全身淋巴結腫大,肺退化不全或形成固化、緻密病灶時,應懷疑本病。可見
淋巴組織內淋巴細胞減少,
單核吞噬細胞類細胞浸潤及形成多核巨細胞,若在這些細胞中發現嗜鹼性或兩性染色的細胞質內包涵體,則基本可以確診。
血清學檢查
是生前診斷的一種有效手段。診斷本病的方法有:
間接免疫螢光法(IIF),免疫過氧化物單層培養法,ELISA方法,
聚合酶鏈式反應(PCR)方法,核酸探針雜交及原位雜交試驗(ISH)等方法。
1 IIF方法 宜檢測細胞培養物中的PCV。用組織病料以蓋玻片在PK-15細胞培養,丙酮固定,用兔抗PCV高免血清與細胞培養物中的PCV反應,可對PCV進行檢測和分型。
2 ELISA診斷方法 可用於檢測血清中的病毒抗體。用細胞培養的病毒(PCV2)作為抗原,用PCV2特異性單克隆抗體作為競爭試劑建立競爭ELISA方法,競爭ELISA方法的
檢出率為99.58%,而
間接免疫螢光法的檢出率僅為97.14%。該方法可用於PCV2抗體的大規模監測。
3 PCR方法 是一種快速、簡便、特異的診斷方法。採用PCV2特異的或群特異的引物從病豬的組織、鼻腔分泌物和糞便進行基因擴增,根據擴增產物的限制酶切圖譜和鹼基序列,確認PCV感染,還有一種簡單的複合PCR(multiplex PCR)法。
4 ISH方法 此法可以檢查PCV核酸。但不能區分PCV1和PCV2,具有群特異性,可以精確定位PCV在組織器官中的部位,可用於檢測臨診病料和病理分析。
臨床診斷要點
(1)PMWS主要發生在5~16
周齡的豬,斷奶前生長發育良好。(2)同窩或不同窩仔豬有
呼吸道症狀,腹瀉、
發育遲緩、體重減輕。有時出現皮膚蒼白或黃疸。抗生素治療無效或療效不佳。(3)剖檢淋巴結腫大,脾腫、肺膨大,間質變寬,表面散在大小不等的褐色突變區。其他臟器也可能有不同程度的病變和損傷。
斷乳期:豬圈小,原則上一窩一圈,豬圈分隔堅固;堅持嚴格的全進全出,並有與鄰舍分割的獨立糞尿排出系統;降低飼養密度:>0.33 m2/豬;增加餵料器空間:>7 cm/
仔豬;改善空氣品質:NH3<10×10-6,CO2<0.1%,相對濕度<85%;豬舍溫度控制和調整:3
周齡仔豬為28 ℃,每隔一周調低2 ℃,直至常溫;批與批之間不混群。
生長育肥期:豬圈小,壁式分隔;堅持嚴格的全進全出、空欄、清洗和消毒制度;從斷奶後豬圈移出的豬不混群;整個育肥圈豬不再混群;降低飼養密度:>0.75 m2/豬;改善空氣品質和溫度。
其他:適宜的疫苗接種計畫;保育舍要有獨立的飲水加藥設施;嚴格的保健措施(
斷尾、斷齒、注射時嚴格消毒);將病豬及早移到治療室或撲殺。
預防和控制
(1)採用抗菌藥物,減少並發感染。如氟苯尼考、
丁胺卡那黴素、慶大-小諾黴素、克林黴素、磺胺類藥物等進行治療,同時套用促進腎臟排泄和緩解類藥物進行腎臟的回覆治療。
(2)採用
黃芪多糖注射液並配合維生素B1+B12+Vc肌肉注射,也可以使用佳維素或氨基金維他飲水或拌料。
(3)選用新型的抗病毒劑如
干擾素、白細胞介導素、
免疫球蛋白、轉移因子等進行治療,同時配合中草藥抗病毒製劑,會取得明顯治療效果。
 豬圓環病毒病
豬圓環病毒病