燃料在定容或定壓下燃燒時,其產生的熱量常分為兩個部分:一部分傳給周圍環境,一部分使燃燒產物加熱,溫度升高。傳給外界的熱量越少,燃燒產物的溫度越高。當傳給外界的熱量為零,即實現絕熱的完全燃燒時,燃燒產物的溫度達到最大值,這時燃燒產物所達到的溫度稱為絕熱論燃燒溫度或理想燃燒溫度。
基本介紹
- 中文名:理想燃燒溫度
- 外文名:Ideal burning temperature
- 領域:熱力學
- 別稱:絕熱論燃燒溫度
- 分類:定容、定壓理想燃燒溫度
簡介,相關計算,確定理想燃燒溫度,定容理想燃燒溫度,
簡介
燃料在定容或定壓下燃燒時,其產生的熱量常分為兩個部分:一部分傳給周圍環境,一部分使燃燒產物加熱,溫度升高。傳給外界的熱量越少,燃燒產物的溫度越高。當傳給外界的熱量為零,即實現絕熱的完全燃燒時,燃燒產物的溫度達到最大值,這時燃燒產物所達到的溫度稱為絕熱論燃燒溫度或理論燃燒溫度。此處的完全燃燒包括兩方面的含義,一方面是指燃料被氧化至最高價氧化物,即充分燃燒;另一方面是指燃料的燃燒率為100%。
“理想燃燒溫度”,在一些燃燒學和化學熱力學的書中又常常被稱之為“理想火焰溫度”,它是許多燃燒問題中的一個相當重要的熱力學量。
“理想燃燒溫度”或“理想火焰溫度”的定義,在各有關資料中不外乎被敘述為這樣兩種形式。第一種是:“若混合氣經過絕熱等壓過程達到化學平衡,則系統最終達到的溫度稱理想火焰溫度或燃燒最大溫度”;第二種是:“如果令一化合物在絕熱狀況下完全燃燒。以使放出的熱全部用於加熱產生的氣體,則所達到的溫度叫做絕熱火焰溫度”。儘管這兩種定義的敘述內容不同,但目前各種書籍、資料中對這兩種定義的理想燃燒溫度的計算方法完全一樣,或者說都是按第一種定義的內容進行計算的。
從熱力學觀點分析,上述兩定義敘述兩種不同的概念。前者描述了一個絕熱容器中,反應物經化學反應生成平衡產物過程中釋放的熱量全部用來加熱系統,使系統達到的溫度。顯然隨著氧和燃料混合比例的變化,系統的最高溫度也發生變化。表示了這種變化關係,圖中T和功分別為理論最高燃燒溫度及相應的燃料空氣混合比和當量的燃料空氣混合比的比值。

而後者,它描述的是一個在絕熱環境中的系統,其燃料在當量空氣(或其它氧化劑)下經過化學反應生成平衡產物過程中釋放的熱量全部用來加熱系統,使系統達到的溫度。它和一個實際絕熱容器中,燃料和氧的實際混合情況無關,即和叻無關。因此,這兩種定義所得到的溫度並不相同,只是 的特例下,兩者的數值才一樣。
的特例下,兩者的數值才一樣。

相關計算
確定理想燃燒溫度
在確定理想燃燒溫度時,假定燃料及助燃物的最初溫度均為25℃。經過定壓絕熱燃燒後,由於與外界沒有熱交換,燃料的燃燒熱全部被用來加熱生成物。此時有:

式中: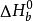 為燃料的標準燃燒熱;
為燃料的標準燃燒熱;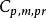 為燃燒反應完成後系統所包含的混合物的摩爾定壓熱容;
為燃燒反應完成後系統所包含的混合物的摩爾定壓熱容;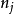 、
、 分別為燃燒產物中第j組元的摩爾數的摩爾定壓熱容;
分別為燃燒產物中第j組元的摩爾數的摩爾定壓熱容; 為理論燃燒溫度;T0=298K。利用上式可以求出燃料定壓燃燒時的理想燃燒溫度。
為理論燃燒溫度;T0=298K。利用上式可以求出燃料定壓燃燒時的理想燃燒溫度。
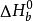
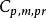
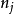


定容理想燃燒溫度
對於定容燃燒,也可以用相似的方法求得定容理想燃燒溫度,即



