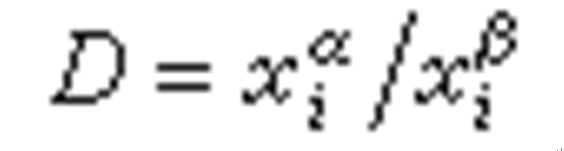液液平衡(英文名稱liquid-liquid equilibrium)是一種物理現象,在一定溫度和壓力下,兩個組分不同的液相經過充分接觸後,某些組分在這兩液相中的濃度不再發生變化,表明這些組分在這兩相間的正反傳遞速率相等,達到了液-液平衡。例如水和苯是兩個液相,當水和苯共存時,存在明顯的液相分界面,下層水中溶有少量苯,上層苯中也溶有少量水,兩者部分互溶,形成具有兩個液相的二元體系。在一定溫度和壓力下,使其充分混合接觸,直到兩個液相的組成恆定,即水中溶解苯的量和苯中溶解水的量不變,即認為水和苯兩個液相達到該溫度和壓力下的液-液平衡。
液-液平衡是物質的一種物理性能,自然界廣泛存在的一種物理現象和規律。在化學化工中利用物質的這種性能和規律可以通過各種化工過程提取、分離、濃縮、精製產品。
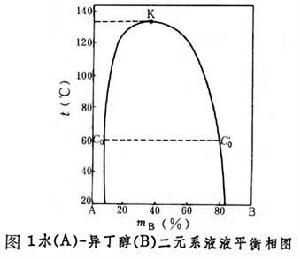 相關圖片
相關圖片