專利背景
碳青黴烯類抗生素是20世紀70年代發現、90年代發展起來的一類新型的非典型β-內醯胺類廣譜抗生素。碳青黴烯類藥物對革蘭陰性菌的外膜透過性很好,也能適度透過革蘭陽性菌的胞壁粘肽層,屬廣譜抗菌藥物。碳青黴烯抗生素能與革蘭陰性菌的PBP-2與PBP-3結合,或者與革蘭陽性菌的PBP-1與PBP-2結合顯示出很強的殺菌活性。碳青黴烯抗生素對大多數β-內醯胺酶穩定,對超廣譜β-內醯胺酶(ESBLs)亦穩定,分子中的β-內醯胺環不容易被β-內醯胺酶水解失活。
第一個上市的碳青黴烯類抗生素是默克公司的亞胺培南,於1985年套用於臨床。但亞胺培南易被腎脫氫肽酶I(DHP-I)降解而失效,且因其在腎內高度代謝和潛在的腎毒性,便開發了DHP-I抑制劑——西司他丁,西司他丁與亞胺培南合用,可阻止後者腎內代謝並消除腎毒性。1994年三共公司上市的帕尼培南對DHP-I的穩定性比亞胺培南好,但仍有部分在體內降解、經腎排泄,具有一定腎毒性,需與有機陰離子轉運抑制劑-苯甲醯胺丙酸(倍他米隆)聯合使用來降低腎毒性。亞胺培南、帕尼培南屬於第一代碳青黴烯類抗生素。後來研究表明,在C-1位引入β-甲基,可增強碳青黴烯的化學穩定性及對DHP-I的穩定性。此後開發上市的1β-甲基碳青黴烯類藥物如:住友公司的美羅培南、默克公司的厄他培南、氰胺公司的比阿培南、鹽野義公司的多尼培南和氰胺公司的替比培南酯等屬於第二代碳青黴烯類抗生素。
比阿培南是美國氰胺製藥公司開發的新型1β-甲基碳青黴烯類抗生素,2002年3月首次在日本上市,對DHP-I穩定。比阿培南與主要的青黴素結合蛋白高度結合,具有廣譜抗菌活性,對革蘭陰性菌的活性優於亞胺培南,對革蘭陽性菌的活性優於美羅培南,並能耐受多種β-內醯胺酶的水解,耐藥性較其他β-內醯胺類抗生素低。而且對耐藥的綠膿桿菌、厭氧菌等均具有較強的抗菌活性。
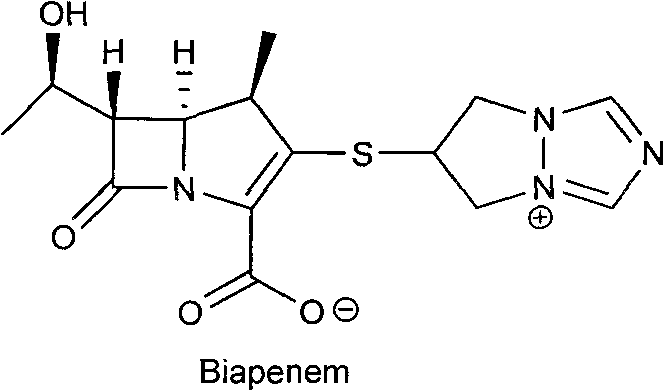
比阿培南化學名稱為:6-[(4R,5S,6S)-2-羧基-6-[(1R)-1-羥乙基]-4-甲基-7-氧代-1-氮雜二環[3、2、0]庚-2-烯-3-基]硫基-6,7-二氫-5H-吡唑並[1,2-α][1,2,4]三唑-4-鎓內鹽,其結構式如下:
截至2010年4月,比阿培南的製備方法均以具有下面式I化合物為原料,脫除保護基R而獲得:
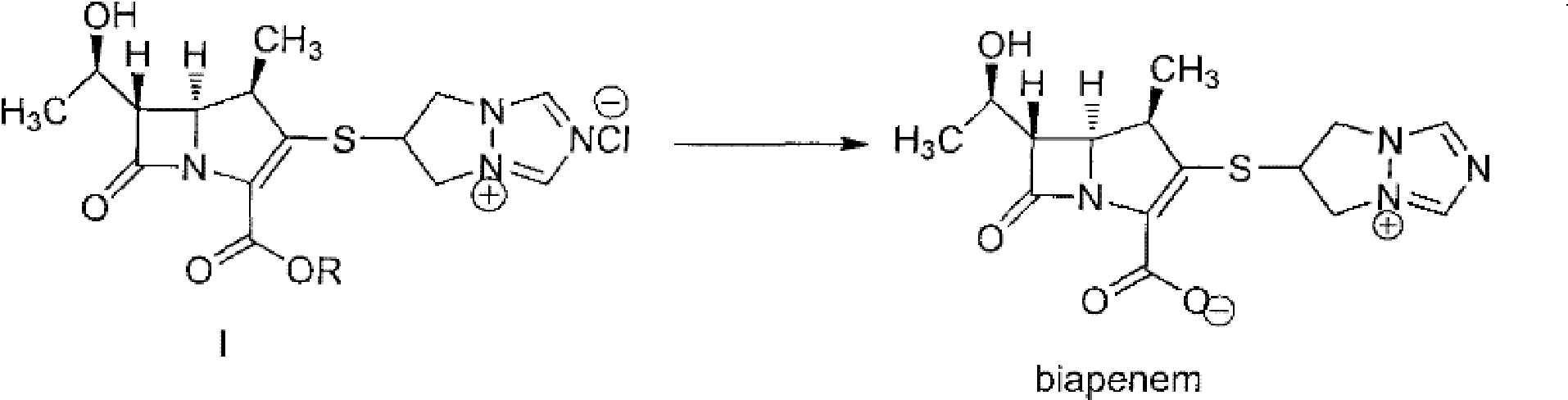
2010年4月前技術主要有以下幾種方法:
第一種是以Pd(OH)2或Pd/C為催化劑,在磷酸鹽緩衝液中加壓氫化,經離子交換樹脂Dowex50-X4純化、濃縮、凍乾後得到產品,收率低於30%(J.Antibiotics.1989,42,374-381);
第二種是以Pd/C為催化劑,在乙酸鹽緩衝液中加壓氫化,經大孔吸附樹脂SP-207純化、濃縮、凍乾重結晶得到產品,收率60%(US5412103);
第三種是以鋅粉為催化劑,在pH=5.6的磷酸鹽緩衝液中脫除保護基,經大孔吸附樹脂SP-207純化後得到產品(J.Org.Chem.1998,63,8145-8149)。
上述三種方法的缺點在於:為避免反應產物比阿培南在酸性較強的環境中被破壞,反應時都會加入緩衝鹽以控制反應液的pH,但是該緩衝鹽的存在使反應所得含有比阿培南的溶液無法結晶,因此,反應後必須先用樹脂純化去除該緩衝鹽;而在洗脫時又需要用到大量的水。如下面三篇文獻中記載:
(1)專利EP0289801中的實施例6中記載,以吸附樹脂HP-40純化,以含3%丙酮的水洗脫,洗脫液冷凍乾燥;
(2)J.Org.Chem.1992,57(15),4243-4249中4249頁記載,以離子交換樹脂Dowex50-X4純化,需用水洗脫,洗脫液冷凍乾燥;
(3)J.Org.Chem.1998,63,8145-8149中8149頁記載,以吸附樹脂SP-207純化,以含3%丙酮的水洗脫。
由於比阿培南是一種熱敏性物質,在水中不穩定,水中加熱比阿培南會裂解,所以無法用長時間加熱蒸餾的方法去除水,只能夠用冷凍乾燥的方法。但冷凍乾燥存在投資大、設備複雜、乾燥速率低、時間長、能耗高,維護費用高等缺點,因而使得產品成本居高不下,增加了工業化投資成本,也使得生產效率低下。
此外,比阿培南的水溶性較差,重結晶需要大量的水,造成結晶時所用水量大,結晶損失大,收率低。
發明內容
專利目的
《比阿培南的製備方法》的目的是解決上述2010年前方法製備比阿培南存在的缺陷,提供一種能適應工業化生產且產率高的製備方法。
經過大量的實驗研究,《比阿培南的製備方法》的發明人發現,雖然比阿培南在pH值3.0~7.0的水溶液中穩定,但在進行氫化反應時,水和有機溶劑混合液中無需加入緩衝鹽以控制反應液的pH,只需在反應後立即加入有機鹼調節pH到一定範圍,再加入有機溶劑即可得到結晶比阿培南;而在比阿培南重結晶時加入有機酸可以增加比阿培南在水中的溶解性,能減少水的用量,提高結晶收率。
技術方案
《比阿培南的製備方法》提供的具體技術方案如下:
一種比阿培南的製備方法,其包括以下步驟:
(a)、以具有式I化合物為原料,在水和有機溶劑的混合液中,與H
2進行催化氫化反應,脫除保護基R;
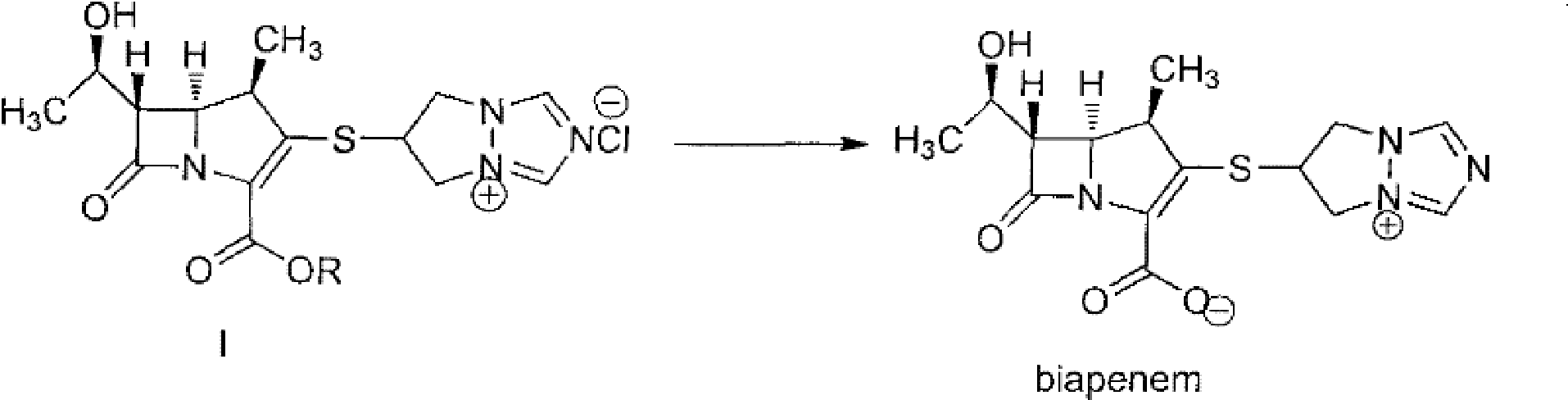
其中R為羧基保護基。
(b)、濾除步驟(a)反應所用催化劑後加入有機鹼調節pH值或在步驟(a)反應液中加入有機鹼調節pH值後濾除反應所用催化劑;分液,則水相含有比阿培南;
(c)、向步驟(b)所得比阿培南水溶液中加入有機溶劑,析出比阿培南結晶。
《比阿培南的製備方法》的製備方法還包括:(d)將步驟(c)所得比阿培南結晶加入到水和有機酸中,再加入醇或酮重結晶。
其中,上述羧基保護基R包括碳青黴烯行業內眾所周知的能夠與羧基反應或脫除而不引起該分子內其他部分的任何所不希望變化的羧基保護基。具體地,該羧基保護基R包括C1~C8的成酯性烷基,較佳的為甲基、甲氧甲基、乙基、乙氧乙基、碘乙基、丙基、異丙基、丁基、異丁基、三氯乙基或叔丁基;C3~C8的鏈烯基,較佳的為丙烯基、乙烯基、異丙烯基、苯丙烯基或己烯基;C7~C19的芳香烷基,較佳的為苄基、甲基苄基、二甲基苄基、甲氧基苄基、乙氧基苄基、對硝基苄基、氨基苄基、二苯甲基、苯乙基、三苯甲基、二叔丁基羥基苄基或苯甲醯甲基;C6~C12的芳香基,較佳的為苯基、甲苯基、二異丙基苯基、二甲苯基、三氯苯基或五氯苯基;C1~C12的氨基,較佳的為丙酮肟或苯乙酮肟;C3~C12的烴化甲基烷基,較佳的為三甲基矽烷基、二甲基甲氧基矽烷基或叔丁基二甲基矽烷基。更佳的為對硝基苄基、苄基或對甲氧基苄基。最佳的為對硝基苄基。
步驟(a)中所使用的有機溶劑沒有特別限制,目的是為了溶解具有式I化合物的原料,並溶解反應後脫下的保護基R,只要它們不對該反應產生有害影響即可,所述有機溶劑包括C1~C4的鹵代烷烴,較佳的為二氯甲烷、氯仿或二氯乙烷;C1~C4的腈類,較佳的為乙腈或丙腈;C1~C4的醇類,較佳的為甲醇或乙醇;C1~C4的酮類,較佳的為丙酮或丁酮;C1~C8的乙酸酯,較佳的為乙酸乙酯或乙酸甲酯;C1~C4的醚,較佳的為乙醚或四氫呋喃;C3~C4的醯胺,較佳的為二甲基甲醯胺或二甲基乙醯胺;C6~C10的含苯溶劑,較佳的為甲苯、二甲苯或氯苯。一般選用醚類或乙酸酯類。最優選的有機溶劑為四氫呋喃。
步驟(a)中所使用的催化劑為氫化領域常用到的催化劑,如鈀碳、氫氧化鈀、乙酸鈀、鉑碳、二氧化鉑或鎳,催化劑的用量為具有式I化合物的重量的5~50%。
步驟(a)中氫化時的壓力為1~100千克/平方米,優選4~20千克/平方米;
步驟(a)中氫化時的反應溫度為0~100℃,優選10~30℃。
步驟(a)中所述的反應時間為0.5~5小時。
步驟(b)中,既可以濾除催化劑後調節pH值,也可以先調節pH後濾除催化劑。如果採用先濾除催化劑後調節pH值,為了防止步驟(a)生成的比阿培南在反應後的酸性介質中被破壞,應在儘可能短的時間內執行步驟(b),較佳地,在步驟(a)反應完成後的60分鐘內執行步驟(b)中的操作,更佳地,在步驟(a)反應完成後的20分鐘內執行步驟(b)中的操作;如果先調節pH後濾除催化劑,對處理時間沒有特別要求,只要不讓反應液放置太久導致比阿培南被破壞即可。
步驟(b)中所述的pH值為1~8,優選為3~6。
步驟(b)中所述的有機鹼為芳香含氮雜環、脂肪族三元胺或脂肪族二元胺等鹼性化合物,其中芳香含氮雜環有機鹼包括吡啶、4-二甲氨基吡啶、2-甲基吡啶、2,6-二甲基吡啶、2,4,6-三甲基吡啶或吡咯;脂肪族三元胺有機鹼包括三甲胺、三乙胺、二異丙基乙基胺、N-甲基嗎啉、N-甲基吡咯烷、N-甲基哌啶或三丁胺;脂肪族二元胺有機鹼包括乙二胺、丙二胺、丁二胺、哌啶、嗎啉、甲基乙基胺或四氫吡咯。最優選的有機鹼是N-甲基嗎啉、N-甲基哌啶或4-二甲氨基吡啶。
步驟(c)中所使用的有機溶劑沒有特別限制,只要它們和水混溶即可,所述有機溶劑包括C1~C4的腈類,較佳的為乙腈或丙腈;C1~C4的醇類,較佳的為甲醇、乙醇或異丙醇;C1~C4的酮類,較佳的為丙酮或丁酮;C1~C4的醚,較佳的為四氫呋喃;C3~C6的醯胺,較佳的為二甲基甲醯胺、二甲基乙醯胺或N-吡咯烷酮。一般選用醇類或酮類。最優選的有機溶劑為丙酮或乙醇。
步驟(c)中結晶溫度為0~100℃,優選0~25℃。
步驟(c)中結晶時間為0.5~3小時。
步驟(d)中所使用的醇包括C1~C4的醇類,較佳的為甲醇或乙醇;酮包括C1~C4的酮類,較佳的為丙酮或丁酮。優選乙醇、丙酮。
步驟(d)中所使用的有機酸為C1~C10的脂肪酸,較佳的為甲酸、乙酸、丙酸、丁酸、丁二酸、丙二酸、草酸、檸檬酸、馬來酸、富馬酸或丙酮酸;C7~C10的芳香酸,較佳的為苯甲酸,水楊酸,酒石酸。優選乙酸或丙酸。
步驟(d)中重結晶溫度為0~100℃,優選0~25℃。
步驟(d)中重結晶時間為0.5~3小時。
《比阿培南的製備方法》方法所用的試劑和原料均市售可得。
各步反應結束後可按照本領域常規處理方法進行。
有益效果
《比阿培南的製備方法》在製備比阿培南的氫化過程中不需要緩衝鹽以保證反應液的pH,只需在反應後立即用有機鹼調節pH到一定範圍,再加入有機溶劑即可析出比阿培南的晶體,最後用水和有機酸重結晶得比阿培南精製品。本製備方法操作簡單,也無需吸附樹脂或離子交換樹脂純化,提高了生產效率,降低了能耗,減少了設備投資;在重結晶時加入有機酸增加其在水中的溶解性,減少了水的用量,提高了結晶收率和純度,適合工業化生產。
技術領域
《比阿培南的製備方法》涉及比阿培南的製備方法。
權利要求
1.一種比阿培南的製備方法,其包括以下步驟:
(a)以具有式I化合物為原料,在水和有機溶劑的混合液中,與H
2進行催化氫化反應,脫除保護基R;
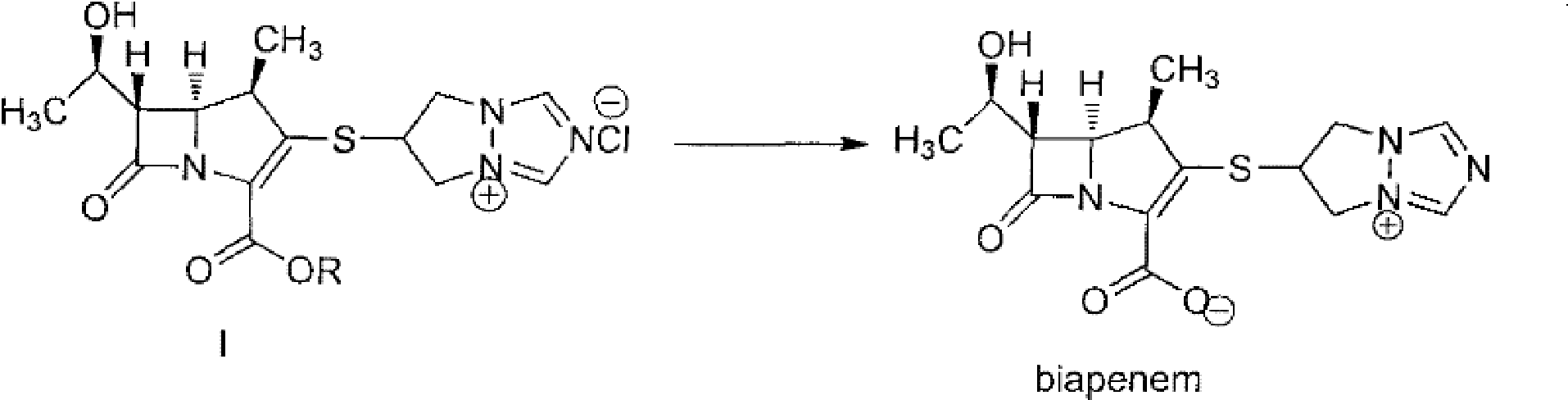
其中R為羧基保護基;
(b)濾除步驟(a)反應所用催化劑後加入有機鹼調節pH值或在步驟(a)反應液中加入有機鹼調節pH值後濾除反應所用催化劑;分液,則水相含有比阿培南;
(c)向步驟(b)所得比阿培南水溶液中加入有機溶劑,析出比阿培南結晶。
2.根據權利要求1所述的比阿培南的製備方法,其特徵在於:所述羧基保護基R包括C1~C8的成酯性烷基、C3~C8的鏈烯基、C7~C19的芳香烷基、C6~C12的芳香基、C1~C12的氨基或C3~C12的烴化甲基烷基。
3.根據權利要求2所述的比阿培南的製備方法,其特徵在於:所述C1~C8的成酯性烷基包括甲基、甲氧甲基、乙基、乙氧乙基、碘乙基、丙基、異丙基、丁基、異丁基、三氯乙基或叔丁基;C3~C8的鏈烯基包括丙烯基、乙烯基、異丙烯基、苯丙烯基或己烯基;C7~C19的芳香烷基包括苄基、甲基苄基、二甲基苄基、甲氧基苄基、乙氧基苄基、對硝基苄基、氨基苄基、二苯甲基、苯乙基、三苯甲基、二叔丁基羥基苄基或苯甲醯甲基;C6~C12的芳香基包括苯基、甲苯基、二異丙基苯基、二甲苯基、三氯苯基或五氯苯基;C1~C12的氨基包括丙酮肟或苯乙酮肟;C3~C12的烴化甲基烷基包括三甲基矽烷基、二甲基甲氧基矽烷基或叔丁基二甲基矽烷基。
4.根據權利要求3所述的比阿培南的製備方法,其特徵在於:所述羧基保護基R為對硝基苄基。
5.根據權利要求1所述的比阿培南的製備方法,其特徵在於:步驟(a)中的有機溶劑包括C1~C4的鹵代烷烴、C1~C4的腈類、C1~C4的醇類、C1~C4的酮類、C1~C8的乙酸酯、C1~C4的醚、C3~C4的醯胺或C6~C10的含苯溶劑。
6.根據權利要求5所述的比阿培南的製備方法,其特徵在於:所述C1~C4的鹵代烷烴包括二氯甲烷、氯仿或二氯乙烷;C1~C4的腈類包括乙腈或丙腈;C1~C4的醇類包括甲醇或乙醇;C1~C4的酮類包括丙酮或丁酮;C1~C8的乙酸酯包括乙酸乙酯或乙酸甲酯;C1~C4的醚包括乙醚或四氫呋喃;C3~C4的醯胺包括二甲基甲醯胺或二甲基乙醯胺;C6~C10的含苯溶劑包括甲苯、二甲苯或氯苯。
7.根據權利要求6所述的比阿培南的製備方法,其特徵在於:步驟(a)中的有機溶劑為四氫呋喃。
8.根據權利要求1所述的比阿培南的製備方法,其特徵在於:步驟(a)中所用催化劑為鈀碳、氫氧化鈀、乙酸鈀、鉑碳、二氧化鉑或鎳,且所述催化劑的用量為具有式I化合物的重量的5~50%。
9.根據權利要求1所述的比阿培南的製備方法,其特徵在於:步驟(a)中氫化時的壓力為1~100千克/平方米
10.根據權利要求9所述的比阿培南的製備方法,其特徵在於:步驟(a)中氫化時的壓力為4~20千克/平方米
11.根據權利要求1所述的比阿培南的製備方法,其特徵在於:步驟(a)中氫化時的反應溫度為0~100℃。
12.根據權利要求11所述的比阿培南的製備方法,其特徵在於:步驟(a)中氫化時的反應溫度為10~30℃
13.根據權利要求1所述的比阿培南的製備方法,其特徵在於:步驟(a)中所述的反應時間為0.5~5小時。
14.根據權利要求1所述的比阿培南的製備方法,其特徵在於:在步驟(a)反應完成後的60分鐘內執行步驟(b)。
15.根據權利要求14所述的比阿培南的製備方法,其特徵在於:在步驟(a)反應完成後的20分鐘內執行步驟(b)。
16.根據權利要求15所述的比阿培南的製備方法,其特徵在於:步驟(b)中所述的pH值為3~6。
17.根據權利要求16所述的比阿培南的製備方法,其特徵在於:步驟(b)中所述的有機鹼為芳香含氮雜環、脂肪族三元胺或脂肪族二元胺。
18.根據權利要求17所述的比阿培南的製備方法,其特徵在於:所述芳香含氮雜環有機鹼包括吡啶、4-二甲氨基吡啶、2-甲基吡啶、2,6-二甲基吡啶、2,4,6-三甲基吡啶或吡咯;脂肪族三元胺有機鹼包括三甲胺、三乙胺、二異丙基乙基胺、N-甲基嗎啉、N-甲基吡咯烷、N-甲基哌啶或三丁胺;脂肪族二元胺有機鹼包括乙二胺、丙二胺、丁二胺、哌啶、嗎啉、甲基乙基胺或四氫吡咯。
19.根據權利要求18所述的比阿培南的製備方法,其特徵在於:步驟(b)中所述的有機鹼為N-甲基嗎啉、N-甲基哌啶或4-二甲氨基吡啶。
20.根據權利要求1所述的比阿培南的製備方法,其特徵在於:步驟(c)中的有機溶劑包括C1~C4的腈類、C1~C4的醇類、C1~C4的酮類、C1~C4的醚或C3~C6的醯胺。
21.根據權利要求20所述的比阿培南的製備方法,其特徵在於:所述C1~C4的腈類包括乙腈或丙腈;C1~C4的醇類包括甲醇、乙醇或異丙醇;C1~C4的酮類包括丙酮或丁酮;C1~C4的醚包括四氫呋喃;C3~C6的醯胺包括二甲基甲醯胺、二甲基乙醯胺或N-吡咯烷酮。
22.根據權利要求21所述的比阿培南的製備方法,其特徵在於:步驟(c)中的有機溶劑為丙酮或乙醇。
23.根據權利要求1所述的比阿培南的製備方法,其特徵在於:步驟(c)中結晶溫度為0~100℃。
24.根據權利要求23所述的比阿培南的製備方法,其特徵在於:步驟(c)中結晶溫度為0~25℃
25.根據權利要求1所述的比阿培南的製備方法,其特徵在於:步驟(c)中結晶時間為0.5~3小時。
26.根據權利要求1至25任一項所述的比阿培南的製備方法,其特徵在於,所述製備方法還包括:(d)將步驟(c)所得比阿培南結晶加入到水和有機酸中,再加入醇或酮重結晶。
27.根據權利要求26所述的比阿培南的製備方法,其特徵在於:步驟(d)中的醇為C1~C4的醇類,酮為C1~C4的酮類。
28.根據權利要求27所述的比阿培南的製備方法,其特徵在於:步驟(d)中的醇為乙醇,酮為丙酮。
29.根據權利要求26所述的比阿培南的製備方法,其特徵在於:步驟(d)中的有機酸為C1~C10的脂肪酸或C7~C10的芳香酸。
30.根據權利要求28所述的比阿培南的製備方法,其特徵在於:所述C1~C10的脂肪酸包括甲酸、乙酸、丙酸、丁酸、丁二酸、丙二酸、草酸、檸檬酸、馬來酸、富馬酸或丙酮酸;C7~C10的芳香酸包括苯甲酸,水楊酸或酒石酸。
31.根據權利要求30所述的比阿培南的製備方法,其特徵在於:步驟(d)中的有機酸為乙酸或丙酸。
32.根據權利要求26所述的比阿培南的製備方法,其特徵在於:步驟(d)中結晶溫度為0~100℃。
33.根據權利要求32所述的比阿培南的製備方法,其特徵在於:步驟(d)中結晶溫度為0~25℃
34.根據權利要求26所述的比阿培南的製備方法,其特徵在於:步驟(d)中結晶時間為0.5~3小時。
實施方式
實施例1
6-[(4R,5S,6S)-2-(4-硝基苄氧羰基)-6-[(1R)-1-羥乙基]-4-甲基-7-氧代-1-氮雜二環[3、2、0]庚-2-烯-3-基]硫基-6,7-二氫-5H-吡唑並[1,2-α][1,2,4]三唑-4-鎓·氯化物(I,R=O2NPhCH2)300克(0.58摩爾),加入到水1.5升和四氫呋喃1.0升中,攪拌溶解,加入鈀碳(10%)70克,控制氫化壓力4~5千克/平方米,10~20℃反應2.5小時;反應結束後立即過濾掉鈀碳,用4-二甲氨基吡啶調節pH為3.0~6.0,分液,水相加入丙酮4.0升,10~20℃攪拌3.0小時,析出晶體,過濾,固體用丙酮300毫升洗滌,減壓乾燥,得到比阿培南180克,(收率:90%)。
實施例2
6-[(4R,5S,6S)-2-(4-硝基苄氧羰基)-6-[(1R)-1-羥乙基]-4-甲基-7-氧代-1-氮雜二環[3、2、0]庚-2-烯-3-基]硫基-6,7-二氫-5H-吡唑並[1,2-α][1,2,4]三唑-4-鎓·氯化物(I,R=O2NPhCH2)600克(1.16摩爾),加入到水3.0升和四氫呋喃2.0升中,攪拌溶解,加入氫氧化鈀(10%)120克,控制氫化壓力10~15千克/平方米,10~15℃反應1.0小時;反應結束後用N-甲基嗎啉調節pH為3.0~6.0,過濾掉氫氧化鈀,分液,水相加入乙醇8.0升,0~5℃攪拌0.5小時,析出晶體,過濾,固體用乙醇600毫升洗滌,減壓乾燥,得到比阿培南364克,(收率:91.0%)。
實施例3
6-[(4R,5S,6S)-2-(4-硝基苄氧羰基)-6-[(1R)-1-羥乙基]-4-甲基-7-氧代-1-氮雜二環[3、2、0]庚-2-烯-3-基]硫基-6,7-二氫-5H-吡唑並[1,2-α][1,2,4]三唑-4-鎓·氯化物(I,R=O2NPhCH2)600克(1.16摩爾),加入到水3.0升和四氫呋喃2.0升中,攪拌溶解,加入鉑碳(5%)200克,控制氫化壓力20千克/平方米,25~30℃反應0.5小時;反應結束後10分鐘內過濾掉鉑碳,用N-甲基哌啶調節pH為4.0~6.0,分液,水相加入乙醇8.0升,5~10℃攪拌2.0小時,析出晶體,過濾,固體用乙醇600毫升洗滌,減壓乾燥,得到比阿培南360克,(收率:90%)。
實施例4
6-[(4R,5S,6S)-2-(苄氧羰基)-6-[(1R)-1-羥乙基]-4-甲基-7-氧代-1-氮雜二環[3、2、0]庚-2-烯-3-基]硫基-6,7-二氫-5H-吡唑並[1,2-α][1,2,4]三唑-4-鎓氯化物(I,R=PhCH2)132克(0.252摩爾),加入到水1.0升,乙酸乙酯600毫升,攪拌溶解,加入二氧化鉑(10%)40克,控制氫化壓力10~15千克/平方米,15~20℃反應5.0小時;反應結束後用N-甲基嗎啉調節pH為4.0~6.0,過濾掉二氧化鉑,分液,水相加入乙醇2.0升,20~25℃攪拌1.5小時,過濾,固體用乙醇300毫升洗滌,減壓乾燥,得到比阿培南77.6克,(收率:88%)。
實施例5
用三乙胺替代實施例1中的4-二甲氨基吡啶,其他不變,收率:75%。
實施例6
用吡啶替代實施例2中的N-甲基嗎啉,其他不變,收率:65%。
實施例7
用丁二胺替代實施例3中的N-甲基哌啶,其他不變,收率:56%。
實施例8
用二異丙基乙基胺替代實施例1中的4-二甲氨基吡啶,其他不變,收率:80%。
實施例9
用N-甲基吡咯烷替代實施例2中的N-甲基嗎啉,其他不變,收率:72%。
實施例10
用乙二胺替代實施例1中的4-二甲氨基吡啶,其他不變,收率:69%。
實施例11
用三丁胺替代實施例3中的N-甲基哌啶,其他不變,收率:76%。
實施例12
實施例1中得到比阿培南180克加入2.7升的注射用水中,加入乙酸(先經過過濾除菌和除細菌內毒素)5.0毫升,攪拌溶解,加入針用活性炭18克,攪拌20分鐘,濾除活性炭,濾液用0.22μ濾膜過濾,在濾液中滴加10.8升無水乙醇(先經過過濾除菌和除細菌內毒素),滴加完畢,冷卻到0~5℃,攪拌2.0小時,過濾,濾餅真空乾燥,得到比阿培南精製品170克,純度:99.66%。
實施例13
實施例4中得到比阿培南77.6克加入1.2升的注射用水中,加入丙酸(先經過過濾除菌和除細菌內毒素)3.0毫升,攪拌溶解,加入針用活性炭18克,攪拌20分鐘,濾除活性炭,濾液用0.22μ濾膜過濾,在濾液中滴加3.5升丙酮(先經過過濾除菌和除細菌內毒素),滴加完畢,冷卻到0~5℃,攪拌3.0小時,過濾,濾餅真空乾燥,得到比阿培南精製品72.1克,純度:99.87%。
實施例14
實施例3中得到比阿培南360克加入5.6升的注射用水中,加入酒石酸(先經過過濾除菌和除細菌內毒素)10.6克,攪拌溶解,加入針用活性炭18克,攪拌20分鐘,濾除活性炭,濾液用0.22μ濾膜過濾,在濾液中滴加21.5升無水乙醇(先經過過濾除菌和除細菌內毒素),滴加完畢,冷卻到5~10℃,攪拌3.0小時,過濾,濾餅真空乾燥,得到比阿培南精製品324克,純度:99.13%。
實施例15
實施例1中得到比阿培南180克加入2.7升的注射用水中,加入馬來酸(先經過過濾除菌和除細菌內毒素)5.0克,攪拌溶解,加入針用活性炭18克,攪拌20分鐘,濾除活性炭,濾液用0.22μ濾膜過濾,在濾液中滴加12.2升丙酮(先經過過濾除菌和除細菌內毒素),滴加完畢,冷卻到20~25℃,攪拌0.5小時,過濾,濾餅真空乾燥,得到比阿培南精製品152克,純度:98.78%。
榮譽表彰
2018年12月20日,《比阿培南的製備方法》獲得第二十屆中國專利獎優秀獎。