標準燃燒熱是在標態及TK條件下以確定的穩定產物的焓值為0反應物的相對焓值。
基本介紹
- 中文名:標準燃燒熱
- 外文名:Standard heat of combustion
- 釋義:1mol物質完全燃燒時的反應熱
- 全稱:標準摩爾燃燒熱
- 學科:化學
定義
標準燃燒熱的含義

定義原因
注意事項

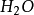

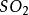
套用實例
熱化學方程式的意義
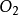

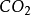

標準燃燒熱是在標態及TK條件下以確定的穩定產物的焓值為0反應物的相對焓值。


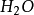

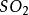
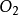

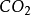
標準燃燒熱是在標態及TK條件下以確定的穩定產物的焓值為0反應物的相對焓值。...... 標準燃燒熱是在標態及TK條件下以確定的穩定產物的焓值為0反應物的相對焓值。...
燃燒熱是指物質與氧氣進行完全燃燒反應時放出的熱量。它一般用單位物質的量、單位質量或單位體積的燃料燃燒時放出的能量計量。燃燒反應通常是烴類在氧氣中燃燒生成...
熱化學的一個分支,是測定物質燃燒反應熱效應的實驗科學。這種熱效應稱作燃燒熱。單位是千焦/摩爾。...
標準摩爾燃燒焓是指在標準壓力100kPa和指定溫度(一般為298.15K)時下,一摩爾物質完全燃燒時的反應焓變。...
32.氣相標準燃燒熱(焓)(kJ/mol):764.933.氣相標準生成熱(焓)( kJ/mol) :-201.534.氣相標準熵(J·mol-1/K) :239.88...
氣相標準燃燒熱(焓)(kJ·mol-1):2051.42氣相標準生成熱(焓)( kJ·mol-1) :-272.42氣相標準熵(J·mol-1·K-1) :309.20...
24.氣相標準熵 :461.6625.氣相標準生成自由能:-86.526.液相標準燃燒熱(焓):-4443.827.液相標準聲稱熱(焓)):-311.528.液相標準熵 :348.5...
氣相標準燃燒熱(焓)(kJ·mol-1):-2876.4氣相標準聲稱熱(焓)( kJ·mol-1):-126.8氣相標準熵(J·mol-1·K-1):309.91氣相標準生成自由能( kJ·mol-1...
9.氣相標準燃燒熱(焓)(kJ·mol-1):-11446.9 10.氣相標準聲稱熱(焓)( kJ·mol-1) :-781.2 11.液相標準燃燒熱(焓)(kJ·mol-1):-11343.4 12.液相標...
15.氣相標準燃燒熱(焓)(kJ·mol-1):-9269.216.氣相標準聲稱熱(焓)( kJ·mol-1) :-527.417.液相標準燃燒熱(焓)(kJ·mol-1):-9216.0...
22.氣相標準燃燒熱(焓)(kJ·mol-1):-4491.523.氣相標準聲稱熱(焓)( kJ·mol-1) :-263.524.氣相標準熵(J·mol-1·K-1) :461.66...
23.氣相標準燃燒熱(焓)(kJ·mol-1):-6829.6324.氣相標準聲稱熱(焓)( kJ·mol-1):-249.5825.氣相標準熵(J·mol-1·K-1) :545.85...
彭昌軍;鏈烷烴標準燃燒熱的拓樸計算法[J];天然氣化工(C1化學與化工);1996年06期彭昌軍 ,陳亞琴;用拓撲學方法研究烷烴的化學?[J];化學工程師;1994年05期...
28.氣相標準燃燒熱(焓):-3535.7329.氣相標準聲稱熱(焓):-146.8230.氣相標準熵 :349.5631.氣相標準生成自由能:-8.632.氣相標準熱熔:120.04...
熱效應是指在一定溫度下,體系在變化過程中放出或吸收的熱量。隨著變化性質的不同,有燃燒熱、溶解熱、稀釋熱、生成熱、中和熱等。化學反應中的熱效應又稱反應熱,...
與空氣混合可爆,遇明火、高溫、氧化劑易燃; 燃燒產生刺激煙霧,與氧化劑、酸類...職業標準 TWA 410 毫克/立方米; STEL 615 毫克/立方米[4] 安全信息 危險品...
