診斷
病史
多系早產、刮宮產兒,或有窒息史、孕母有糖尿病、妊娠高血壓綜合徵等。 生後6~12小時內出現進行性
呼吸困難。
體徵
患兒呆鈍,面色灰白或青紫,四肢鬆弛。出現進行性
呼吸困難、呼氣性呻吟及吸氣性
三凹征。心率先快後慢,心音由強轉弱,胸骨左緣可聽到收縮期
雜音。呼吸頻率60-100次/分或更快,呼吸節律不規則,間有暫停,兩肺呼吸音減低,早期肺部羅音常不明顯,以後可聽到細
濕羅音,叩診可出現濁音。肝臟可增大。
輔助檢查
羊水泡沫試驗、胃液振盪試驗均呈陰性;羊水
卵磷脂和鞘磷脂(L/S)<2∶1;血pH值、PaO2、HCO3-降低而PCO2、BE增高,呈
代謝性酸中毒。血鉀早期常增高,恢復期利尿後可降低。肺部X線檢查早期兩肺有細小顆粒陰影,最後兩肺均不透明變白,伴有黑色“支氣管充氣征”。X線檢查應在用正壓呼吸前進行,否則萎陷不久的
肺泡可以重新張開使胸片無
陽性表現。
治療措施
不論臨床擬診或確診病例均應積極處理,力爭度過3天,存活有望。
一般治療
1、注意保暖,保證
體溫在36~37℃,暖箱相對濕度50%左右。用監護儀監測
體溫、呼吸、心率,經皮測PO2、PCO2和pH。
 新生兒肺透明膜病
新生兒肺透明膜病2、經常清除咽部粘液,保持呼吸道通暢。
3、保證營養和液體入量,不能哺乳者用1/5張含鈉液60~80ml/(kg·d),第2日以後100~120ml(kg·d),
靜脈滴注。使用人工呼吸機者,如果吸入氣中水蒸汽已飽和?掛毫坑?跎儻?0~60ml/(kg·d)。
4、
吸氧和機械呼吸:使PaO2維持在6.7~9.3kPa(50~70mmHg),PaO2過高可導致
早產兒視網膜病(ROP)而失明。吸入氧度(FiO2)>0.6,超過24小時對肺有一定毒性,可導致
支氣管肺發育不良(慢性
肺部疾病)。
表面活性物質(PS)替代療法
表面活性物質(PS)有天然、人工合成和混合製劑三種。由
羊水、牛肺、豬肺或羊肺洗液中提取的天然製劑療效較人工合成者為好,混合製劑系在天然製劑中加少量人工合成的二棕櫚
卵磷脂和磷脂甘油。
一般將表面活性物質(PS)製劑100-200mg/(kg·次)混懸於4ml生理鹽水中,儘早由氣管導管分別滴入四個不同體位(仰臥、右、左側臥,再仰臥),分別用面罩氣囊復甦器加壓呼吸1~2分鐘,使PS在兩側肺內均勻分布,用藥後1-2小時可見症狀好轉,隔12小時重複同劑量。生後2天內多次(2~3次)治療的治癒率可提高到90%以上,生後正常呼吸前就給PS可起預防作用。
對症治療
1、糾正水、電解質和酸鹼平衡紊亂 酸中毒時首選5%碳酸氫鈉3~5ml/(kg·次),或根據測定的BE和CO2-CP計算:BE×體重(kg)=Na+mmol(mEq),但一日量不超過6~8mmHg/kg。高血鈉時用0.3M THAM2~3ml/次,靜脈注射。高血鉀時用15%葡萄糖50mg/kg,並按每3~4g葡萄糖加1IU普通胰島素,
靜脈滴注。
2、控制
心力衰竭 用毛地黃快速製劑,如毒毛旋花子甙K0.01mg/(kg·次),或西地蘭0.015mg/(kg·次),緩慢
靜脈注射。
動脈導管重新開放者可試用消炎痛0.02mg/(kg·次),共用3次,每劑間隔12小時;小於2天者後2劑的劑量減半。
3、嚴重缺氧出現抽搐時,用20%甘露醇5ml/(kg·次),靜脈注射。
5、煩躁和抽搐者用安定0.2~0.3mg/(kg·次),靜脈注射;或苯巴比妥鈉5~7mg/(kg·次),肌肉注射。
6、關閉
動脈導管 在使用呼吸機時或治療後恢復期,由於肺小動脈痙攣解除,肺動脈壓力降低至低於主動脈壓力,可出現由左向右分流,分流量大時可導致心衰及肺水腫,尤其是在體重<1500g者。可用消炎痛靜滴以關閉
動脈導管:出生體重kg,>7天者則0.2mg/kg,12及36小時後再各用1次;本藥口服效果差,如經心導管直接滴入動脈導管口,則療效更佳。用藥無效時應考慮手術結紮。
四、預防和控制感染:嚴格消毒隔離制度;選用有效抗生素,一般用青黴素20~25萬U/(kg·d)。
病因學
本病是因為缺乏由Ⅱ型
肺泡細胞產生的表面活性物質(PS)所造成,表面活性物質的80%以上由磷脂(PL)組成,在
胎齡20~24周時出現,35周后迅速增加,故本病多見於早產兒,胎齡越小,發病率越高。表面活性物質(PS)缺乏的原因有:① 早產:小於35周的早產兒Ⅱ型細胞發育未成熟,PS生成不足;② 缺氧、
酸中毒、低溫:均能抑制早產兒生後PS的合成;③ 糖尿病孕婦的
胎兒:其胎兒
胰島細胞增生,而
胰島素具有拮抗腎上腺皮質激素的作用,延遲胎肺成熟;④ 剖宮產:因其缺乏正常子宮收縮,刺激腎上腺皮質激素增加,促進肺成熟,PS相對較少;⑤ 通氣失常:可影響PS的合成;⑥
肺部感染:Ⅱ型細胞遭破壞,PS產量減少。
 新生兒肺透明膜病 病因
新生兒肺透明膜病 病因發病機理
表面活性物質能降低
肺泡壁與肺泡內氣體交界處的表面張力,使肺泡張開,其半衰期短而需要不斷補充。表面活性物質缺乏時,
肺泡表面張力增高,按照公式P(肺泡回縮率)=2T(表面張力)/r(肺泡半徑),呼氣時半徑最小的肺泡就最先萎陷,於是發生進行性
肺不張、導致臨床上呼吸困難和青紫等症狀進行性加重。其過程如下:
肺泡表面活性物質不足→肺泡壁表面張力增高(肺泡回縮力增高)→半徑最小肺泡最先萎陷→進行性肺不張→缺氧、
酸中毒→肺小動脈痙攣→肺動脈壓力增高→
卵圓孔及
動脈導管開放→右向左分流(持續
胎兒循環)→肺灌流量下降→肺組織缺氧更重→毛細血管通透性增高→纖維蛋白沉著→透明膜形成→缺氧、酸中毒更加嚴重,造成惡性循環。
 新生兒肺透明膜病 病因
新生兒肺透明膜病 病因病理改變
大體
兩肺呈深暗紅色,邊緣銳,質韌如肝,外側緣常有肋骨壓跡,大小塊肺組織沉水,擠肺時支氣管口往往有淺紅血水可見。
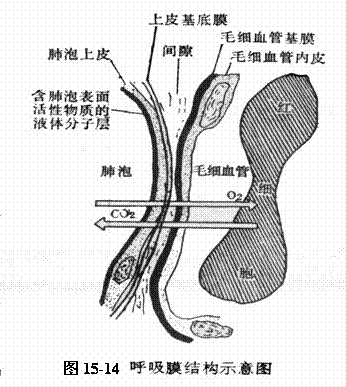 呼吸膜結構
呼吸膜結構鏡檢
肺小動脈收縮,毛細血管及小靜脈瘀血,絕大多數
肺泡萎縮,有廣泛的再吸收性肺不張。典型病變為未萎陷及部分擴張的
肺泡、肺泡管壁及終末毛細支氣管壁上有一層透明的均勻無結構或顆粒狀嗜伊紅膜樣物附著,它由損壞脫落的肺泡上皮細胞、纖維素和含蛋白質的基質組成。死胎中從未見過透明膜。死於生後8小時以內者,透明膜形成不全,多數還斷續游離於泡腔。
肺泡間隔血管瘀血。
臨床表現
出生時心跳、呼吸亦可完全正常。一般出生後立即開始或在6小時內逐漸出現
呼吸困難、青紫,伴呼氣性呻吟、吸氣性
三凹征,並進行性加重。胸腹呼吸動作不協調,呼吸由快轉慢、不規則或呼吸暫停,青紫明顯。經急救後呼吸可好轉,但過後又復發,常呈原發性發作,程度漸次加重,持續時間延長,發作間隔縮短。體溫不穩定,往往不升。死亡多發生在出生後48小時內。部分病例經治療病情漸漸緩解,病程如能超過72小時,肺成熟度增加,則多數患兒能逐漸康復。
輔助檢查
泡沫試驗:取等量羊水置於5個小試管中,加入不等量的純酒精,用力振盪15秒鐘,靜置15分鐘後觀察泡沫的形成。若為本病,用很少量酒精即能阻止羊水泡沫的形成。
 新生兒肺透明膜病
新生兒肺透明膜病卵磷脂和鞘磷脂:肺發育成熟者,羊水中的卵磷脂(L)達3.5mg/dl,與鞘磷脂(S)的比值(L/S)應為2~3∶1。若L/S<2∶1,示為肺發育不良。
2.胃液振盪試驗:胃液1ml加95%酒精1ml,振盪15秒後靜置15分鐘,如果沿管壁仍有一圈泡沫為
陽性,可初步除外HMD,陰性則提示本病。假陽性只1%,但假陰性可達10%,抽胃液時間越晚,假陰性越多,因羊水已進入腸道。
3.羊水磷脂醯甘油(PG)測定:出生後咽部或氣管吸出物作PG測定能早期提示發病可能。
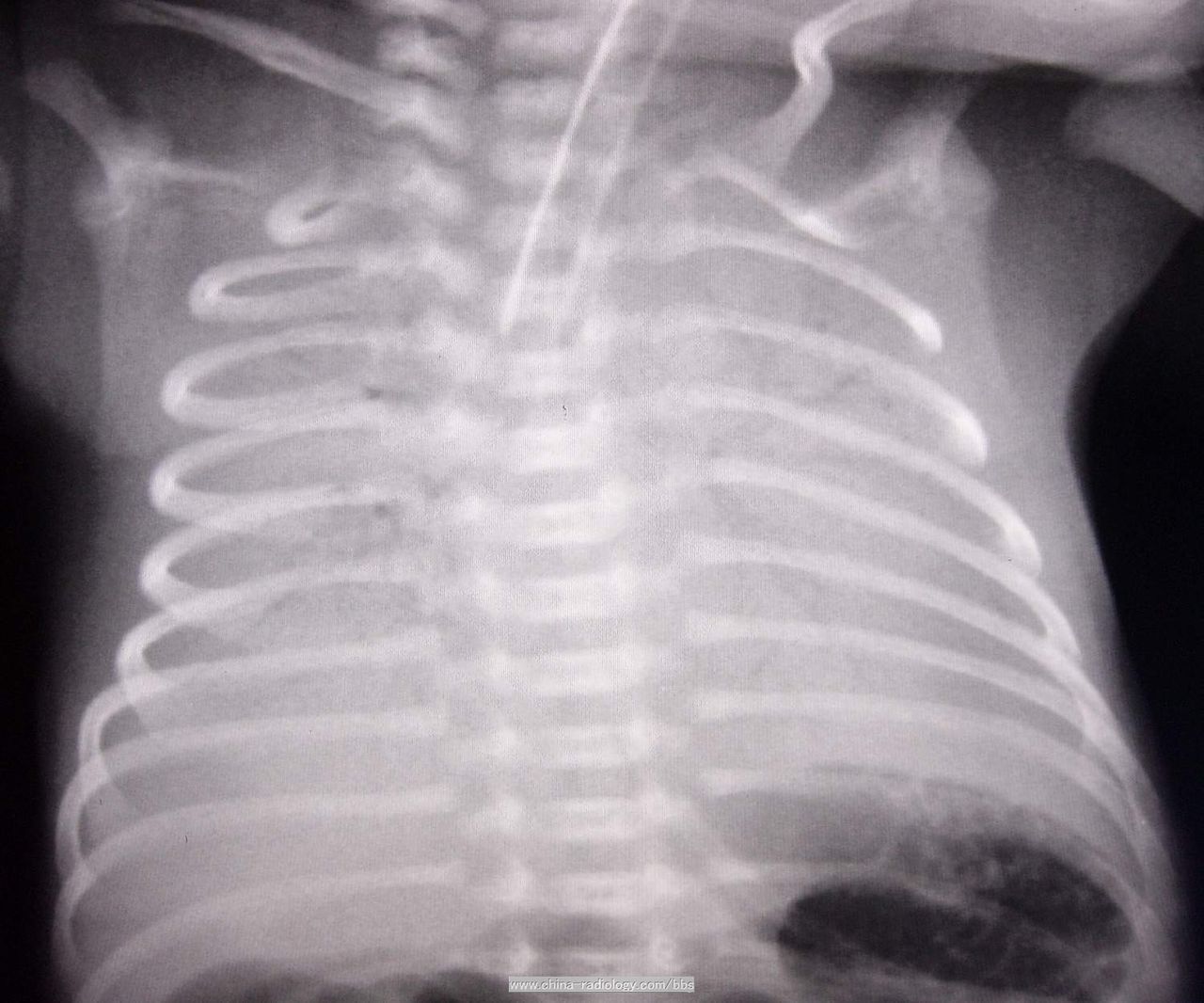
 新生兒肺透明膜病X線表現
新生兒肺透明膜病X線表現4.
血液檢查:血pH值、PaO2、HCO3-降低而PCO2、BE增高,呈代謝性酸中毒。血鉀早期常增高,恢復期利尿後可降低。
5.肺部X線檢查:按病情輕重可分四級。
第一級為細粟粒狀毛玻璃樣陰影,兩肺透亮度減低;
第二級除粟粒陰影外可見超出心影的空支氣管影;
第三級除上述影像外,心緣與隔緣模糊;
第四級為廣泛的白色陰影稱"白色肺",其中有黑色的禿葉樹枝狀空支氣管樹影由肺門向外周放射伸展至末梢氣道,形成"支氣管充氣征"。用高壓氧通入肺內,X線變化可獲改善。
鑑別診斷
1、B群β溶血性鏈球菌(GBS)感染 國內甚少見。臨床表現與胸片均像HMD,但患兒常有胎膜早破或
產程延長史,其母宮頸拭子GBS培養陽性,患兒胃液或氣管抽吸物可發現鏈狀排列的革蘭氏陽性球菌,尿液鏈球菌抗原試驗陽性。不能除外GBS感染時,可試用青黴素。
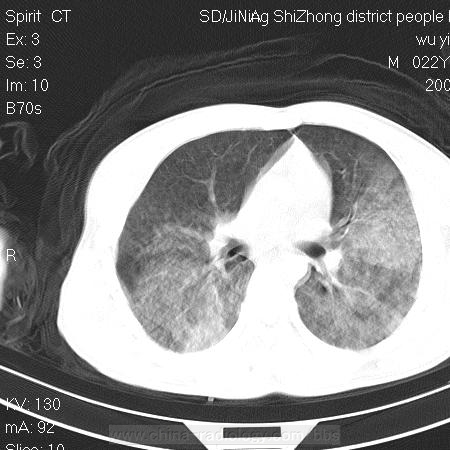 濕肺
濕肺2、
濕肺 多發生於
足月兒或剖宮產兒。病情較輕,病程較短,
預後良好。胃液振盪試驗陽性,胸片無HMD表現,肺氣腫、肺瘀血、葉間積液較常見,偶有胸腔少量積液。
3、胎糞
吸入性肺炎 多見於
足月兒、過期產兒,有窒息及胎糞吸入史。胃液振盪試驗陽性,胸片有不規則斑片狀陰影,肺氣腫明顯。
預防
做好
孕婦保健,防止早產。及早治療糖尿病孕婦,剖宮產儘可能推遲到分娩發作後施行。對可能早產、羊水振盪試驗陰性、L/S<2或PG<20mg/L的孕婦,如無嚴重高血壓或感染者,可在分娩前1~7天口服倍他米松0.5mg或地塞米松0.75mg,均1日3次,共2天;或靜注氫化可的松100mg,每12小時1次,共4次。
對可能發生本病的早產兒,尤其是氣管內抽吸物無PG或胃液振盪試驗陰性者可滴入1次表面活性物質150mg/kg,12小時後可再滴1次。
預後
病死率很高,早期套用加壓輔助通氣者大多可以存活。存活72小時以上者如無嚴重併發症,患兒常可產生足夠的表面活性物質,使病情逐漸好轉。並發
腦室出血者預後惡劣。
 新生兒肺透明膜病 病因
新生兒肺透明膜病 病因 新生兒肺透明膜病 病因
新生兒肺透明膜病 病因 呼吸膜結構
呼吸膜結構 新生兒肺透明膜病
新生兒肺透明膜病 新生兒肺透明膜病X線表現
新生兒肺透明膜病X線表現 濕肺
濕肺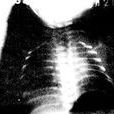
 新生兒肺透明膜病
新生兒肺透明膜病 早產兒
早產兒