在一個含有對峙反應的連續反應中,如果在對峙反應後存在速控步驟,則總反應速率及表觀速率常數僅取決於速控步及它以前的平衡過程,與速控步以後的各快反應無關。由於速控步反應很慢,可以假定快速平衡不受其影響,對峙反應的平衡關係仍然存在,從而利用平衡常數K及反應物濃度來求出中間產物的濃度,這種處理方法稱為平衡假設法(equilibrium hypothesis)。
基本介紹
- 中文名:平衡假設法
- 外文名:equilibrium hypothesis
- 又名:平衡態近似法
- 類別:物理化學
平衡假設法,注意事項:,
平衡假設法
平衡假設法是化學動力學中求解複合反應速率近似的一種重要方法。對於含有對峙反應的連續反應中,如果在對峙反應後存在速控步驟,則總反應速率及表觀速率常數僅取決於速控步及它以前的平衡過程,與速控步以後的各快反應無關。由於速控步反應很慢,可以假定快速平衡不受其影響,對峙反應的平衡關係仍然存在,從而利用平衡常數K及反應物濃度來求出中間產物的濃度。
對於反應機理:
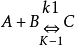

若 或
或 很大,且
很大,且 ,則第二步為控制步驟。而第一步事實上是處於化學平衡的。其正向逆向反應速率應近似相等。
,則第二步為控制步驟。而第一步事實上是處於化學平衡的。其正向逆向反應速率應近似相等。



K1CACB=K-1CC
即

反應的總速率控制等於控制步驟的反應速率:
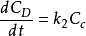
將 帶入上式得:
帶入上式得:

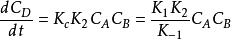
令 得速率方程:
得速率方程:


這就是用平衡近似法由反應機理求得的速率方程。
注意事項:
用平衡假設法從機理推導速率方程的思路首先是找出控制步驟,並將其速率除以該反應的計量數作為總反應的速率。然後套用控制步驟前的快速平衡步驟的平衡關係式消除該反應速率表達式中出現的任何中間體的濃度。
