語源學
chroma意為“色彩”,graphy源自希臘文,意為“寫”。
色譜為層析的同義語,都是從英語chromatography譯來的。
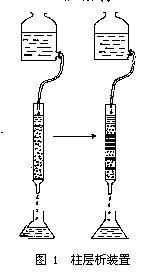
層析(色譜) chromatography
在把微細分散的固體或是附著於固體表面的液體作為
固定相,把液體(與上述液體不相混合的)或氣體作為移動相的系統中,使試料混合物中的各成分邊保持向兩相分布的
平衡狀態邊移動,利用各成分對固定相親和力不同所引起的移動速度差,將它們彼此分離開的定性與
定量分析方法,稱為層析,亦稱
色譜法。根據移動相種類的不同,分為液體層析、氣體層析二種。用作固定相的有
矽膠、活性炭、
氧化鋁、
離子交換樹脂、離子交換纖維等,或是在硅藻土和纖維素那樣的無活性的載體上附著適當的液體,也可使用其他物質。將作為
固定相的微細粉末狀物質裝入細長形圓筒中進行的層析稱為
柱層析(column chromatogra-phy),在
玻璃板上塗上一層薄而均的物質作為固定相的稱為薄層層析(thin-layer chromatography),後者可與用
濾紙作為固定相的
紙上層析進行同樣的分析,即在固定相的一端,點上微量試料,在密閉容器中,使移動相(液體)從此端滲入,移動接近另一端。通過這種展開操作,各成分呈斑點狀移動到各自的位置上,再根據Rf值的測定進行鑑定。當斑點不易為肉眼觀察時,可利用適當的
顯色劑,或通過紫外燈下產生螢光的方法進行觀察。也可採用在第一種移動相展開後再用另一移動相進行展開(這時的展開方向應與原方向垂直),使各成分分離完全的雙向層析(two-dimensional chromatography)。分離後,將斑點位置的
固定相切取下來,把其中含有來自試料的物質提取進行定量分析。但為製備與定量,
柱層析則更為適宜。在柱層析中,移動相從加入試料的一端展開到達另一端後,繼續展開使各成分和移動相一起向柱外分別溶出,這就是廣泛使用的所謂洗提層析(elution chromatography)。層析根據固定相與
溶質(試料)間親和力的差異分為吸附型、分配型、
離子交換型(
離子交換層析)等三種類型。但這並不是很嚴格的,有時常見到其中間類型。此外,近來也套用親和層析,即將與基質類似的化合物(通常為
共價鍵)結合到
固定相上,再利用其特異的親和性沉澱與其對應的特定的酶或蛋白質。
類別
◆按層析的機理劃分:
吸附層析:利用吸附劑表面對不同組分吸附性能的差異,達到分離鑑定的目的。
離子交換層析:利用不同組分對
離子交換劑親和力的不同。
凝膠層析:利用某些凝膠對於不同分子大小的組分阻滯作用的不同。
◆按流動相與固定相的不同劃分:
◆按操作形式劃分:
柱層析:將
固定相裝於柱內,使樣品沿一個方向移動而達到分離。
紙層析:用
濾紙做液體的載體,點樣後,用
流動相展開,以達到分離鑑定的目的。
薄層層析:將適當粒度的吸附劑鋪成薄層,以紙層析類似的方法進行物質的分離和鑑定。
以上劃分無嚴格界限,有些名稱相互交叉,如親和層析應屬於一種特殊的
吸附層析,紙層析是一種
分配層析,柱層析可做各種層析。
基本原理
層析須在兩相系統間進行。一相是
固定相,需支持物,是固體或液體。另一相為
流動相,是液體或氣體。當流動相流經固定相時,被分離物質在兩相間的分配,由
平衡狀態到失去平衡到又恢復平衡,即不斷經歷吸附和解吸的過程。隨著流動相不斷向前流動,被分離物質間出現向前移動的速率差異,由開始的單一區帶逐漸分離出許多區帶,這個過程叫展層。
係數K是物質在兩相中的濃度比。K值大,則在固定相中吸附牢,K值小吸附差。各物質間的K值差別大,則易被分離。不同類型層析的K值含義不同,可視為吸附平衡常數,
分配常數或
離子交換常數等。
研究層析現象而發展的
塔板理論,與有機化學實驗中的
分餾法原理有些相似。被分餾的有機溶劑在
分餾柱內的填充物上形成許多熱交換層,從而把低沸點溶劑先分餾出來,達到純化的目的。在層析時用
理論塔板數n來衡量層析效能。
tR為物質在
層析柱上的保留時間,W為洗脫下來的物質峰形的寬度。n值愈大表示層析柱的效能愈高。如用
理論塔板高度H表示,則包含了層析柱長度的因子。
式中L為層析柱的柱長。H值越大,則柱效越低。
此外影響層析分離效果的還有
渦流擴散、
縱向擴散和傳質阻抗等因素。因此選擇層析
固定相支持物的粒度、均勻度等物理性能,
流動相的層析系統和溫度等都是做好層析的關鍵。
常用層析
吸附劑的吸附力強弱,是由能否有效地接受或供給電子,或提供和接受活潑氫來決定。被吸附物的
化學結構如與吸附劑有相似的電子特性,吸附就更牢固。常用吸附劑的吸附力的強弱順序為:活性炭、
氧化鋁、矽膠、氧化鎂、
碳酸鈣、磷酸鈣、石膏、纖維素、澱粉和糖等。以活性炭的吸附力最強。吸附劑在使用前須先用加熱脫水等方法活化。大多數吸附劑遇水即鈍化,因此吸附層析大多用於能溶於
有機溶劑的有機化合物的分離,較少用於無機化合物。洗脫溶劑的解析能力的強弱順序是:醋酸、水、甲醇、乙醇、
丙酮、
乙酸乙酯、醚、氯仿、苯、
四氯化碳和己烷等。為了能得到較好的分離效果,常用兩種或數種不同強度的溶劑按一定比例混合,得到合適洗脫能力的溶劑系統,以獲得最佳分離效果。
在支持物上形成部分互溶的兩相系統。一般是
水相和有機溶劑相。常用支持物是矽膠、纖維素和澱粉等,這些親水物質能儲留相當量的水。被分離物質在兩相中都能溶解,但分配比率不同,展層時就會形成以不同速度向前移動的區帶。
支持物是人工交聯的帶有能解離
基團的有機
高分子,如
離子交換樹脂、離子交換纖維素、離子交換凝膠等。帶
陽離子基團的,如磺酸基(—SO3H)、羧甲基(—CH2COOH)和磷酸基等為陽離子交換劑。帶陰離子基團的,如DEAE—(
二乙基胺乙基)和QAE—(四級胺乙基)等為陰離子交換劑。離子交換層析只適用於能在水中解離的化合物,包括有機物和
無機物。對於蛋白質、核酸、胺基酸及核苷酸的分離分析有極好的分辨力。離子交換基團在
水溶液中解離後,能吸引水中被分離物的離子,各種物質在
離子交換劑上的離子濃度與周圍溶液的離子濃度保持
平衡狀態,各種離子有不同的交換常數,K值愈高,被吸附愈牢。洗脫時,增加溶液的
離子強度,如改變pH,增加鹽濃度,離子被取代而解吸下來。洗脫過程中,按K值不同,分成不同的區帶。
支持物是人工合成的交聯高聚物,在水中膨脹後成為凝膠。凝膠內為內水層,凝膠周圍的水為外水層。控制
交聯度以形成不同
孔徑的
網狀結構。交聯度小的孔徑大,交聯度大的孔徑小。凝膠只允許被分離物質中小於孔徑的分子進入,大於孔徑的分子被排斥在外水層,最先被洗脫下來。而進入孔徑的分子也按分子量大小大致分離成不同的區帶。選擇不同規格的凝膠,可把一個混合物按分子量的差異分成不同的組分。這種方法曾被稱為分子篩。目前常用的凝膠商品有:
葡聚糖凝膠(sephadex)、
聚丙烯醯胺凝膠(bio-gel)、
瓊脂糖凝膠(sepharose)和
聚苯乙烯凝膠(styragel)等。
在一對有專一的相互作用的物質中,把其中之一聯結在支持物上,用於純化相對的另一物質。常見的親和對如:酶和抑制劑,抗原和抗體,激素和
受體等。支持物為瓊脂糖或纖維素等。
屬於
分配層析或
吸附層析,僅適用於分析分離
揮發性和低揮發性物質。
固定相是在惰性支持物(如磨細的
耐火磚)上覆蓋一層高沸點液體,如矽油、高沸點
石蠟和油脂、環氧類聚合物。外塗層約為支持物重量的20%。分析時操作溫度範圍,一般從室溫到200℃。特殊的
層析柱能達到500℃。
流動相常用氦、氬或氮為展層氣體。氣相層析分離的區帶十分清晰,是由於揮發性物質在兩相間能很快達到平衡,所需分析時間大為縮短,一般為數分鐘至10餘分鐘。檢測記錄系統繪出的各峰是測定流出氣體電阻變化的結果,因而測定樣品量可到微克和毫微克水平。具有快速、靈敏和微量的優點。氣相層析也能用於分離製備樣品,但需增加將流出氣體通過冷凍將分離物回收的裝置。
以
濾紙為支持物的
分配層析。組成濾紙的纖維素是親水物質,能形成
水相和展層溶劑的兩相系統,被分離物質在兩相中的分配保持平衡關係。紙層析用於分析簡單的混合物時可做單向層析。對於複雜的混合物,可做
雙向層析。1944年A.J.P.馬丁第一次用紙層析分析胺基酸,得到很好的分離效果,開創了近代層析的發展和套用的新局面。70年代以後,紙層析已逐漸為其他分辨力更高、速度更快和更微量化的新方法,如
離子交換層析、薄層層析、高效
液相層析等所代替。
在玻璃片、金屬箔或塑膠片上鋪上一層約1~2毫米的支持物,如纖維素、矽膠、
離子交換劑、氧化鋁或
聚醯胺等,根據需要做不同類型的層析。
聚醯胺薄膜是一種特異的薄層,將
尼龍溶解於濃甲酸中,塗在
滌綸片基上,當甲酸揮發後,在滌綸片基上形成一層多孔的薄膜,其分辨力超過了用尼龍粉鋪成的薄層。薄層層析較紙層析優越在於分辨高,展層時間短。例如用紙層析做
胺基酸分析,往往需要兩天時間,而且對層析條件要求嚴格,不易得到滿意的分離效果。如用薄層層析做,一般約需半小時,分離效果更好。薄層層析一般用於定性分析。也能用於定量分析和製備樣品。
70年代新發展的層析法。其特點是:用高壓輸液泵,壓強最高可達5000psi(相當於34個
標準大氣壓)。用直徑約3~10微米的超細支持物裝填均勻的不鏽鋼柱。常用的支持物是在玻璃小珠上塗一層1~2微米的
二氧化矽,經
硫醯氯反應生成Si—Cl,進一步連線疏水的烷基,如Si—C18H37,或陽離子交換基團—Si(CH2)n—C6H4SO3H,或
陰離子交換基團—Si(CH2)nNH2。這種支持物能承受很高的壓力,化學性能穩定。用不同類型支持物的HPLC,可做
吸附層析、
離子交換層析和
凝膠過濾層析。其分析微量化可達10-10克水平。但用於製備,可以純化上克的
樣品。展層時間短,一般需幾分鐘到10餘分鐘。其分析速度、
精確度可與氣相層析媲美。HPLC適於分析分離不揮發和
極性物質。而氣相層析只適用於
揮發性物質,兩者互為補充,都是目前最為理想的層析法。HPLC配有程式控制洗脫溶劑的梯度混合儀,數據處理的積分儀和記錄儀等
電子系統,成為一種先進的分析儀器,在生物化學、化學、醫藥學和環境科學的研究中發揮了重要作用。
在
吸附層析中,高極性物質在
層析柱上吸附較牢,洗脫時發生拖尾現象和保留時間長的問題。如果在支持物上塗上一層高碳原子的疏水性強的
烷烴類,洗脫液用極性強的溶劑,如甲醇和水的混合物。則被分離樣品中的極性強的物質不被吸附,最先洗下來,得到較好的分離效果。這種層析法與普通的
吸附層析法相反,故稱為反相層析。目前用HPLC做反相層析常用的ODS柱,即在支持物的表面上連線了C18H37Si—基團。
在核酸分析中,將樣品經
核酸酶部分裂解成不同長度的
核苷酸片段,用
同位素標記後,在DEAE纖維素薄層上分離,用含有未標記的相同的核苷酸片段作展層溶劑,這樣,未標記的核苷酸把標記過的核苷酸推進,使按分子量大小不同把標記核苷酸片段,按由小到大的次序排列,達到分離的目的。於是把這種層析法稱為同系層析。同系層析和電泳相結合曾用於寡核苷酸的順序分析。
紙層析是層析法的一種,要了解紙層法還得從層析法開始.層析法又稱色層分析法或
色譜法(Chromatography),是一種基於被分離物質的物理、化學及生物學特性的不同,使它們在某種基質中移動速度不同而進行分離和分析的方法。例如:我們利用物質在溶解度、吸附能力、立體化學特性及分子的大小、帶電情況及
離子交換、親和力的大小及特異的生物學反應等方面的差異,使其在
流動相與
固定相之間的分配係數(或稱
分配常數)不同,達到彼此分離的目的。
層析法的最大特點是
分離效率高,它能分離各種性質極相類似的物質。而且它既可以用於少量物質的分析鑑定,又可用於大量物質的
分離純化製備。因此,作為一種重要的分析分離手段與方法,它廣泛地套用於科學研究與工業生產上。現在,它在石油、化工、醫藥衛生、生物科學、環境科學、農業科學等領域都發揮著十分重要的作用。
層析根據
固定相基質的形式分類,層析可以分為紙層析、薄層層析和
柱層析。其中紙層析是指以
濾紙作為基質的層析。
層析發展
起步期
在層析技術發展之初,對於一些物質的分離方式都處在比較原始的狀態,並且分離的結果也並不是很理想。
bio-rad專家談到層析技術最初是在1903~1906年由俄國植物學家M.Tswett首先提出來的。
那時,他將葉綠素的石油醚溶液倒入碳酸鈣管柱,並繼續以石油醚淋洗,由於碳酸鈣對葉綠素中各種色素的吸附能力不同,所以色素被逐漸分離,在管柱中出現了不同的色譜圖。於是就稱這種混合物的分離方法為,有色的圖譜法(Chromato+graphy),簡稱色譜法,又叫層析法。不過,當時這種方法並未引起人們的注意。
接下來隨著科學技術的發展以及生產實踐的需要,層析技術也得到了迅速的發展。這裡就不得不提到兩位在層析技術發展史上做出重要貢獻的人,他們是英國生物學家馬丁(Martin)和辛格(Synge)。是他們首先提出了色譜塔板理論。
色譜塔板理論其實是基於熱力學近似的理論,這個理論中涉及的對象有目標分離物,色譜柱。這裡色譜柱好比是一個分餾塔。理論是這樣的:將目標分離物倒入“分餾塔”,這樣就會在分餾塔板間移動,在每一個塔板內組分分子在固定相和流動相之間形成平衡,隨著流動相的流動,組分分子不斷從一個塔板移動到下一個塔板,並不斷形成新的平衡。一個色譜柱的塔板數越多,則其分離效果也就越好。這個分離過程提升分離效率,並且定量的進行描述,分析這個分離過程。
這是個進步,並且馬丁(Martin)和欣革(Synge)還提出更為遠見卓識的預言:1、流動相可用氣體代替液體,因為與液體相比,分離時候,物質間作用力更小,對分離也就更有好處。2、若能夠使用非常細的顆粒填料,並在色譜柱兩端施加較大的壓差,從而增加了理論培板數,這將會大大提高分離效率。
發展期
上世紀60、70年代是色譜/層析技術快速發展的時代,首先是層析介質有了飛速的發展,各種人工合成的介質出現,如矽膠、聚苯乙烯二乙烯基樹脂、瓊脂糖、葡聚糖、聚丙烯醯胺等樹脂或凝膠的出現,極大地拓展了層析技術的套用領域和範圍,基於不同介質的層析方法也如雨後春筍般不斷湧現。
現代層析法特點
色譜法或是層析法是簡單點說,就是依據被分離物的物理、化學及生物學特性的不同,使它們在某種基質中移動速度不同而進行分離和分析的方法。


