反向色譜是指固定相的極性低於流動相的極性,在這種色譜分離過程中,極性大的分子比極性小的分子移動速度快而先從柱中流出。一般來說,分離純化極性大的分子(帶電離子等)採用正相色譜(或正相柱),而分離純化極性小的有機分子(有機酸、醇類、酚類等)多採用反向色譜(或反向柱)。反向色譜中使用的色譜柱即為反向離子色譜柱。
基本介紹
- 中文名:反向離子對色譜柱
- 外文名:Invert ion chromatographic column
- 用途:反向離子對色譜技術中
- 組成:固定相,流動相等
- 原理:極性大分子比小的先從柱中流出
- 套用:分離純化極性小的有機分子
反向離子對色譜柱介紹,反向離子對色譜柱系統的選擇,色譜柱的選擇,離子對試劑的選擇,有機溶劑的選擇,無機鹽濃度的影響,pH值影響,柱溫的選擇,反向離子對色譜柱在使用中需要注意的問題,
反向離子對色譜柱介紹
1、C18是連線了18烷基碳鏈的反相固定相的總稱。ODS是以矽膠為基質鍵合的C18填料,而C18還包括其他基質的填料,比如高聚物小球為基質,氧化鋁為基質,氧化鋯為基質等鍵合C18鏈形成的反相固定相,這些可以稱為"C18",但是不是ODS。
2、RP-18也是C18中的一種,不同的公司對C18填料有不同的商名稱,本質應該都是一樣的。Merck公司的填料喜歡叫RP-18。比如Merck的LiChrospherRP-18,SuperspherRP-18,PurospherRP-18。因此,有人認為說"RP-18"是改進型是不妥當的。Merck的改進表現在前邊的名字上,比如LiCHrospher,Superspher,Purospher表現的是不同的性能。
3、C8是矽膠鍵合辛烷基,C18是矽膠鍵合十八烷基,C18的極性較C8的極性小,C18對分析物的保留性能強於C8,含碳量對分離效果和主要組分的保留時間起很大的影響,所以含碳量高,主要組分的保留時間越長。C8和C18都是反相色譜柱的一種,適用於分析弱極性的物質,C8適合分析弱極性物質里極性稍強的一類物質,C18適合分析弱極性物質里極性更弱的物質。這是他們極性上的差別,但是差別並不是特別明顯,一般能用C8分析的物質,在C18上也能分離。C18比C8的碳鏈更長,因此帶來更好的保留特性。因此C8就更適合分析大分子類的物質,比如一些球蛋白等,都用C8和緩衝鹽洗脫劑來配合使用。相反,分子量較小的物質,經常用C18來進行分析和分離。鍵合相不同,導致同種組分在不同色譜柱上的保留時間不一致,對各組分的保留能力也會不同,峰位置就變化了。
C18前面看到“ODS”的字樣,ODS是英文octadecylsilane的所寫,意思是十八(烷)基矽烷,是以矽膠為基質鍵合的C18填料,由於大部分的C18柱都是矽膠基質,因此有時還會看到色譜柱上只標稱二者之一。其中以ODS居多。有時你還會看到ODS-x,x是不同的數字,這個x雖然是數字,但是不同廠家的產品代表的含義不同,一般以含碳量區分,但這也不是絕對的。有時還可能看到RP-18或RP-8,RP-18和C18意義基本一致,但是不同的廠家有不同的規定。RP-C8、RP-C18,這裡的RP是指"ReversalPhase",就是“反相”的意思,所以RP-C8、RP-C18就是指反相C8和反相C18。其實C8和C18也沒怎么見過用於正相,它們本身就是反相柱,只是商家為了區別其它的C8或C18做出的一個標識。鍵合烷基的鏈長對鍵合相的樣品負荷量、溶質的容量因子及其選擇性有不同的影響,當烷基鍵合相表面濃度相同時,隨著烷基鏈長增加,碳含量成比例增加,溶質的何留值增加。C18、C6、C8短鏈烷基,由於分子尺寸較小,與矽膠表面鍵合時可以有比長鏈烷基更高的覆蓋和較少的殘餘羥基,適合極性樣品或做離子抑制的樣品的分析。一般說,C18比C8的分離效果好。但是如果遇到性質差別比較大的樣品,也就是說比較容易分離的樣品,C8比C18的效率高。
反向離子對色譜柱系統的選擇
為了獲得滿意的分離分析結果,反向離子對色譜中應考慮的主要因素如下:
(1)選擇合適的色譜柱,一般來說C18或C8是優先選擇的填料。
(2)甲醇,水可作為沖洗劑的初始選擇,如需要提高分離選擇性,乙腈可以代替沖洗劑中的甲醇。 ·
(3)在不損害色譜柱穩定性的前提下,沖洗劑緩衝液的pH值應使被分離物質達到最大離解度。為了避免鹽析效應,緩衝液的鹽濃度應在1Xl0-2到5X10-3mol/l範圍內。
(4)儘可能確定被分離物質的物化性質:它們是強酸、強鹼、弱酸、弱鹼或中性化合物。
(5)選擇一個適當的離子對試劑,對於烷基很大的離子對試劑其初始濃度在5 mmol/l左右比較合適,對烷基較小的離子對試劑其初始濃度選在10 mmol/l比較合適。要確認離子對試劑完全溶於流動相中並與相應的檢測器相兼容。
色譜柱的選擇
對於一般的離子對色譜分離系統,高鍵合量的10 μmC18擔體的填充柱或5μmC18擔體的填充柱可作為第一選擇。C18擔體的柱尺寸250X4.5 mm左右比較合適。此外,高鍵合量的C8擔體也可作為離子對色譜的柱填料。儘管至今從理論上還很難闡明不同廠家填充擔體的差別對分離效果有什麼影響,但許多實踐表明,填料的鍵合量和鍵合碳鏈的構型對分離選擇性有一定的影響。所以在很多情況下,很多重要文獻中已獲得的分離結果,我們只能依據文獻中的分離條件為出發點重新尋找新的分離條件。其最根本的原因是擔體的重複性較差。
離子對試劑的選擇
離子對試劑的種類、大小相濃度對分離效果都有重要的影響,離子對試劑種類的選擇依靠被分離樣品的性質,圖1列出的是離子對試劑的一般性選擇原則。如被分離溶質是強酸或強鹼,則選用的離子對試劑可以是強鹼、弱鹼或強酸,弱酸;如被分離的溶質是弱酸或弱鹼,則選用的離子對試劑必須是強鹼或強酸,圖1列出的是對應於被分離樣品的種類所選用的離子對試劑種類。對於溶質結構性質相差較大的混合樣品,對離子對試劑種類的選擇並沒有特殊要求,離子對試劑疏水性的差別可以通過調節離子對試劑濃度和有機溶劑濃度獲得滿意的分離效果。但如被分離物質的結構性質很相似,則離子對試劑的選擇又可能對分離選擇性發生作用。如十二烷基硫酸鹽和十二烷基磺酸鹽對兒茶酚胺的分離表現出不同的選擇性。這種差別至今很難從理論上獲得完善的解釋。只有通過實驗比較來實現。對於疏水性較大的離子對試劑,其濃度在4~10 mmol/l比較台適.對疏水性較小的離子對試劑,其濃度在10~40 mmol/l比較合適。 圖1 反向離子對色譜用離子對試劑的選擇
圖1 反向離子對色譜用離子對試劑的選擇
 圖1 反向離子對色譜用離子對試劑的選擇
圖1 反向離子對色譜用離子對試劑的選擇有機溶劑的選擇
有機溶劑是調節溶質在離子對色譜中保留值的重要參數。在反相離子對色譜中,有機溶劑對保留值的影響主要通過改變溶質與流動相間的相互作用和離子對試劑在固定相表面的吸附量來實現,從我們研究的結果來看,有機溶劑疏水性對保留值有較大的影響,但對它們的選擇性無明顯的影響。因此對有機溶劑種類的差別對保留值的影響可以由有機溶劑濃度的改變來補償。
無機鹽濃度的影響
無機鹽濃度的增大將降低溶質在反相離子對色譜中的保留值,這主要由與溶質電荷同號的離子與溶質競爭吸附或競爭與離子對試劑配對,從而減弱溶質與離子對試劑的相互作用來產生。一般來說,鹽濃度對保留值的影響比有機溶劑和離子對試劑的影響要小。在恆定其它條件下,改變鹽的種類對保留值也有一定影響。一般情況下,無機鹽濃度控制在10~50 mmol/l比較合適。有研究表明,無機鹽濃度梯度沖洗可以改善複雜樣品的分離度。
pH值影響
眾所周知,對於酸性溶質pH>>pKa時,溶質將以離子狀態存在。此時,離子對試劑的保留值發揮非常重要的作用,而當pKa>>pH時,溶質將以中性狀態存在,離子對試劑對保留值幾乎無作用。pH值對有機鹼的影響與pH值對有機酸的影響恰好相反。與反相色譜中pH值的影響相似,pH值是影響保留值和選擇性最重要的因素之一。因此,在反相離子對色譜中,選擇合適的緩衝液,以使被分離物質以所需的狀態存在是非常必要的。圖2列出的是一些被分離樣品選擇流動相pH值的基本原則。值得注意的是,在特定pH值下,某些被分離溶質沒有完全解離,酸鹼平衡的慢動力學過程可能引起分裂峰和峰展寬。
柱溫的選擇
隨著柱溫升高,反相離子對色譜中的保留值下降,但柱溫對k'的影響沒有像有機溶劑、離子對試劑和pH值以及鹽濃度那樣明顯。在一般情況下,室溫就可以滿足離子對色譜的分離要求。必須注意的是柱溫對某些樣品的分離最佳化條件很有幫助。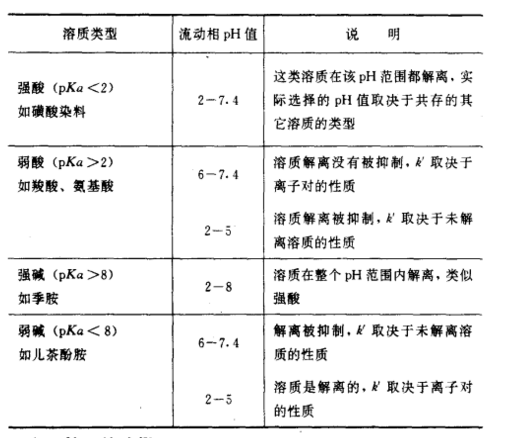 圖2 反相離子對色譜沖洗劑pH值選擇
圖2 反相離子對色譜沖洗劑pH值選擇
 圖2 反相離子對色譜沖洗劑pH值選擇
圖2 反相離子對色譜沖洗劑pH值選擇反向離子對色譜柱在使用中需要注意的問題
由於反相離子色譜法中使用了離子對試劑和無機鹽,因此在操作上要注意以下幾個方面:
1、改變沖洗劑濃度或梯度沖洗操作後,柱系統的沖洗時間要長些,以保證柱內平衡;
3、一經發現離子對試劑在柱內產生了不可逆吸附,則須用甲醇沖洗柱子。

