基本介紹
- 中文名:前線軌道
- 外文名:Frontier Molecular Orbital
- 提出:福井謙一
- 學科:物理、化學
- 研究:分子軌道
概念
產生和發展
前線軌道理論
套用
芳香族取代反應
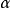

 圖(1)
圖(1)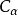
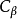


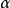
加成反應

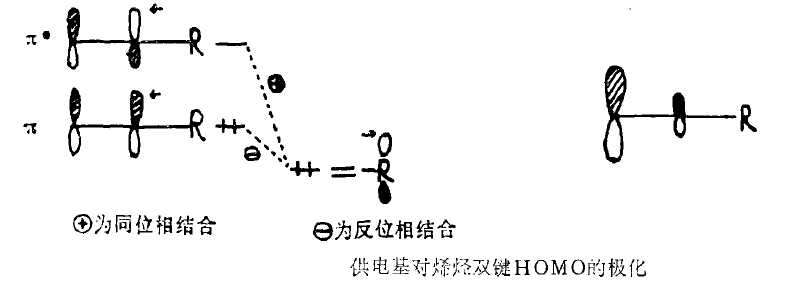 圖(2)
圖(2)
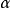

 圖(1)
圖(1)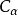
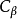


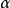

 圖(2)
圖(2)分子軌道中,最高占有分子軌道和最低未占有分子軌道統稱為前線軌道。處在前線軌道中的電子就像原子軌道中的價電子一樣是化學反應中最活潑的電子,是有機化學反應的...
前線軌道理論,是一種分子軌道理論,是日本理論化學家福井謙一賴以成名的理論,這一理論將分子周圍分布的電子云根據能量細分為不同能級的分子軌道,福井認為有電子排布...
分子軌道中,最高占有分子軌道(HOMO)和最低未占有分子軌道(LUMO)統稱為前線軌道。處在前線軌道中的電子就象原子軌道中的價電子一樣是化學反應中最活潑的電子,是有...
前線分子軌道理論,簡稱“前線軌道理論”。解釋化學中成鍵規律的定性理論。是日本化學家福井謙一於1952年提出。...
前線(分子)軌道理論frontier (maleculGr) orhital theory福並謙一於20世紀50年代提出的一種分子軌道理論。...
已占有電子的能級最高的軌道稱為最高已占軌道,用HOMO表示。未占有電子的能級最低的軌道稱為最低未占軌道,用LUMO表示。HOMO、LUMO統稱為前線軌道,處在前線軌道上...
分子軌道(MO)可用原子軌道線性組合。是可以通過相應的原子軌道線性組合而成。有幾個原子軌道相組合,就形成幾個分子軌道。在組合產生的分子軌道中,能量低於原子軌道的...
highest occupied molecular orbital;HOMO 最高占據分子軌道。 在已占據電子的分子軌道中,能量最高的分子軌道。 類似地,在未被電子占據的分子軌道中,能量最低的分子...
LUMO是未占有電子的能級最低的軌道。...... 前線軌道 LUMO和HOMO統稱 化學鍵 主要是由FMO的相互作用所決定的 LUMO:Lowest Unoccupied Molecular Orbital,未占有電子...
軌道是由原子前線軌道線性組合而成。若A原子的電負性比B原子大,則其前線軌道能級比B原子前線軌道能級低。在形成共價鍵過程中,能量低的成鍵軌道(Bonding Orbital)的...
前線軌道是由日本理論化學家福井謙一提出的,他指出化合物分子的許多性質主要出最高占據分子軌道相最低未占分子軌道所決定的。凡是處於前線軌道的電子,可優先配對。...
根據前線軌道理論,假定反應中發生遷移的σ鍵首先發生均裂,生成一個氫原子(或碳自由基)和一個奇數碳的共軛體系自由基,而反應的實質是氫原子(或碳自由基)在奇數碳...
1965年,美國化學家羅伯·伍德沃德(Rober B.Woodward)與霍夫曼參照福井謙一的前線軌道理論,提出了分子軌道對稱守恆原理。分子軌道理論得到了新的發展。 [1] ...
HOMO-LUMO能級統稱前線軌道,分別指最高占據分子軌道(Highest Occupied Molecular Orbital)和最低未占分子軌道(Lowest Unoccupied Molecular Orbital)。HOMO和LUMO分別指...
LUMO是未占有電子的能級最低的軌道。...... 前線軌道理論的創始人福井謙一指出,分子軌道中能量最高的填有電子的軌道和能量最低的空軌道在反應中是至關重要的。福...
已占有電子的能級最高的軌道稱為最高已占軌道,用HOMO表示。未占有電子的能級最低的軌道稱為最低未占軌道,用LUMO表示。HOMO、LUMO統稱為前線軌道,處在前線軌道上...
