《一種銀杏內酯的藥物組合物》是孫毅於2006年7月26日申請的專利,該專利的申請號為2006101036260,公布號為CN1887283,授權公布日為2007年1月3日,發明人是孫毅。
《一種銀杏內酯的藥物組合物》公開了一種含銀杏內酯注射液。這種注射液中各成份及各成份的比例與所投的銀杏內酯提取物是一致的。而且與銀杏葉中的成份具高度相關性並且能在很長時間內保持穩定。能夠最大限度地發揮白果內酯促進神經生長的作用,以及防止腦、脊髓神經脫髓鞘作用,防止老年性痴呆的發生和發展的作用。
2016年12月7日,《一種銀杏內酯的藥物組合物》獲得第十八屆中國專利優秀獎。
基本介紹
- 中文名:一種銀杏內酯的藥物組合物
- 公布號:CN1887283
- 授權日:2007年1月3日
- 申請號:2006101036260
- 申請日:2006年7月26日
- 申請人:孫毅
- 地址:四川省成都市高新區高朋大道3號A座310
- 發明人:孫毅
- Int.Cl.:A61K31/365(2006.01);A61K9/08(2006.01);A61K9/107(2006.01);A61K9/20(2006.01);A61K9/22(2006.01)等
- 類別:發明專利
專利背景,發明內容,專利目的,技術方案,改善效果,附圖說明,技術領域,權利要求,實施方式,榮譽表彰,
專利背景
銀杏內酯是從中草藥銀杏葉當中提取獲得的有效物質,銀杏內酯是二萜烯類化合物,是包括1個四氫呋喃環、3個r-內酯基和由2個戊碳環連結在1個碳原子上形成的螺[4,4]壬烷系統,共6個戊碳環與叔丁基相結合的獨特的C20籠蔽分子。其順式稠環F、A、D與C被塑造成半球形的空腔,這個空腔是足以容納1個陽離子或陽性極化的有機分子。
P.Braquet等(1988)報導已知的銀杏內酯有5種,用A、B、C、M、J命名(GinkgolidesA、B、C、M、J),銀杏內酯的基本結構是共同的,不同的銀杏內酯之間的差別僅是羥基的數目與位置的不同。銀杏內酯M與J,實際上是銀杏內酯B的同分異構物。銀杏內酯A.B.C既存在於銀杏根皮內,也存在於銀杏葉內,銀杏內酯M僅存在於根皮內;銀杏內酯J發現較晚,僅存在於銀杏葉內。銀杏內酯的化學性質不活潑,是極為穩定的。
對於銀杏內酯的提取方法已經有詳細的文獻報導,例如,李新崗等人介紹了銀杏內酯的實驗室提取方法(參加李新崗等,銀杏葉中銀杏內酯的實驗室提取方法研究,中國醫藥工業雜誌1998第1期),中國專利文獻CN1195665A介紹了銀杏內酯的提取方法和含有銀杏內酯的製劑,該方法是將銀杏葉用水煮沸提取,用吸附劑對提取濾液吸附,再用乙醇脫附,回收乙醇,將析出的結晶溶解,重結晶,乾燥製得銀杏內酯。中國專利文獻CN1313287A公開了一種銀杏內酯的生產工藝。從銀杏內酯的總提取物當中分離銀杏內酯單體的方法,也有很多相關的文獻報導,例如,游松等人介紹了銀杏內酯中銀杏內酯的分離與結構測定方法(參見游松等,銀杏葉中銀杏內酯的分離與結構測定,中國藥物化學雜誌1995年第4期)。中國專利文獻CN1287121A公開了由銀杏葉或銀杏葉浸膏製備藥物銀杏內酯A、B的方法。銀杏內酯作為一個有效的活性物質,可以將其製備成不同的臨床藥物劑型。劉潔等使用銀杏葉注射劑治療急性腦梗塞取得了一定療效[參見劉潔等,銀杏葉注射液對急性腦梗塞後肢體運動功能及TXB-2、6-Keto-PGF-(la)的影響]。關於銀杏內酯的藥理作用,已經有較為詳細的文獻報導(參見陳維軍等,銀杏內酯的化學結構及藥理作用研究進展,中國藥學雜誌1998年第9期)。儘管2006年7月前技術當中對於銀杏內酯及其製劑的研究已經有很多的報導,但是,對於銀杏內酯的研究一直沒有停止,特別是對於銀杏內酯單體的分離及其衍生物的研究,不斷有文獻報導。截至2006年7月,對於銀杏內酯當中有效單體的研究,已經報導了銀杏內酯A、B、C等結構,將銀杏內酯製備成注射劑,很重要一項技術問題是如何解決其難溶解性,銀杏內酯注射劑製備過程當中,對於助溶劑的選擇也非常重要,這直接影響到產品的穩定性和臨床療效。
根據銀杏內酯的內酯環結構,一般很容易想到用酸或鹼使開環,或者用有機溶劑溶解,但是它在一般的有機溶劑中溶解性也很差,如乙醇,聚乙二醇400,甘油,丙二醇中溶解度都很小。所以,截至2006年7月,銀杏內酯製備注射劑的方法有通過使用鹼溶液增加銀杏內酯的溶解性而製得,例如CN200510040497.0,CN00115134.7,CN02134223.7。加入葡甲胺的情況下,對銀杏內酯有很好的助溶作用例如CN02128962.X。對銀杏內酯採用羥丙基-β-環糊精增溶製得的水溶液例如CN200510072466.3,CN200410013937.9,CN200410041120.2。另外,CN03100334.6公開針劑中含有5-99%銀杏葉提取物、1-95%泊洛沙姆188和pH值調節劑以及其它賦形劑。CN03137720.3一種銀杏內酯B針劑的製備方法,將銀杏內酯B原料溶解於注射用非水溶劑聚乙二醇中,聚乙二醇可單獨使用或與無水乙醇配成混合溶劑,按體積計,聚乙二醇:乙醇=0.5:0.5~0.9。
這些方法中,加羥丙基-β-環糊精,泊洛沙姆,聚乙二醇等試劑,其作為注射液的安全性值得商榷。羥丙基-β-環糊精具有潛在的腎毒性,截至2006年7月,僅用抗真菌藥伏力康唑注射液中,在中國沒有作為合法的注射用附加劑。泊洛沙姆因為安全性問題在中國也沒有作為合法的注射用附加劑。聚乙二醇濃度較大時有溶血的危險。所以基本無實用的可能。加鹼或加葡甲胺都屬於讓內酯開環成鹽,在中性或酸性條件下,很難形成有藥效形式的內酯原形,甚至沒有白果內酯。而白果內酯是銀杏中最受關注的化學成分,動物試驗報導,白果內酯具有促進神經生長的作用,以及防止腦、脊髓神經脫髓鞘作用,其神經營養、神經保護作用比銀杏內酯強。近年來還發現白果內酯可防止腦細胞線粒體氧化應激引起的功能改變,選種抗氧化應激對改善老年記憶功能,防止老年性痴呆的發生和發展起到有益的作用,因此國際上對銀杏提取物的要求(德國衛生部CommissionE制訂的規格)是,白果內酯含量應為2.6-3.2%。
為了解決有效性問題。《一種銀杏內酯的藥物組合物》公開了一種銀杏內酯注射液的處方,能使所投的銀杏內酯原料與銀杏內酯注射液,各組份和比例保持不變。並且與銀杏葉中的組份比例接近。
銀杏內酯A18%-36%、銀杏內酯B10%-29%、銀杏內酯C15%-24%、白果內酯12%-57%。平均為26%,18%,19%,36%。(參見唐紅芳等的銀杏葉中銀杏萜內酯的GC-MS定性定量分析,中草藥,第34卷第3期2003年3月)
發明內容
專利目的
《一種銀杏內酯的藥物組合物》的目的是提供一種含有銀杏內酯的製劑,特別是銀杏內酯注射液,同時還提供該注射液的製備工藝。
技術方案
《一種銀杏內酯的藥物組合物》所述的銀杏內酯的製劑是以高純度的銀杏內酯為有效成份製備而成,銀杏內酯A,銀杏內酯B,銀杏內酯C,白果內酯之和大於總提取物的80%以上(重量比)。
《一種銀杏內酯的藥物組合物》的注射液的各組成部分的重量比為:銀杏內酯:乙醇:甘油:水=(0.05%~1.5%):(20%~70%):(10%~40%):(20%~70%)。
上述組份的優選重量比為:銀杏內酯:乙醇:甘油:水=(0.2%~0.7%):(30%~50%):(10%~30%):(30%~50%)。
其中還需加入適量的10%檸檬酸溶液調節pH值。
製劑處方:處方(以1000劑量單位計):銀杏內酯10克、甘油400毫升、乙醇800毫升、注射用水加至2000毫升、製成1000支。
製備方法:取處方量約80%的注射用水,處方全量的甘油和乙醇,置配液缸中,加入處方量的銀杏內酯,攪拌溶解後,加注射用水至全量,用10%檸檬酸溶液調節pH,攪勻,半成品檢驗合格後,用0.65微米和0.45微米複合耐醇微孔濾膜作濾材的微膜過濾系統過濾澄明,灌封於2毫升玻瓶中,於100℃滅菌20分鐘,冷卻,燈檢,貼標,即得。
製備《一種銀杏內酯的藥物組合物》銀杏內酯杏內酯注射液所使用的銀杏內酯原料,可以通過已知的提取方法提取,或者通過市售購得,但是銀杏內酯A、B、C和白果內酯的比例應該與銀杏葉中的比例大體一致。
銀杏內酯B10%~90%;白果內酯10%~90%(重量比)
更優選:銀杏內酯A:銀杏內酯B:銀杏內酯C:白果內酯為(10%~45%):(5%~40%):(3%~35%):(10%~70%)。
更優選:銀杏內酯A:銀杏內酯B:銀杏內酯C:白果內酯為(15%~40%):(7%~30%):(5%~20%):(20%~60%)。
含量測定用高效液相色譜一蒸發光散射檢測法(HPLC-ELSD)直接測定銀杏葉中銀杏萜類內酯A、B、C及白果內酯的含量。方法:10%甲醇製作供試品溶液,經C18色譜柱,以甲醇一水為流動相。梯度洗脫,以蒸發光檢測器檢測。(參見顏玉貞,謝培山HPLC-ELSD法測定銀杏葉中的4種萜類內酯含量《藥物分析雜誌》:2001年21卷3期173-176頁)。
從所投料的銀杏內酯原料和所得成品的HPLC圖譜上可見:銀杏內酯A、B、C及白果內酯各成份及各成份的比例沒有變化。(見附圖1,2)
初步穩定性試驗
仿市售包裝,於室內常溫下放置(溫度8~32℃,相對濕度60%~90%),樣品於當月考察一次後,分別於1月、2月、3月、6月、12月、18月取樣按自擬的《銀杏內酯注射液質量標準(小針劑)(草案)》進行考察(其中無菌、溶血、刺激性僅在0、3和18月進行)。結果均符合規定,說明《一種銀杏內酯的藥物組合物》的銀杏內酯注射液基本穩定。
銀杏內酯注射液主要藥效學試驗資料
供試藥品
銀杏內酯注射液,銀杏內酯注射劑輔料溶液(簡稱空白溶液),燈盞花素注射液,規格:5毫克/2毫升,系雲南箇舊生物藥業有限公司產品。
1、抗血小板聚集性試驗
富血小板血漿(platelet-richplasma,PRP)和貧血小板血漿(platelet-poorplasma,PPP)的製備:取健康家兔,體重2~3千克,雌雄均用。自清醒家兔頸動脈取血收集於塑膠離心管中,以3.8%枸櫞酸鈉抗凝(血與抗凝劑體積比9:1)。室溫下900轉每分離心10分鐘,得PRP,吸出PRP於潔淨塑膠管中;剩餘血液再以3000轉每分離心10分鐘得PPP。PPP用於調零或調整PRP中的血小板數目,試驗過程中血小板數控制在5×10cell/升。
①銀杏內酯注射液在體外對血小板聚集功能的影響
將銀杏內酯注射液用空白溶液、燈盞花素注射液用生理鹽水稀釋成不同濃度的藥液備用,分別取10微升藥液或空白溶液於PRP中,37℃溫育10分鐘。按Born比濁法,即PPP調零及PRP調幅後,加入5微升的PAF(終濃度7.2納摩爾/升),在血小板聚集儀上測定血小板聚集性並記錄5分鐘內最大血小板聚集率。血小板聚集抑制率按下式計算,用直線回歸法求出藥物的半數抑制濃度(50%inhibitoryconcentration,IC50).
血小板聚集抑制率(%)=[1-(對照管聚集百分率/給藥管聚集百分率)]×100
結果顯示,銀杏內酯注射液呈濃度依賴性明顯抑制PAF誘導的血小板聚集,其IC50為9.4毫克/升,燈盞花素注射液IC50為214.8毫克/升(表1,2)。表明銀杏內酯注射液抑制PAF誘導的血小板聚集,顯著強於燈盞花素注射液。
表1.銀杏內酯注射液在體外對PAF誘導的血小板聚集功能的影響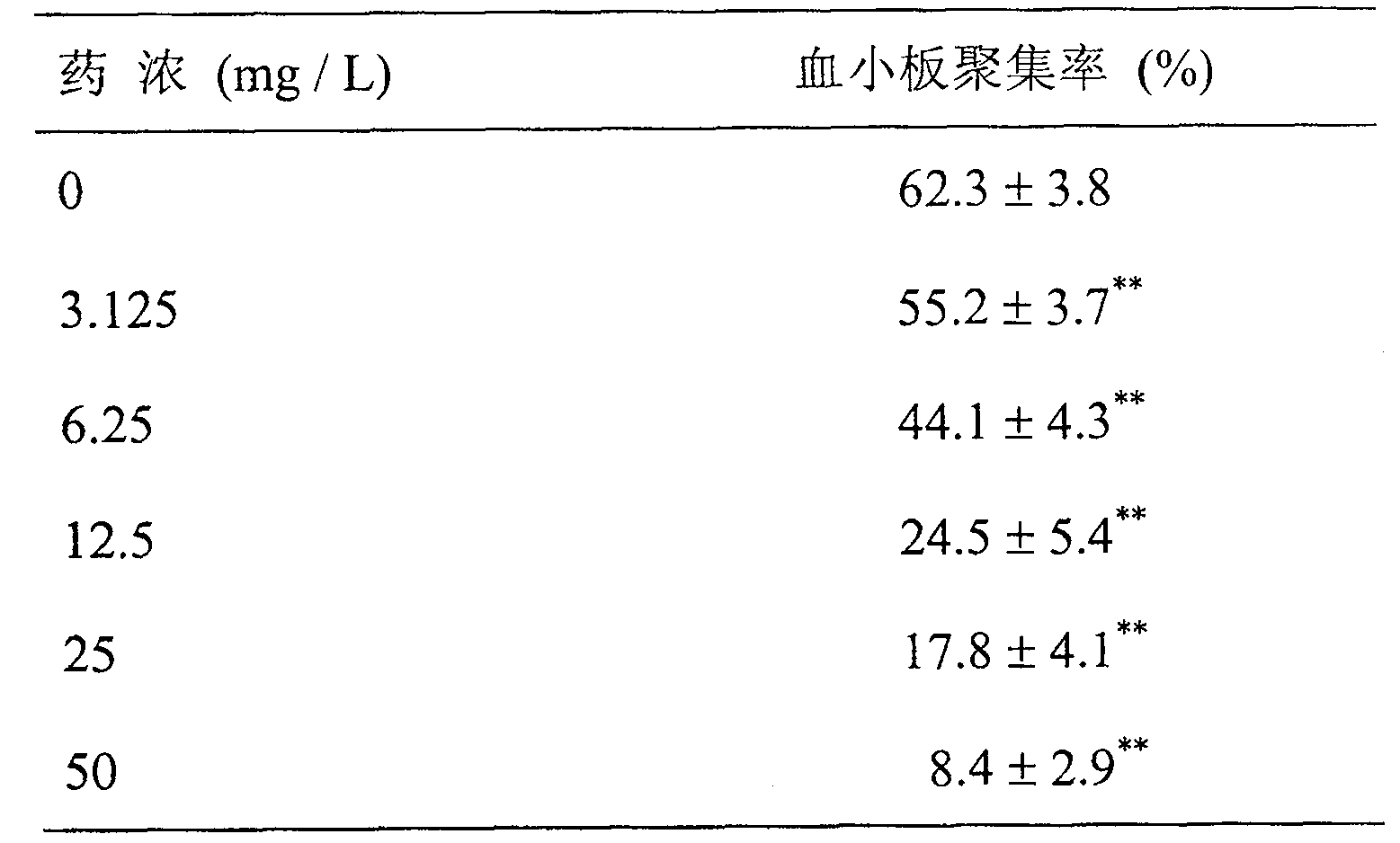

表1
n=5,x±s,P<0.01與空白溶液組比較(Studentt-檢驗)。
表2.燈盞花素注射液在體外對PAF誘導的血小板聚集功能的影響

表2
n=5,x±s,P<0.01與空白溶液組比較(Studentt-檢驗)。
2、銀杏內酯注射液在體內對血小板聚集功能的影響
健康家兔30隻,體重2.0~2.5千克,雌雄均用,隨機分成5組,每組6隻,即等體積空白溶液組、2.0、4.0、8.0毫克/千克的銀杏內酯注射液組和13.2毫克/千克的燈盞花素注射液組。上述各組份均以5.0毫升/千克體重經耳緣靜脈注射給藥。給藥前取血一次,給藥後10、30、60、90和120分鐘分別取血,同體外試驗方法製備PRP和PPP,觀察藥物靜脈注射後對PAF誘導血小板聚集功能的影響。
實驗結果表明,銀杏內酯注射液靜脈注射後,劑量為2.0毫克/千克時對PAF誘導的血小板聚集功能無明顯抑制作用,4.0毫克/千克時,於注射後30和60分鐘明顯抑制PAF引起的血小板聚集,8.0毫克/千克時,於注射後10分鐘起效,於60分鐘達最大抑制作用,抗PAF作用持續至90分鐘;13.2毫克/千克(臨床劑量的40倍)的燈盞花素注射液的作用特點與8.0毫克/千克(臨床劑量的20倍)的銀杏內酯注射液相似。注射後60分鐘,8.0毫克/千克(臨床劑量的20倍)銀杏內酯注射液的抗PAF作用強度明顯高於13.2毫克/千克(臨床劑量的40倍)燈盞花素注射液組(表3)。
表3.銀杏內酯注射液靜脈注射對PAF誘導的血小板聚集功能的影響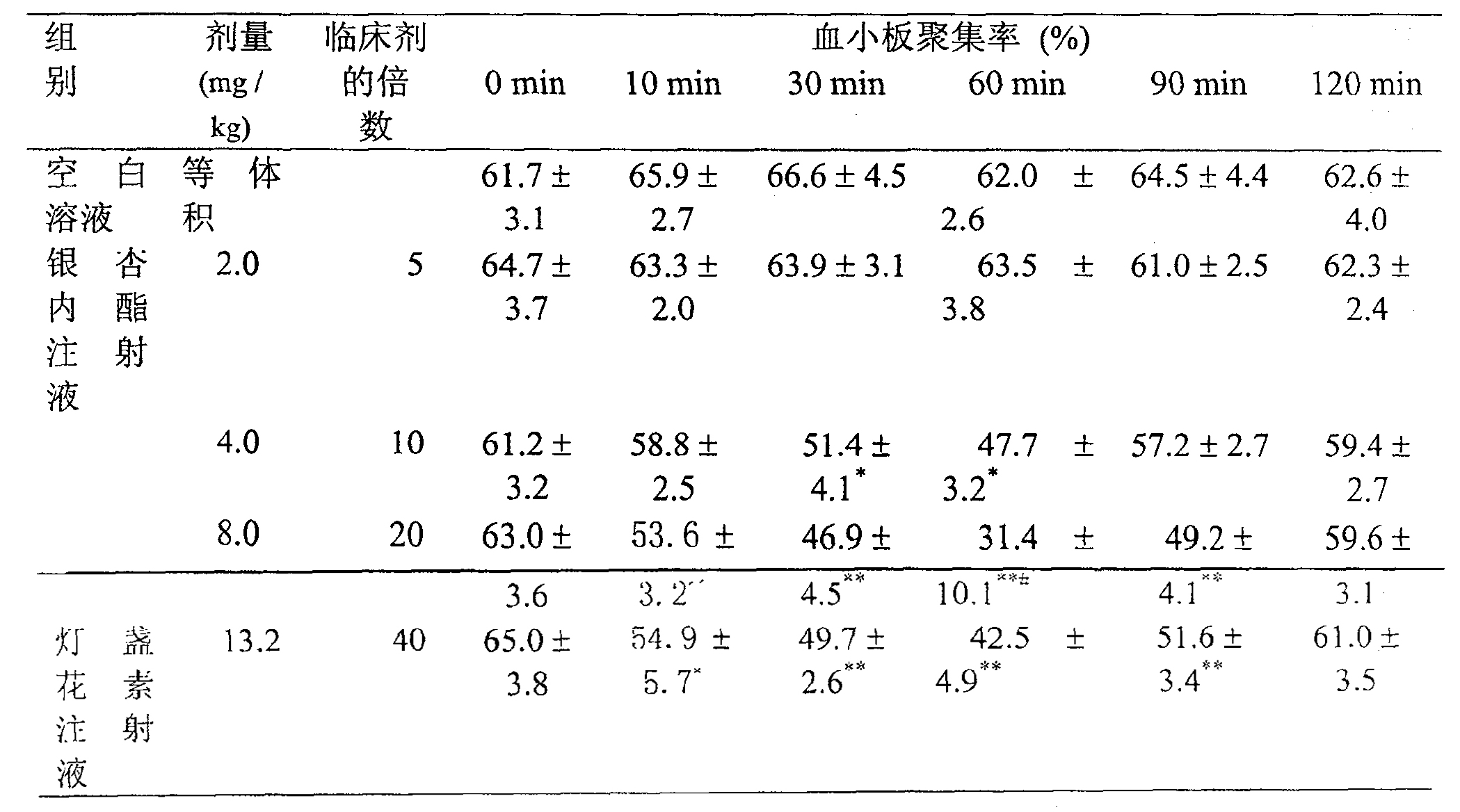

表3
n=5,x±s,P<0.05,P<0.01,與等時間點的空白溶液組或0分鐘比較,P<0.05與燈盞花素注射液比較(Studentt-檢驗)。
3、對電刺激大鼠頸動脈血栓形成的影響試驗
雄性SD大鼠50隻,體重190~230克,隨機分成5組,每組10隻,即空白溶液組(等體積)、2.0、4.0、8.0毫克/千克的銀杏內酯注射液組和13.2毫克/千克的燈盞花素注射液組。上述各組份均以0.2毫升/100克體重腹腔注射(ip),1次/天,共2次,於末次給藥30分鐘後,套用Charlton等方法並加以改良,即用30毫克/千克戊巴比妥鈉腹腔注射麻醉大鼠,分離左頸總動脈,測定正常血流量;藥物再以0.2毫升/100克體重經股靜脈注射,10分鐘後置兩根銀制電極於血管兩端,間距0.5厘米,電極及血管下襯一絕緣薄膜,通以1.5毫安直流電連續刺激7分鐘,同時用5兆赫茲點式超聲探頭,連續測量刺激部位遠心端的血流量。從刺激開始至血流量為零的時間間隔,代表血管栓塞時間(occlusiontime,OT),此為血栓形成時間。若60分鐘內血管仍開放,則以60分鐘作為記錄終點。實驗數據用Studentt-檢驗行統計學處理。
結果顯示,銀杏內酯注射液靜脈注射後,呈劑量相關性明顯延長電刺激大鼠頸動脈的血栓形成時間;13.2毫克/千克(臨床劑量的40倍)燈盞花素注射液組的血栓形成時間與8.0毫克/千克(臨床劑量的20倍)銀杏內酯注射液組的相當(表4)。
表4.銀杏內酯注射液靜脈注射對電刺激雄性大鼠頸動脈血栓形成的影響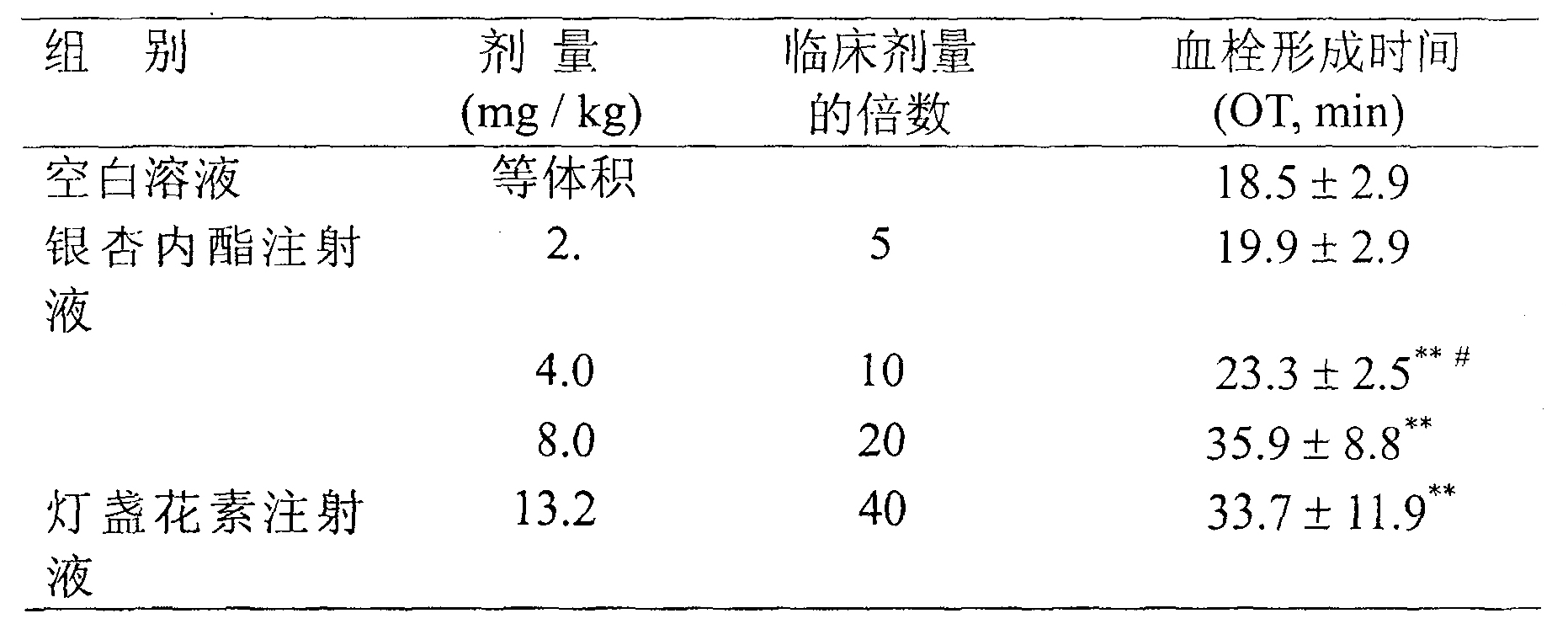

表4
n=10,x±s,P<0.01與空白溶液組比較,P<0.01與燈盞花素注射液組比較(Studentt-檢驗)。
4、銀杏內酯注射液的溶栓試驗
血栓模型的製備
雄性SD大鼠50隻,體重240~280千克,隨機分為5組,每組10隻,即等體積的空白溶液組、13.2毫克/千克燈盞花素注射液組、2.0、4.0和8.0毫克/千克的銀杏內酯注射液組。改良Charlton等方法,即用30毫克/千克的戊巴比妥鈉ip麻醉大鼠,分離大鼠左頸總動脈,置兩根銀制電極(間距0.8厘米),超聲探針置遠心端。用電刺激器以2毫安的直流連續刺激大鼠頸動脈5分鐘。用超音波雙向血流儀連續探測頸動脈血流量。以血流量降低為刺激前的50%作為血栓形成。
溶栓活性的測定
以刺激結束後至血流量降低為刺激前的50%所需的時間定為血栓形成時間。形成血栓後20分鐘,上述各組分均經股靜脈一次性注射,觀察給藥後1小時內血管再通情況;該段時間內,若血管沒有再通,則認為再通失敗。若再通,則繼續觀察血管開放狀態1小時。以≥50%或≤25%的刺激前血流量者判定為持續再通或繼後的再栓塞;再通後1小時內,每隻動物的頸動脈血流量以刺激前血流量為基線可分為≥50%,>25%至<50%,和≤25%。頸動脈血管開放程度分別為(1)持續栓塞(persistent occlusion,PO):無再通;(2)再通與再栓塞交錯出現(cyclic reflow,CR);(3)再通後持續開放(persistent patency,PP):再通後無再栓塞。
結果表明,2.0毫克/千克銀杏內酯注射液組的栓塞血管與空白溶液組相似,均無一再通,4.0、8.0毫克/千克銀杏內酯注射液組及燈盞花素注射液組的血管再通率分別為30、60和60%;4.0毫克/千克銀杏內酯注射液組的血管再栓率為66.7%,8.0毫克/千克(臨床劑量的20倍)銀杏內酯注射液組的再栓率與13.2毫克/千克(臨床劑量的40倍)燈盞花素注射液組相當,均為50%(表5)。再通後1小時內,血管開放狀態表現為,空白溶液組均持續栓塞;13.2毫克/千克(臨床劑量的40倍)的燈盞花素注射液組的血管開放狀態分值與8.0毫克/千克(臨床劑量的20倍)的銀杏內酯注射液組相當(表6)。
表5.銀杏內酯注射液對動脈血栓的溶栓作用

表5
n=10,x±s,P<0.05與空白溶液比較(Xtest)。
表6.一次性靜注銀杏內酯注射液溶栓後1小時動脈開放狀態

表6
n=10雄性大鼠。
5、銀杏內酯注射液對小鼠抗缺血、耐缺氧試驗
ICR小鼠50隻,體重18~22克,雌雄各半,隨機分成5組,每組10隻,即等體積的空白溶液組、2.0、4.0、8.0毫克/千克的銀杏內酯注射液組和13.2毫克/千克的燈盞花素注射液組。各組動物按0.1毫升/10克體重ip,1次/天,連續2天。於末次給藥後30分鐘,再分別經尾靜脈緩慢注射上述各組分,10分鐘後將小鼠逐只斷頭,立即按秒表記錄小鼠斷頭後張口喘氣停止時間作為抗腦缺血、耐缺氧指標,數據以Studentt-檢驗行組間統計學處理。
結果顯示,高、中劑量的銀杏內酯注射液及燈盞花素注射液均明顯延長正常小鼠斷頭張口喘氣時間,13.2毫克/千克(臨床劑量的40倍)的燈盞花素注射液組的喘氣時間與8.0毫克/千克(臨床劑量的20倍)銀杏內酯注射液組相當(表7)。
表7.銀杏內酯注射液靜脈注射對小鼠斷頭張口喘氣時間的影響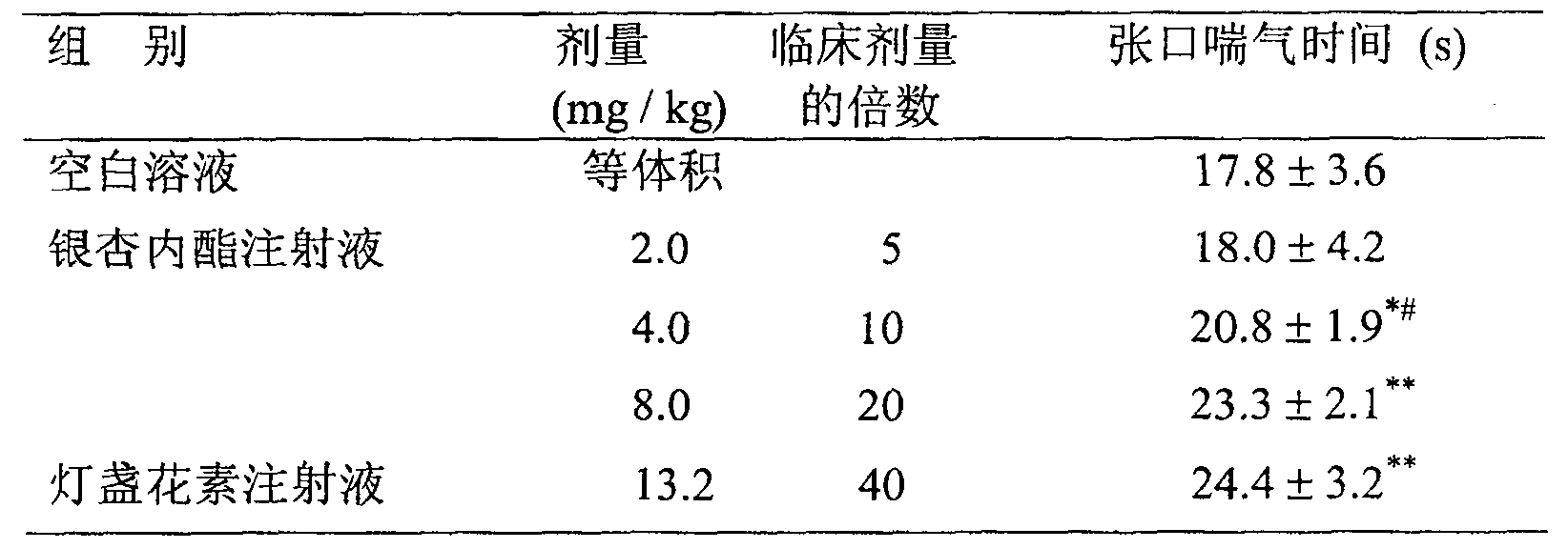

表7
n=10,x±s,P<0.05,P<0.01與空白溶液組比較,P<0.05與燈盞花素,注射液組比較(Studentt-檢驗)。
6、對沙土鼠腦缺血再灌注損傷改善試驗
模型:健康沙土鼠40隻,體重50~70克,雌雄兼用。2%戊巴比妥鈉(50毫克·千克)ip麻醉動物,頸部正中切口,分離頸總動脈,用無損傷動脈夾夾閉雙側頸總動脈10分鐘,松夾後直視血管再通(再灌注),造成腦缺血再灌注損傷模型,假手術組行同樣操作,但不夾閉頸總動脈。縫合皮膚切口,放回原條件繼續飼養5天(d)。手術過程中保持肛溫約37℃。
分組:動物隨機分為5組,每組8隻,分別為:假手術組、缺血模型組、銀杏內酯注射液中、高劑量組和燈盞花素注射液陽性對照組。造型前2天,分別ip溶媒(假手術組和缺血模型組)、銀杏內酯注射液4.0、8.0毫克/千克和燈盞花素注射液13.2毫克/千克,每天1次,夾閉動脈前5分鐘股靜脈注射各受試樣品1次,再灌注期間ip1次/天,共5次。
檢測指標
(1).記錄腦電圖(EEG):參照文獻(Sun F,Liu TP.Tetrandrine vs nicardipine in cerebral ischemia-reperfusion damages in gerbils.Acta Pharmacol Sin.1995,16(2):145)用單個針形電極插入沙土鼠前腦皮下,參比電極置於枕部皮下,另一端接日本光電VC-11型記憶示波器,記錄缺血前、靜脈注射5分鐘、缺血10分鐘、再灌注10、30和60分鐘的EEG,並將腦電信號輸入日本光電QC-111J型疊加直方分析儀,記錄其直方圖,以x軸的μv數作為EEG電位幅度,以缺血前EEG為100%,按下式計算EEG電位幅度%。
EEG電位幅度(%)=缺血或再灌注後幅度÷缺血前幅度×100
(2).大腦皮層組織Ca、Na、水含量測定:腦缺血10分鐘再灌注5天后,脫頸處死動物,參照Young法(Young W,Rappaport H,Chalif DJ,Flamm ES.Regional brain sodium,potassium and water changes in the rat middle cerebral artery occlusion of ischemia.Stroke 1987;18:751)取右側顳頂葉皮質,用濾紙吸去血跡,置預先稱重的坩鍋中,精確稱取濕重,後置100℃烤箱烘烤5小時致恆重,再稱取乾重,按下式計算組織的含水量:
水含量(%)=(濕重-乾重)÷濕重×100
之後經消化、灰化、稀釋處理,用原子吸收分光光度計測定大腦皮層Ca、Na含量(Bradbury,MWB,Kleeman,CR,Bagdoyan,H,BerberianA.The calcium and magnesium content of skeletal muscle,brain,and cerebrospinal fluidas deter分鐘ed by atomic absorption flame photometry.JLabClinMed1968;71:884)。
實驗結果表明,夾閉雙側頸總動脈後,缺血再灌注組動物EEG電位幅度立即降低,持續低平,與假手術對照組相比差異有顯著性(P<0.01),再灌注後電位幅度恢復緩慢,60分鐘時,僅恢復至缺血前的40.5%。給予銀杏內酯注射液4.0、8.0毫克/千克燈盞花素注射液13.2毫克/千克後,均能促進EEG電位幅度的恢復,再灌注60分鐘時分別恢復至缺血前的49.5%,58.1%和70.8%,明顯高於缺血再灌注組,P<0.05(表8)。
表8.銀杏內酯注射液注射給藥對沙土鼠腦缺血再灌損傷EEG的影響

表8
x±s,n=8.P<0.05,P<0.01,與缺血再灌注組比較(Studentt-檢驗)。
缺血10分鐘再灌注5天后,缺血再灌注組動物大腦皮層水、鈉和鈣含量明顯高於假手術對照組(P<0.01)。銀杏內酯注射液8.0毫克/千克(臨床劑量的20倍)能減輕缺血再灌注損傷引起的腦水腫,與缺血再灌注組比較,差異有顯著性;對鈣鈉累積具有減少趨勢,但未達到統計學顯著意義。燈盞花素注射液13.2毫克/千克(臨床劑量的40倍)對腦水腫影響不明顯,但能減輕鈣鈉累積(表9)。
表9.銀杏內酯注射給藥對沙土鼠腦缺血10分鐘再灌5天

表9
x±s,n=8.P<0.05,P<0.01,與缺血再灌注組比較(Studentt-檢驗)。
7、對大鼠局灶性腦缺血改善試驗
雄性SD大鼠80隻,體重310±17克,隨機分為6組,分別為:假手術組、缺血模型組(均給予等體積溶媒)、銀杏內酯注射液高劑量組(8.0毫克/千克)、中劑量組(4.0毫克/千克)、低劑量組(2.0毫克/千克)和燈盞花素注射液陽性對照組(13.2毫克/千克)。於實驗前2天每天ip.1次,第3天於缺血前5分鐘給藥1次。參照文獻方法(徐叔雲,卞如濂,陳修.藥理學實驗方法學,第三版,人民衛生出版社,2002,pp.1066),採用頸內動脈線栓法製備大鼠大腦中動脈閉塞(MCAO)模型。用10%水合氯醛(300毫克/千克)ip麻醉動物,將矽化的0.28毫米直徑尼龍線經頸總動脈插入大腦前動脈(以頸總動脈分叉處為標記,約為17毫米)造成局灶性腦缺血模型。假手術組行同樣操作,但不閉塞大腦中動脈。手術過程中保持肛溫約37℃。術後24小時對動物出現的神經症狀進行行為評分,標準如下:
0 | 無異常 |
1 | 豎毛,輕度運動低下 |
2 | 行動不協調,屈曲姿勢,旋轉運動 |
3 | 偏癱,不能站立或行走 |
4 | 痙攣,昏睡 |
5 | 死亡 |
MCAO後24小時,脫頸處死動物,取出全腦,做冠狀切片,用1%TTC溶液37℃避光孵育25分鐘,分離蒼白區(梗塞區)和非蒼白區(正常區),稱重,按下式計算百分比:
梗塞百分比(%)=梗塞區重量÷(梗塞區重量+正常區重量)×100
結果表明,ip銀杏內酯注射液4.0毫克/千克(臨床劑量的10倍)和8.0毫克/千克(臨床劑量的20倍)和燈盞花素注射液13.2毫克/千克(臨床劑量的40倍)均能明顯縮小MCAO大鼠的梗塞範圍,試驗各組的腦切片見圖1,與缺血模型組比較,差異有顯著性(P<0.05,0.01);銀杏內酯注射液和燈盞花素注射液均能降低MCAO大鼠的腦卒中評分和動物死亡率(表10)。
表10.銀杏內酯注射液注射給藥對大鼠MCAO24小時神經缺陷評分和梗塞百分比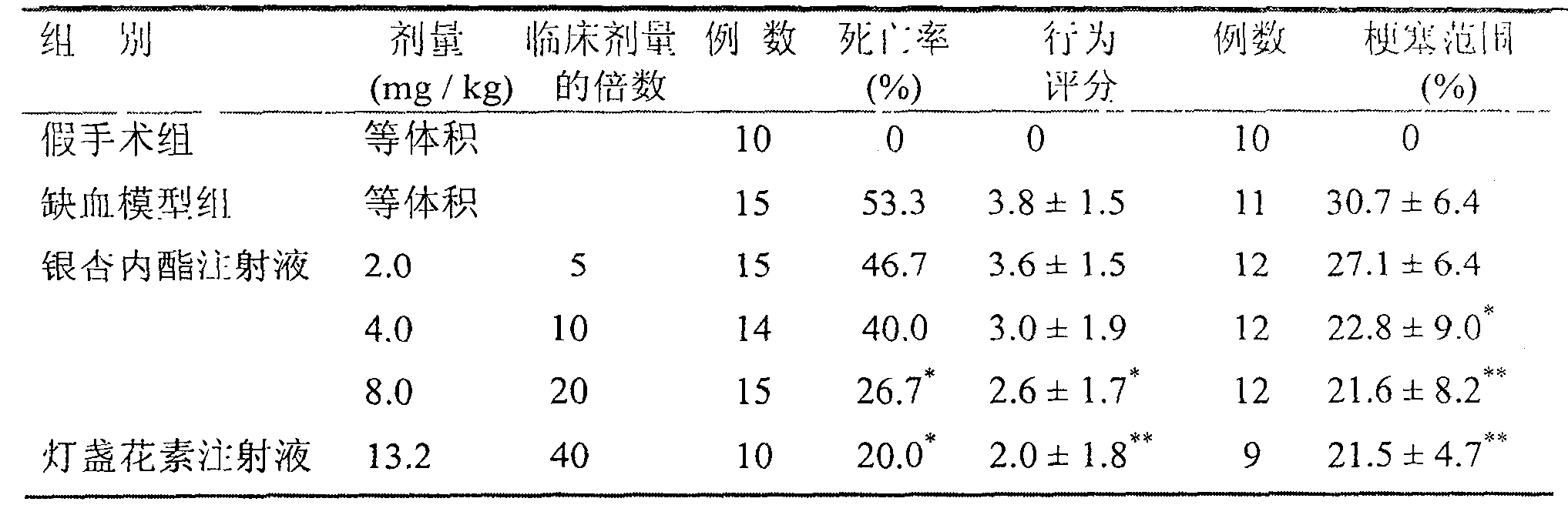

表10
x±s.行為評分和梗塞百分比採用Studentt-檢驗:P<0.05,P<0.01,與缺血模型組比較;死亡率採用X-檢驗:P<0.05,與缺血模型組比較。
8、增加小鼠腹腔毛細血管通透性試驗
小鼠隨機分為5組,每組10隻,即空白溶液組、2.0、4.0、8.0毫克/千克銀杏內酯組和13.2毫克/千克的燈盞花素注射液組。各組動物均先以0.1毫升/10克體重腹腔注射,1次/天,共2次,於末次給藥後30分鐘,再繼以尾靜脈注射,10分鐘後,0.5%伊文思藍以0.2毫升/只尾靜脈注射並及時腹腔注射0.7%醋酸0.2毫升/只,15分鐘後處死動物,腹腔注射生理鹽水5毫升,輕揉後抽取腹腔液,離心,上清液於590納米處測定其OD值,數據行組間t檢驗.
結果表明,高、中劑量的銀杏內酯注射液和燈盞花素注射液均能促進H刺激引起小鼠腹腔毛細血管通透性的增高(表11)。
表11.銀杏內酯注射液靜脈注射對小鼠腹腔毛細血管通透性的影響組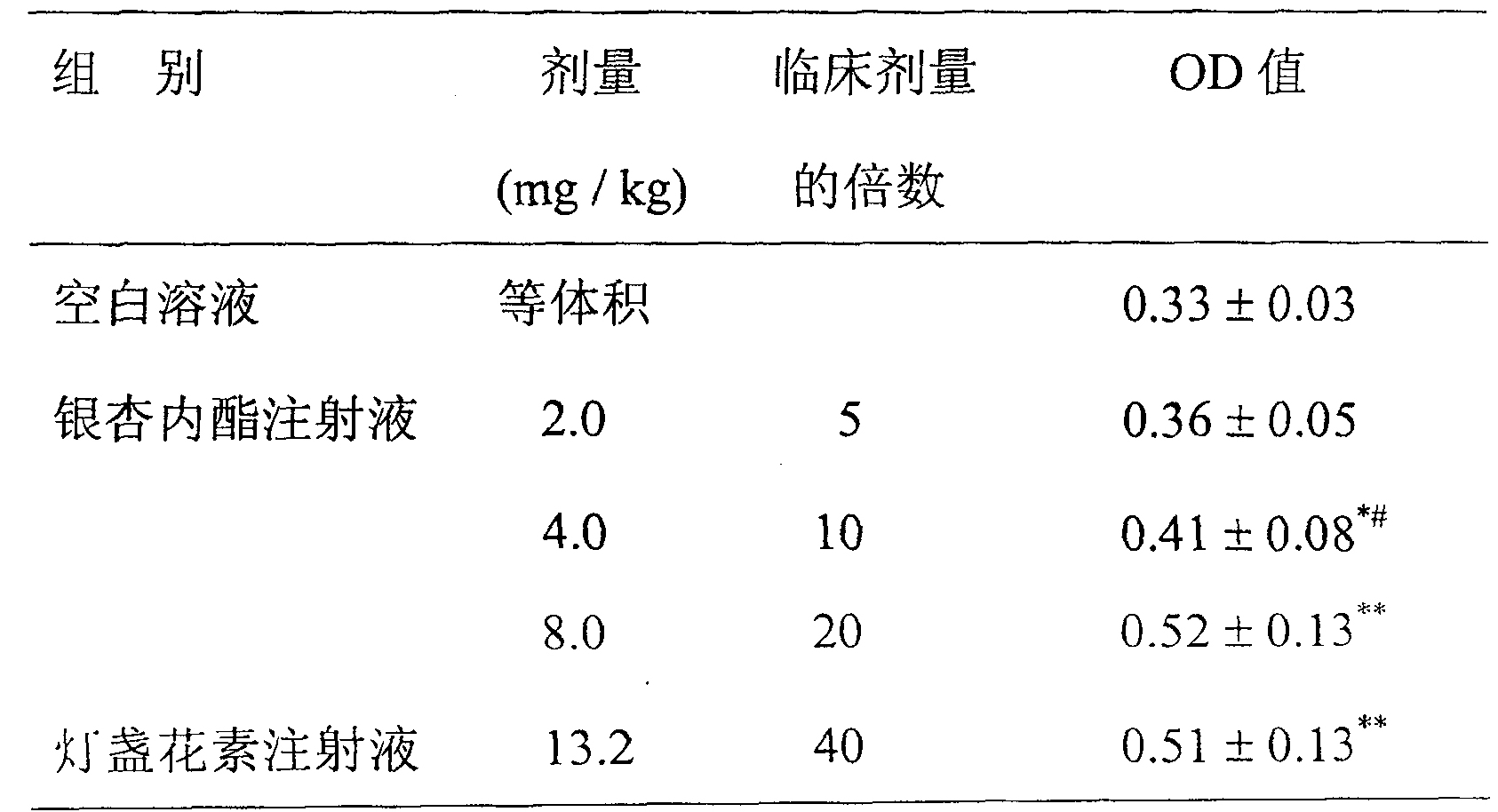

表11
n=10,x±s,P<0.05,P<0.01與空白溶液組比較,P<0.05與燈盞花素注射液組比較(Studentt-檢驗。
1.8對原代培養小鼠皮層神經細胞的保護作用
小鼠皮層神經細胞的原代培養:取孕14-17天齡ICR胎鼠大腦皮層,D-Hanks液洗2次後,剪成糜狀,加入0.125%胰酶消化10分鐘,用含10%小牛血清的DMEM培養液終止消化,用吸管輕輕吹打,使細胞分散,200目金屬網篩過濾,細胞濾液以800r.分鐘離心5分鐘,棄上清液,用DMEM培養液(含10%小牛血清,青黴素G100U/毫升,鏈黴素100U/毫升)重新懸浮細胞,將細胞濃度調整為1.5×10/毫升,接種於多聚賴氨酸包被過的24孔和96孔板中,接種體積分別為400微升和100微升。於37℃5%CO2培養箱中培養。每周換液2次,3~5天后,加入阿糖胞苷10微米ol/升培養24小時,以抑制非神經細胞增殖。
谷氨酸對培養的神經細胞的損傷:於培養第8天加入受試樣品(用DMSO助溶)或空白溶媒,24小時後吸去培養液,用DMEM洗1次,加谷氨酸(終濃度500微摩爾/升)處理1小時,吸去含谷氨酸的培養液,用DMEM洗1次,再加入含小牛血清的DMEM繼續培養24小時。
MTT微量自動比色法:谷氨酸處理後24小時,在96孔板中加入MTT(終濃度0.5毫克/毫升),繼續培養4小時,再加入三聯液溶解藍紫色結晶(Formazan),次日用EL340型酶標儀測定570納米的吸收度,按公式計算細胞的相對存活率(相對存活率%=加樣孔OD值或Glu損傷孔OD值÷空白對照孔OD值×100),結果進行t-檢驗。
LDH活性測定:谷氨酸處理後24小時,測定24孔板培養液中即細胞外液的LDH活性,之後將細胞凍存於-30℃冰櫃,以破壞細胞,次日再次測定培養液中總的LDH活性,兩次差值的大小反應細胞的損傷程度,差值越小損傷越重,說明LDH泄漏到細胞外液越多,結果進行t-檢驗。
在缺血性腦損傷的機制研究中,興奮性胺基酸在缺血性腦損傷病理過程中發揮著重要作用,研究表明谷氨酸與原代培養的大腦皮層神經細胞接觸一定時間後將引起神經細胞的死亡,LDH泄漏到細胞外液中。本實驗結果表明:銀杏內酯注射液和燈盞花素注射液均能減少谷氨酸引起的神經細胞LDH的泄漏,兩者相比無顯著性差異,提示對谷氨酸所致細胞膜損傷有一定的保護作用;但對提高谷氨酸損傷後細胞的相對存活率影響不明顯(表12)。
表12.銀杏內酯注射液對谷氨酸誘導小鼠原代培養皮層神經原損傷的影響

表12
x±s,P>0.01與0濃度比較(Studentt-檢驗);P>0.05與燈盞花素注射液比較(Studentt-檢驗)。
改善效果
綜上所述,銀杏內酯注射液具有顯著改善腦組織的缺血和缺氧作用,銀杏內酯注射液具有明顯的通脈、活血化瘀及促進血瘀性物質的吸收之功效。大部分藥效學試驗項目中,銀杏內酯注射液8.0毫克/千克(臨床劑量的20倍)作用與燈盞花素注射液13.2毫克/千克(臨床劑量的40倍)相當,但前者選擇性強力拮抗PAF,抗腦水腫作用較強,後者減輕鈣、鈉累積作用較明顯。本試驗為銀杏內酯注射液作為防治中風和外周血栓性疾病提供了較為可靠的依據。
附圖說明
圖1銀杏內酯提取物的含量測定HPLC圖,其中峰1是銀杏內酯C、峰2是白果內酯、峰3是銀杏內酯A、峰4是銀杏內酯B。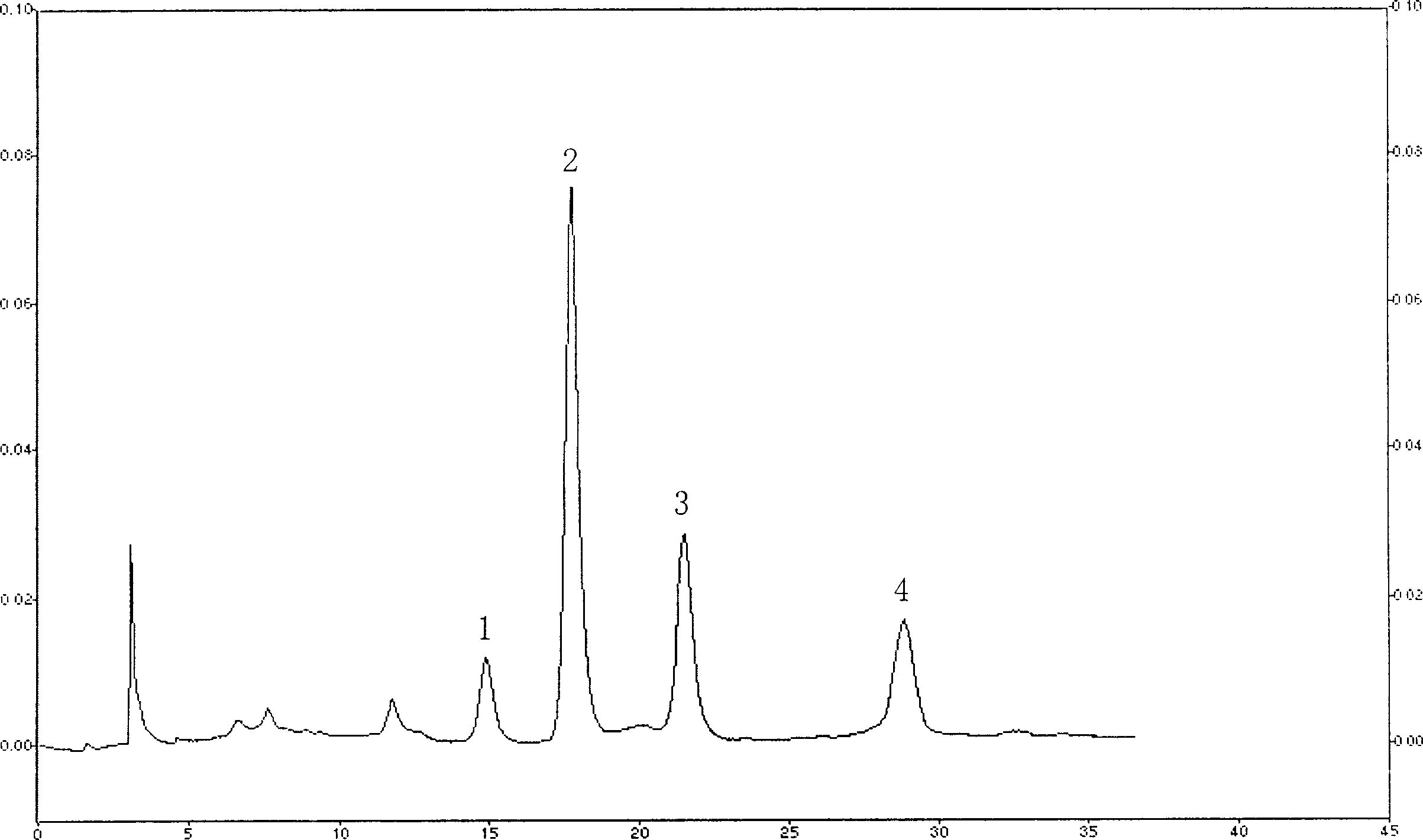

圖1
圖2銀杏內酯注射液的含量測定HPLC圖,其中峰1是銀杏內酯C、峰2是白果內酯、峰3是銀杏內酯A、峰4是銀杏內酯B。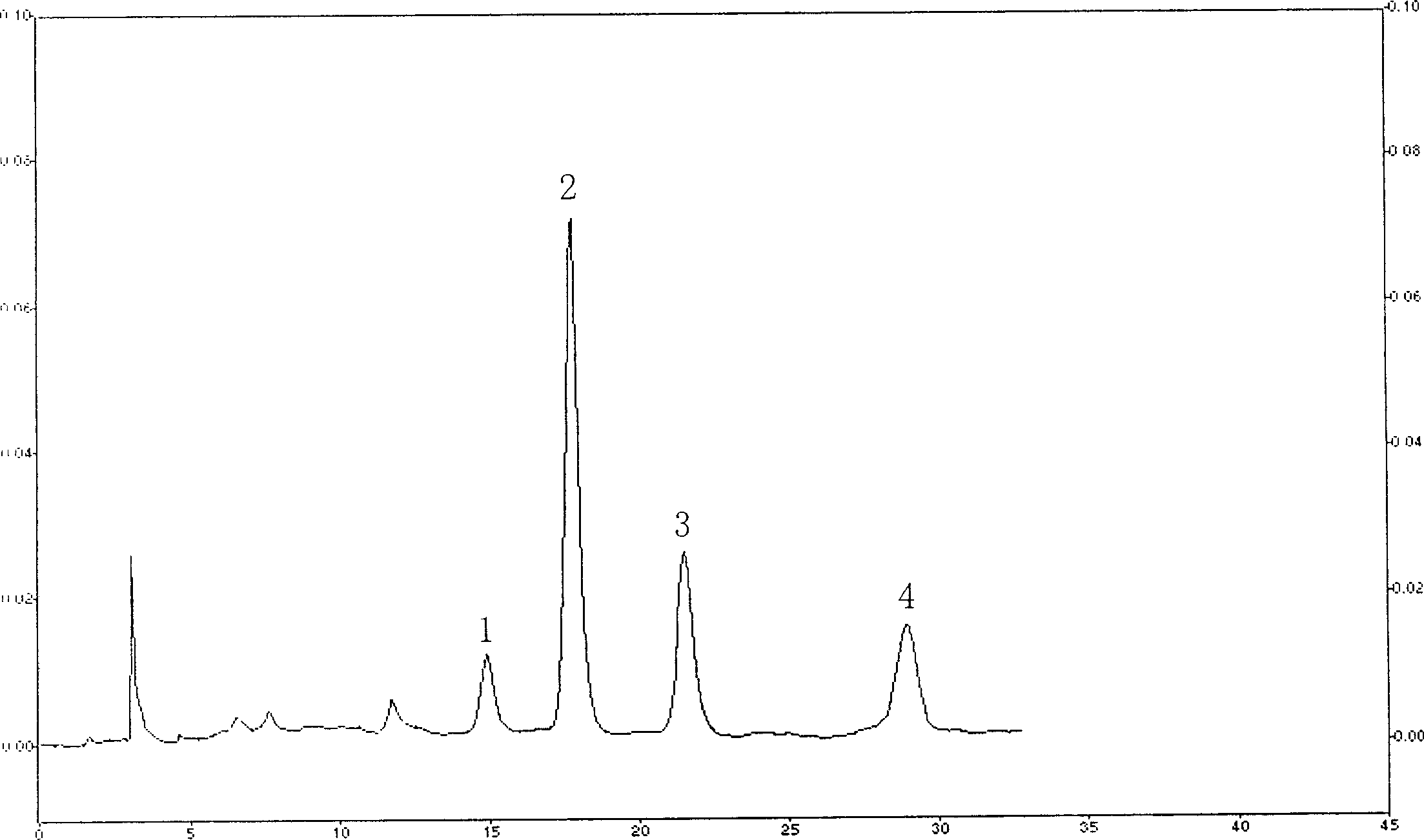

圖2
技術領域
《一種銀杏內酯的藥物組合物》涉及一種含銀杏內酯的製劑,特別是銀杏內酯注射液,同時還提供該注射液的製備工藝,屬於藥物組合物領域。
權利要求
1.一種銀杏內酯的藥物組合物,其特徵在於,該藥物組合物中含有白果內酯。
2.根據權利要求1所述的一種銀杏內酯的藥物組合物,其特徵在於,該藥物組合物中銀杏內酯的重量比例為:銀杏內酯B10%-90%:白果內酯10%-90%。
3.根據權利要求1所述的一種銀杏內酯的藥物組合物,其特徵在於,該藥物組合物中銀杏內酯的重量比例銀杏內酯A:銀杏內酯B:銀杏內酯C:白果內酯=10%-45%:5%-40%:3%-35%:10%-70%。
4.根據權利要求1所述的一種銀杏內酯的藥物組合物,其特徵在於,該藥物組合物中銀杏內酯的重量比例銀杏內酯A:銀杏內酯B:銀杏內酯C:白果內酯=15%-40%:7%-30%:5%-20%:20%-60%。
5.根據權利要求1所述的一種銀杏內酯的藥物組合物,其特徵在於,銀杏內酯A、銀杏內酯B、銀杏內酯C、白果內酯重量之和占提取物總重80%以上。
6.根據權利要求1所述的一種銀杏內酯的藥物組合物,其特徵在於,它的劑型是適合臨床套用的注射劑、乳劑、丸劑、滴丸、片劑、緩釋片、膠囊、軟膠囊、顆粒劑、散劑、錠劑、煎膏劑、口服液合劑、糖漿劑等藥劑學上可以接受的劑型中的任何一種藥物劑型;其中注射劑包括輸液、凍乾粉針,片劑包括分散片、口崩片。
7.根據權利要求1-6中任一項所述的一種銀杏內酯的藥物組合物,其特徵在於,該藥物組合物在防治中風和外周血栓形成疾病上的用途。
實施方式
實施例一
處方(以1000劑量單位計):銀杏內酯10克、甘油1000毫升、乙醇2500毫升、注射用水加至5000毫升、製成1000支。
製備方法:取處方量約80%的注射用水,處方全量的甘油和乙醇,置配液缸中,加入處方量的銀杏內酯,攪拌溶解後,加注射用水至全量,用10%檸檬酸溶液調節pH,攪勻,半成品檢驗合格後,用0.65微米和0.45微米複合耐醇微孔濾膜作濾材的微膜過濾系統過濾澄明,灌封於5毫升玻瓶中,於100℃滅菌20分鐘,冷卻,燈檢,貼標,即得。
含量測定用高效液相色譜一蒸發光散射檢測法(HPLC-ELSD)直接測定銀杏葉中銀杏萜類內酯A、B、C及白果內酯的含量。方法:10%甲醇製作供試品溶液,經C18色譜柱,以甲醇-水為流動相。梯度洗脫,以蒸發光檢測器檢測
結果:銀杏萜類內酯A、B、C及白果內酯的含量分別為1毫克,0.5毫克,1.5毫克,7毫克。
實施例二
處方(以1000劑量單位計):銀杏內酯10克、甘油400毫升、乙醇800毫升、注射用水加至2000毫升、製成1000支。
製備方法:取處方量約80%的注射用水,處方全量的甘油和乙醇,置配液缸中,加入處方量的銀杏內酯,攪拌溶解後,加注射用水至全量,用10%醋酸溶液調節pH,攪勻,半成品檢驗合格後,用0.65微米和0.45微米複合耐醇微孔濾膜作濾材的微膜過濾系統過濾澄明,灌封於2毫升玻瓶中,於100℃滅菌20分鐘,冷卻,燈檢,貼標,即得。
含量測定用高效液相色譜一蒸發光散射檢測法(HPLC-ELSD)直接測定銀杏葉中銀杏萜類內酯A、B、C及白果內酯的含量。方法:10%甲醇製作供試品溶液,經C18色譜柱,以甲醇-水為流動相。梯度洗脫,以蒸發光檢測器檢測
結果:銀杏萜類內酯A、B、C及白果內酯的含量分別為1.8毫克,0.7毫克,3.5毫克,4毫克。
實施例三
處方(以1000劑量單位計):銀杏內酯10克、甘油400毫升、乙醇800毫升、注射用水加至2000毫升、製成1000支。
製備方法:取處方量約80%的注射用水,處方全量的甘油和乙醇,置配液缸中,加入處方量的銀杏內酯,攪拌溶解後,加注射用水至全量,用10%檸檬酸溶液調節pH,攪勻,半成品檢驗合格後,用0.65微米和0.45微米複合耐醇微孔濾膜作濾材的微膜過濾系統過濾澄明,灌封於2毫升玻瓶中,於100℃滅菌20分鐘,冷卻,燈檢,貼標,即得。
含量測定用高效液相色譜一蒸發光散射檢測法(HPLC-ELSD)直接測定銀杏葉中銀杏萜類內酯A、B、C及白果內酯的含量。方法:10%甲醇製作供試品溶液,經C18色譜柱,以甲醇一水為流動相。梯度洗脫,以蒸發光檢測器檢測
結果:銀杏萜類內酯A、B、C及白果內酯的含量分別為1毫克,0.7毫克,0.3毫克,6毫克。
實施例四
處方(以1000劑量單位計):銀杏內酯10克、甘油400毫升、乙醇800毫升、注射用水加至2000毫升、製成1000支。
製備方法:取處方量約80%的注射用水,處方全量的甘油和乙醇,置配液缸中,加入處方量的銀杏內酯,攪拌溶解後,加注射用水至全量,用10%檸檬酸溶液調節pH,攪勻,半成品檢驗合格後,用0.65微米和0.45微米複合耐醇微孔濾膜作濾材的微膜過濾系統過濾澄明,灌封於2毫升玻瓶中,於100℃滅菌20分鐘,冷卻,燈檢,貼標,即得。
含量測定用高效液相色譜一蒸發光散射檢測法(HPLC-ELSD)直接測定銀杏葉中銀杏萜類內酯A、B、C及白果內酯的含量。方法:10%甲醇製作供試品溶液,經C18色譜柱,以甲醇一水為流動相。梯度洗脫,以蒸發光檢測器檢測
結果:銀杏萜類內酯A、B、C及白果內酯的含量分別為4毫克,4毫克,1毫克,1毫克。
實施例五
處方(以1000劑量單位計):銀杏內酯10克、甘油400毫升、乙醇800毫升、注射用水加至2000毫升、製成1000支。
製備方法:取處方量約80%的注射用水,處方全量的甘油和乙醇,置配液缸中,加入處方量的銀杏內酯,攪拌溶解後,加注射用水至全量,用10%檸檬酸溶液調節pH,攪勻,半成品檢驗合格後,用0.65微米和0.45微米複合耐醇微孔濾膜作濾材的微膜過濾系統過濾澄明,灌封於2毫升玻瓶中,於100℃滅菌20分鐘,冷卻,燈檢,貼標,即得。
含量測定用高效液相色譜一蒸發光散射檢測法(HPLC-ELSD)直接測定銀杏葉中銀杏萜類內酯A、B、C及白果內酯的含量。方法:10%甲醇製作供試品溶液,經C18色譜柱,以甲醇一水為流動相。梯度洗脫,以蒸發光檢測器檢測。
結果:每瓶銀杏萜類內酯A、B、C及白果內酯的含量分別為4.5毫克,3.5毫克,1毫克,1毫克。
實施例六
處方(以1000劑量單位計):銀杏內酯10克、甘油400毫升、乙醇800毫升、注射用水加至2000毫升、製成1000支。
製備方法:取處方量約80%的注射用水,處方全量的甘油和乙醇,置配液缸中,加入處方量的銀杏內酯,攪拌溶解後,加注射用水至全量,用10%醋酸溶液調節pH,攪勻,半成品檢驗合格後,用0.65微米和0.45微米複合耐醇微孔濾膜作濾材的微膜過濾系統過濾澄明,灌封於2毫升玻瓶中,於100℃滅菌20分鐘,冷卻,燈檢,貼標,即得。
含量測定用高效液相色譜一蒸發光散射檢測法(HPLC-ELSD)直接測定銀杏葉中銀杏萜類內酯A、B、C及白果內酯的含量。方法:10%甲醇製作供試品溶液,經C18色譜柱,以甲醇-水為流動相。梯度洗脫,以蒸發光檢測器檢測。
結果:每瓶銀杏萜類內酯A、B、C及白果內酯的含量分別為2.6毫克,1.8毫克,2毫克,3.6毫克。
實施例七
處方(以1000劑量單位計):銀杏內酯10克、甘油400毫升、乙醇800毫升、注射用水加至2000毫升、製成1000支。
製備方法:取處方量約80%的注射用水,處方全量的甘油和乙醇,置配液缸中,加入處方量的銀杏內酯,攪拌溶解後,加注射用水至全量,用10%檸檬酸溶液調節pH,攪勻,半成品檢驗合格後,用0.65μm和0.45微米複合耐醇微孔濾膜作濾材的微膜過濾系統過濾澄明,灌封於2毫升玻瓶中,於100℃滅菌20分鐘,冷卻,燈檢,貼標,即得。
含量測定用高效液相色譜---蒸發光散射檢測法(HPLC-ELSD)直接測定銀杏葉中銀杏萜類內酯A、B、C及白果內酯的含量。方法:10%甲醇製作供試品溶液,經C18色譜柱,以甲醇-水為流動相。梯度洗脫,以蒸發光檢測器檢測。
結果:每瓶銀杏萜類內酯A、B、C及白果內酯的含量分別為0.1毫克,8.8毫克,0.1毫克,1毫克。
實施例八
處方(以1000劑量單位計):銀杏內酯10克、澱粉100克、二氧化矽10克、製成1000粒。
製備方法:取處方量主藥和輔料混勻,裝2號膠囊。
含量測定用高效液相色譜---蒸發光散射檢測法(HPLC-ELSD)直接測定銀杏葉中銀杏萜類內酯A、B、C及白果內酯的含量。方法:10%甲醇製作供試品溶液,經C18色譜柱,以甲醇-水為流動相。梯度洗脫,以蒸發光檢測器檢測。
結果:每粒膠囊銀杏萜類內酯A、B、C及白果內酯的含量分別為1.5毫克,3毫克,2毫克,3.5毫克。
榮譽表彰
2016年12月7日,《一種銀杏內酯的藥物組合物》獲得第十八屆中國專利優秀獎。

