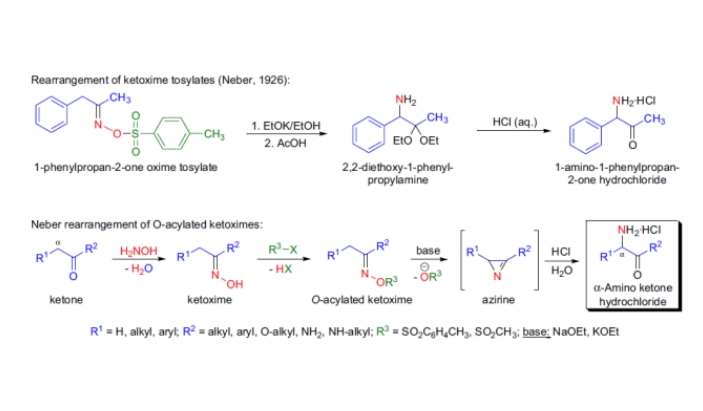
1926年,在貝克曼重排反應的研究期間,P.W. Neber和A. Friedolsheim發表報導:甲苯磺酸酮肟在乙醇鉀,乙酸和鹽酸的作用下得到氨基酮的鹽酸鹽。在鹼誘導下由o-醯化酮肟重排生成相應的α-氨基酮的反應稱為Neber重排。此反應成為以氨基酮為前體的雜環化合物的合成的一個重要合成工具。
基本介紹
- 中文名:Neber重排
- 發現時間:1926年
- 發現人:P.W. Neber和A. Friedolsheim
- 主要套用:雜環化合物的合成
反應機理,反應特點,反應舉例,
反應機理
首先O-醯基酮肟在其α位去質子化得到相應的烯醇,烯醇可以通過兩條路徑進行反應:1、共振陰離子路徑,離去基團直接分子被取代生成孤立的2H-吖丙啶;2、氮賓路徑,此路徑通過氮賓的插入得到相同的2H-吖丙啶中間體,第二條路徑還沒有通過實驗證偽。
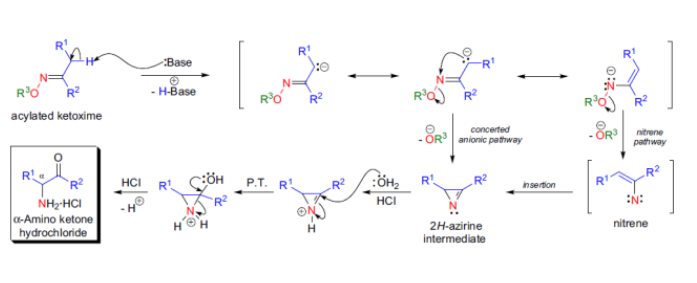 反應機理
反應機理反應特點
1、環型酮和非環型酮都可作為醯化酮肟的底物;2、反應中的肟可以有酮和羥胺在酸性條件下製得;3、o-醯化酮肟可以由醯氯和酸酐在弱鹼性條件下(如吡啶)製得;4、重排反應通常在等摩爾量的醇鹼的醇溶液中進行;5、當在α及α’位的亞甲基均能發生反應的時候,氨基定位在親電子能力更強的碳上;6、此重排反應沒有立體定向選擇性,反應底物的立體化學(順或反)都不影響反應的進行,這與貝克曼重排的反式重排截然不同;7、生成的氨基酮容易發生二聚,因此作為保護產物通常以鹽酸鹽和氨基縮酮的形式製得(氨基縮酮可以由2H-吖丙啶中間體在酸性條件下的醇溶液中得到)。
Neber重排也有一些局限性:1、O-醯化醛肟不能在鹼性條件下重排得到相應的α-氨基醛,而是發生E2消除得到相應的腈或異腈;2、絕大多數Neber重排反應的底物必須在α位有亞甲基,另外一些只含有一個α氫的化合物在鹼性條件下也能發生重排:1)氯化二甲基腙;2)N,N-二氯-仲烷基胺;3)N-氯代亞胺;4)N-氯代亞胺酸酯。
反應舉例
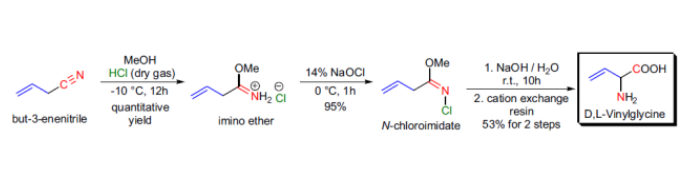 反應舉例
反應舉例