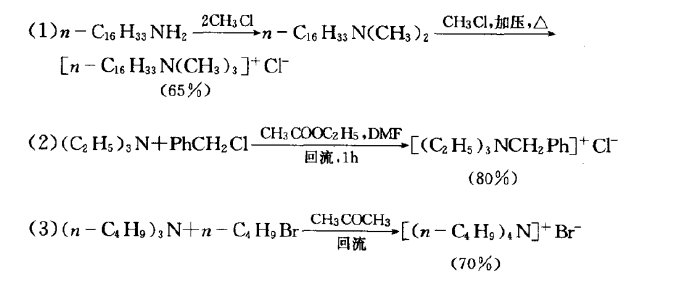
叔胺與鹵代烴作用生成季銨鹽的反應,稱為Menschutkin反應。
Menschutkin反應是研究得較多的親核取代反應之一,對溶劑的動力學效應也進行了廣泛和深入的研究,並獲得了巨大的成功。
基本介紹
- 中文名:Menschutkin反應
- 底物:叔胺與鹵代烴
- 產物:季銨鹽
- 屬於:親核取代反應
- 領域:有機合成
反應機理,決定速率的因素,離去基團的鹼性,親核試劑的親核性,溶劑,空間效應,反應舉例,
反應機理
季銨鹽的生成是按照SN2機理進行的:
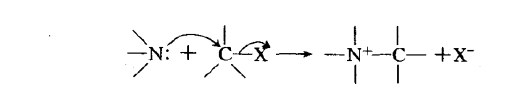
本反應是Hofmann徹底甲基化反應的組成部分。
雙分子親核取代反應反應(SN2)是親核取代反應的一類,其中S代表取代(Substitution),N代表親核(Nucleophilic),2代表反應的決速步涉及兩種分子。與SN1反應相對應,SN2反應中,親核試劑帶著一對孤對電子進攻具親電性的缺電子中心原子,形成過渡態的同時,離去基團離去。反應中不生成碳正離子,速率控制步驟是上述的協同步驟,反應速率與兩種物質的濃度成正比,因此稱為雙分子親核取代反應。無機化學中,常稱雙分子親核取代反應類型的反應機理為“交換機理”。
徹底甲基化反應(Hofmann elimination),指的是季銨鹼與碘化鉀、氫氧化銀反應,從含氫較多的β-碳原子上消除氫,得到的主要產物是雙鍵碳上含取代基比較少的烯烴,這一消除方式與鹵代烴的消除方式相反。
不對稱胺反應時,反應由動力學控制,較少烷基取代的β-碳上的氫由於酸性較強,位阻較小,因此優先被消除,產物主要是不穩定的取代較少的烯烴。這個規則與查依采夫規則相反,稱為霍夫曼規則(Hofmann規則)。β-碳上連有苯基、乙烯基、羰基等取代基時,由於共軛和吸電子效應,未取代的β-碳上氫的酸性較弱,因此反應不符合Hofmann規則。連有強吸電子基團的化合物容易按Hofmann規則發生E2消除。
霍夫曼消除可用於合成用其他方法難以合成的烯烴。由於一級、二級和三級胺引入的甲基數目不一樣,故也可通過引入的甲基數目,來判斷反應物是哪一級的胺。
決定速率的因素
離去基團的鹼性
離去基團的鹼性越強,其離去能力越弱,反之亦然。離子的鹼性隨著所在周期的增加而降低。對於鹵素離子而言,碘離子的鹼性最弱,因此碘離子是一個很好的離去基團;氟離子則相反,氟代烴也因此很難發生SN2反應。鹼性 F-> Cl-> Br-> I-,離去能力與上述順序相反。
親核試劑的親核性
親核性需要與上面的鹼性相區別。鹼性是試劑對質子的親和能力,而親核性是試劑形成過渡態時,對碳原子的親和能力。一般來講,試劑的負電性、鹼性和可極化性越強,其親核性也越強。實際上通常需要綜合考慮這幾個因素以及溶劑的影響。
溶劑
SN2反應在質子溶劑中進行時,一方面,溶劑化作用有利於離去集團的離去;另一方面,溶劑也會與親核試劑發生作用,使親核試劑與底物的接觸變得困難。最後的影響是這兩種因素的綜合結果。相對而言,非極性溶劑分子很少包圍負離子,因此對SN2反應是有利的。
空間效應
反應舉例