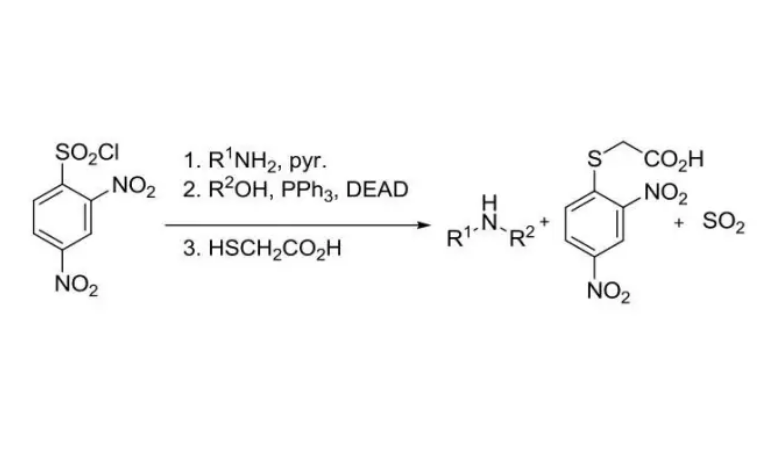
伯胺醯和苯磺醯氯反應生成硝基苯磺醯胺,然後烷基化合成仲胺磺醯胺,脫保護得到仲胺的合成法稱為Fukuyama胺合成反應。N-單取代的苯磺醯胺的烷基化可在一般的烷基化條件或Mitsunobu反應的條件下生成N,N-雙取代的磺醯胺,之後Ns基在溫和的親核試劑作用下經由Meisenheimer中間體很容易脫去,得到相應的仲胺。
基本介紹
- 中文名:Fukuyama胺合成
- 底物:伯胺醯和苯磺醯氯
- 產物:仲胺
- 領域:有機合成
- 特點:反應條件溫和
反應特點,反應機理,反應舉例,仲胺,
反應特點
這一胺合成法的最大優點是烷基化和脫保護步驟都在很溫和的條件下進行,因此,這一方法用在直鏈或大環天然多胺化合物的全合成中非常有效。
硝基苯磺醯胺的質子酸性非常高、在的Mitsunobu反應條件下可以烷基化,而且在弱鹼條件與鹵代烷的烷基化也容易發生。雖然對甲苯磺醯(-Ts)胺也同樣能使用在於烷化反應,但Ns基對硫醇的親核反應的脫保護較容易進行,這點相對脫保護較難的Ts基有優勢。
反應機理
首先伯胺和苯磺醯氯反應生成伯胺的苯磺醯胺,由於形成的苯磺醯胺的質子具有酸性,因此可以和醇進行Mitsunobu反應得到仲胺的苯磺醯胺。巰基乙酸和苯磺醯仲胺發生SNAr反應通過Meisenheimer絡合物,伴隨二氧化硫的離去、脫保護得到仲胺和苯硫醚副產物。
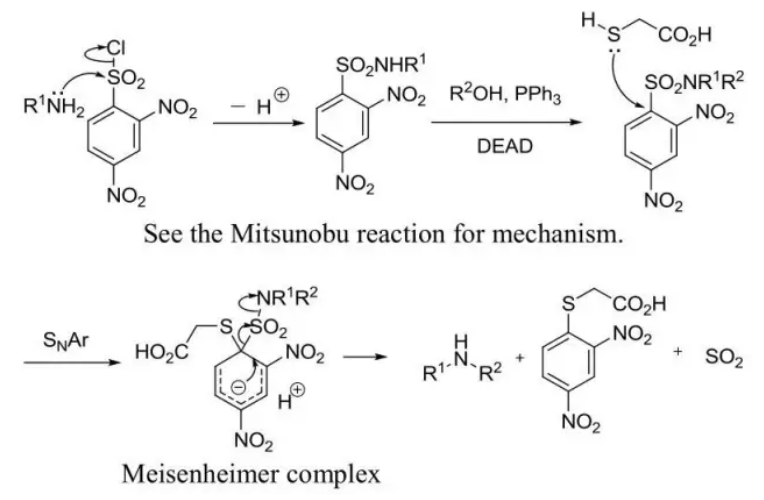 反應機理
反應機理反應舉例
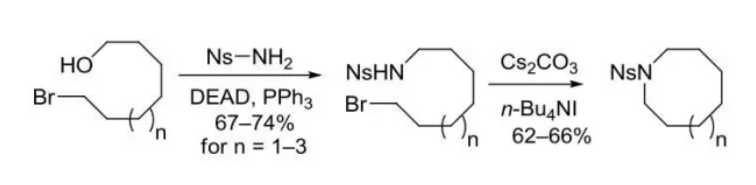 反應舉例
反應舉例仲胺
仲胺(secondary amine)為胺的一種,也稱二級胺,通式為R2NH,與伯胺,叔胺,季銨鹽一起構成了有機胺的四大類。仲胺分子能形成氫鍵。仲胺是眾多天然產物和生物活性分子的合成子,同時也是現代藥物的關鍵活性官能團。
主要有以下兩種合成方法: