事件背景,社會背景,紅曲,事件經過,收到報告,產品檢測,宣布召回,決策遲緩,涉事產品,原因分析,影響人群,事件處置,官方工作,小林製藥,產品下架,對策處理,事件回應,日本政府,日本機構,小林製藥,中國,其他人員,涉事公司,事件影響,影響產品,經濟損失,社會評論,
事件背景
社會背景
保健品在日本被稱作保健功能食品,曾分為特定保健用食品和營養功能食品兩類,2015年後又新增一類“功能性標示食品”。“功能性標示食品”生產商只需在上市銷售前向日本內閤府下屬的消費者廳提交與其聲稱功能相符的科學依據進行備案即可,無需日本政府部門審批許可。這種相對寬鬆的監管機制,可能導致有關各方在安全性檢驗上存在疏忽。
此次事件後,日本政府將著手對所有申報備案過的數千種“功能性標示食品”實施緊急檢查。
紅曲
紅曲是一種在中國已有1000多年套用歷史、目前仍被廣泛使用的食品著色劑
(食用色素),同時也是目前世界上唯一一種利用微生物發酵生產的天然食用色素。紅曲可以賦予食物紅潤鮮艷的顏色,且穩定性較好,又是發酵過程中天然產生的,所以長久以來一直被人們當作天然色素使用。優酪乳、腐乳、果醬、糖果、榨菜、餅乾、速食麵、薯片、飲料等食品中,都可以按生產需要適量使用紅曲。
1979年,日本人從紅麴黴中發現一種能抑制膽固醇合成的活性物質,即Monacolin K(莫納可林),並以此為基礎開發了降膽固醇的藥物洛伐他汀。此後,科學家們又在紅曲中找到了麥角固醇(可在體內轉化為維生素D)、γ-氨基丁酸等更多活性成分。相關科學研究也證實,紅曲中的某些物質具有一定抗癌、降血糖、降血脂、降血壓等功能。不過,這些功效成分含量並不高。另一方面,紅麴黴菌發酵過程中可能會產生微量的有毒物質,如一定程度上具有腎臟毒性和致癌、致畸作用的桔青黴素。
中國食品工業已經篩選出不會產生桔青黴素的優秀紅麴黴菌種,並通過改進生產工藝來減少桔青黴素的產生。同時,中國相關國家標準也對紅曲色素中的桔青黴素作出限量規定。
事件經過
收到報告
2024年1月起,小林製藥已陸續收到13名消費者在服用相關產品後身體不適的報告,其中有6人住院治療,有的患者甚至還需要進行透析。
2024年3月26日,小林章浩在新聞發布會上表明,當他在2月6日收到第一份報告時,就“已經做好了召回的準備”。然而,直至3月中旬公司在重新檢查紅曲等原材料的生產數據並發現分析結果表明存在“未知成分”後,才最終決定主動召回相關產品。
據日本《讀賣新聞》當地時間2024年3月27日報導,相關數據顯示,小林製藥公司在2023年共生產約18.5噸紅曲原料,其中約2.4噸為該公司生產保健品自行使用,餘下的約16.1噸被銷售給其他企業。據悉,這些企業包括食品企業、化妝品企業以及批發商等。數據顯示,銷售給其他企業的約16.1噸紅曲原料中,約6.9噸被用於生產保健品,這其中有一部分紅曲原料里可能含有疑似導致腎臟疾病等健康問題的未知成分。這些原料的全部詳細流通情況尚無法確認。
產品檢測
據報導,在對相關產品初步檢測時並沒有發現“
橘黴素”
(一種已知由紅麴黴菌產生的有毒化合物),於是公司認為患者住院可能是出於過敏等個人原因。因此在公司掌握能夠檢測出未知成分的方法時已經過晚。根據公開資料,橘黴素是一種常見於食物中的黴菌毒素。它是真菌產生的次生代謝產物,會污染長期儲存的食物,並會引起不同的毒性作用,如腎毒性,肝毒性和細胞毒性作用。橘黴素主要存在於貯藏穀物中,但有時也存在於水果和其他植物產品中。
宣布召回
當地時間2024年3月22日,日本小林製藥公司在其官網發通知稱,近期有部分消費者在使用該公司生產的含有紅曲成分的保健品後,出現腎臟等部位的疾病,部分患者進行住院治療,有的甚至需要進行透析。小林製藥稱,對紅曲保健品進行成分分析後發現,部分紅曲原料中可能含有該公司掌握範圍外的未知成分。小林製藥表示,目前這種未知成分與消費者患病之間是否相關還沒有定論,但為了防止消費者健康受損的情況進一步擴大,小林製藥決定對含有紅曲成分的3款產品進行召回,並呼籲消費者立即停止服用這3款產品。
針對此情況,公司對該產品及其所使用的紅麴原料(自社製造)進行了成分分析,結果發現部分紅麴原料中可能含有非預期的成分。部分受影響產品通過跨境渠道銷往中國大陸。在聲明中,小林製藥對天貓小林製藥海外旗艦店、拼多多官方海外旗艦店、小林製藥海外京東直營店的消費者表示,如果持有以下【紅麴膽固醇顆粒 60粒,條形碼4987072059708】,請停止繼續食用。另外,如果消費者曾食用過以上產品,並感覺身體不適,請諮詢客服中心。同時,如果消費者持有該產品,也請聯繫客服中心,公司將向消費者說明退貨及退款方式。
2024年3月22日,日本知名藥企小林製藥公司宣布召回紅曲保健品之後,多家使用了小林製藥生產的紅曲原料的日本企業,陸續對相關產品進行召回。根據日本媒體報導,小林製藥每年生產18.5噸紅曲原料,其中兩成自己使用,其餘八成作為原材料出售給日本國內外的52家企業,最早從8年前就開始進行銷售。截至目前,除了清酒廠商之外,至少還有3家企業陸續召回了零食、海鮮製品和日式點心等食品,相關影響有可能進一步擴大。
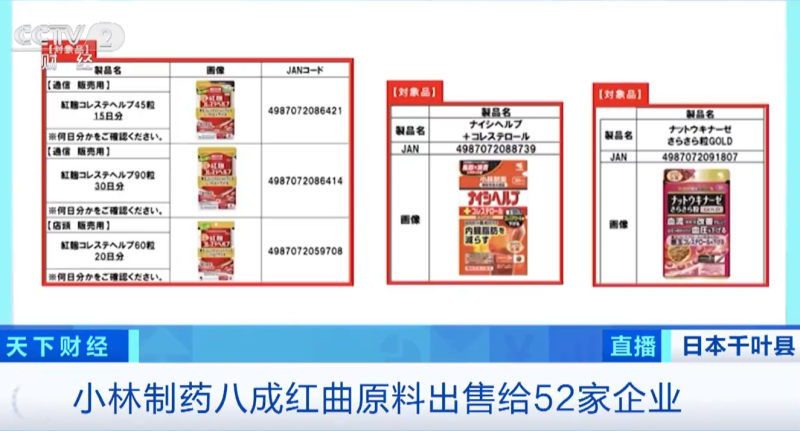
八成作為原材料出售給日本國內外的52家企業
2024年3月24日,小林製藥中國再次發布《關於停止使用紅麴膽固醇顆粒及自主召回的通知》。
2024年3月27日,小林製藥中國在官方微信公眾號發布聲明稱,日本小林製藥株式會社於2024年3月22日,發布了關於對使用紅麴原料的相關產品進行自主召回的公告(公告連結:紅麴関連製品の使用中止のお願いと自主回収のお知らせ)。
日期 | 說明 |
|---|
| 產品可以通過官方渠道退回 記者致電小林製藥詢問召回流程相關事宜,對方表示,在天貓、京東、拼多多海外旗艦店購買的產品可以通過官方渠道退回。 |
| 召回的三款產品均未在中國大陸市場上市銷售,將積極提供產品回收的協助 小林製藥中國在官方微信公眾號發布聲明稱,日本小林製藥株式會社於2024年3月22日,發布了關於對使用紅麴原料的相關產品進行自主召回的公告。小林製藥(中國)有限公司受小林製藥株式會社以及跨境平台官方旗艦店代理商UNQ日本株式會社的委託,將積極協助購買了相關產品的在中國的消費者,做好產品回收的相關事宜。本次召回的三款產品均未在中國大陸市場上市銷售。有中國消費者通過海外跨境平台、境外實體店鋪或是其它渠道購買了相關產品,對此,公司將積極提供產品回收的協助。 |
| 海外消費者與日本消費者享有同樣的對應方案 小林製藥公司社長小林章浩表示,有關海外銷售的相關商品回收,包含紅曲膽固醇顆粒以及作為原料出口的紅曲,將對各公司進行協助,幫助其進行回收。若查明存在健康方面的因果關係,海外消費者將與日本消費者享有同樣的對應方案。 |
決策遲緩
2024年3月22日晚,小林製藥社長公開向公眾鞠躬道歉,但據日媒稱,該公司3月16日已發現問題,卻過了近一周才宣布召回相關產品。對此,小林製藥承認決策遲緩。小林章浩在當日新聞發布會上表明,自1月中旬開始收到為患者進行檢查的醫生的一系列詢問,小林章浩表示,當他在2月6日收到第一份報告時,就“已經做好了召回的準備”。然而,直至3月中旬公司在重新檢查紅曲等原材料的生產數據並發現分析結果表明存在“未知成分”後,才最終決定主動召回相關產品。
2024年4月,小林製藥保健品致死事件持續引發各方關注。分析人士指出,小林製藥的家族企業經營體制弊端和日本“功能性標示食品”制度缺陷是造成目前這一嚴重事態的主要原因。小林製藥公司的董事會由7人組成,其中3人為家族成員,4人為外部董事。該公司從2024年1月15日接到第一例疑似服用含紅曲成分保健品出現健康問題的報告後,直至兩個多月後才公開問題、召回商品,並向外部董事進行報告。
涉事產品
公司官網上公布此次涉事3款產品分別為“紅麴コレステヘルプ”(紅麴膽固醇顆粒)“ナットウキナーゼ さらさら粒GOLD”“ナイシヘルプ+コレステロール”。
據共同社報導,“紅麴膽固醇顆粒”從2021年2月起在電商渠道和門店進行銷售,截至2024年2月底已售出約106萬袋。
2024年3月27日,日本相關政府機構召開聯絡會議公布,可能致人健康受損的產品集中在2023年9月之後的批次。
2024年3月29日,據央視,小林製藥公司生產的可能混有未知有害成分的保健品生產時間集中於2023年4月至10月,上市時間在2023年7月至12月之間。
2024年4月12日,據日本廣播協會電視台(NHK)報導,已於2023年12月關閉的小林製藥公司大阪工廠,在2023年4月曾因生產過程中的疏忽,導致33公斤紅曲生產原料在混合攪拌過程中,散落在地。其中部分原料隨後被收集,並與其它紅曲原料混合後出貨。
原因分析
日本專家認為,此次小林製藥的紅曲相關產品中之所以出現“意想不到”成分,主要有3種可能性:一是在生產過程中混入了“未知成分”的異物,二是混入了能夠生成“未知成分”的微生物,三是紅曲菌株突變成了能產生“未知成分”的菌株。
影響人群
日期 | 影響情況 | 備註 |
|---|
| 小林製藥公司稱,已有33人服用含有紅曲成分保健品後出現腎臟疾病等狀況,其中26人住院。 | |
| 日本小林製藥公司發布訊息稱,收到約50人在服用該公司含紅曲成分的保健品後住院的通報訊息。 | |
在日本厚生勞動省對小林製藥公司進行的聽證會中,小林製藥公司方面報告稱,又有一人或因服用該公司生產的含紅曲成分的保健品而死亡。 |
日本厚生勞動省公布了因攝取含有“小林製藥”公司“紅曲”成分的保健品後發生的第二例死亡案例,入院人數已增至106人。 |
| 日本小林製藥公司發布的訊息,27日該公司收到通報,又有兩名生前服用該公司含有紅曲成分保健品的消費者死亡。截至3月28日,生前服用該公司含有紅曲成分保健品死亡的消費者人數已達到4人。 | 死亡的消費者人數已達到4人,住院的人數修正為93人 |
據日本厚生勞動省訊息,因此前數據存在重複計算,因小林製藥公司相關保健品住院人數修正為93人。 |
| 日本小林製藥公司發布訊息稱,該公司28日收到通報,又有一名生前服用小林製藥含有紅曲成分保健品的消費者死亡。截至3月29日,小林製藥保健品已致5死。 | |
| 截至3月31日,與小林製藥公司含紅曲原料保健品相關的住院人數增至157人。 | |
| 與小林製藥公司含紅曲原料保健品相關的住院人數增至166人。 | |
| 與服用小林製藥公司含紅曲原料保健品相關的住院人數增至177人。 | |
| 與服用小林製藥公司含紅曲原料保健品相關的住院人數增至188人。 | |
| 服用小林製藥含紅曲成分問題保健品的消費者已有5人死亡,住院人數增至196人。 | |
| 服用小林製藥含紅曲成分問題保健品的消費者中,已有212人住院治療,相關諮詢達53000件。 | |
| 與服用小林製藥公司含紅曲原料保健品相關的住院人數增至216人。 | |
| 與服用小林製藥公司含紅曲原料保健品相關的住院人數增至219人。 | |
| 與服用小林製藥公司含紅曲原料保健品相關的住院人數增至226人。 | |
| 與服用小林製藥公司含紅曲原料保健品相關的住院人數增至231人。 | |
事件處置
官方工作
2024年3月26日,TBS報導稱,日本相關部門將對市面上的全部6795種功能食品的安全性等進行緊急檢查。
2024年3月26日,日本岐阜縣西濃保健所對位於岐阜縣池田町的一家小林製藥“紅曲膽固醇顆粒”生產工廠進行了調查。岐阜縣食品衛生科稱,此次調查是應小林製藥公司總部的委託進行的。岐阜西濃保健所的兩名工作人員對工廠的生產方法、日產量等進行了調查。岐阜縣食品衛生科表示,截至26日調查時,尚未收到工廠內有人健康受損的信息。今後將進一步展開調查,並儘快向大阪市報告調查結果。
當地時間2024年3月28日,基於小林製藥公司含紅曲成分保健品導致消費者健康受損的情況,日本消費者廳負責人新井豐宣布,已經開始對市場上全部功能性標識食品的緊急檢查。緊急檢查包括向大約1700家銷售功能性標識食品的企業傳送詢問函,確認是否有醫療機構報告相關健康問題,以及是否已建立了收集健康問題信息的體制。
當地時間2024年3月29日,據日本厚生勞動省發布的信息,52家從小林製藥公司購買紅曲原料的企業進行的自主排查結果顯示,過去3年間,這52家公司沒有相關產品收到過健康損害報告。已知的使用小林製藥公司紅曲原料進行生產的173家企業的自主排查仍在進行中。
據朝日新聞2024年4月4日報導,小林製藥公司3月28日向日本厚生勞動省審議會提交的資料顯示,在小林製藥去年9月生產的紅曲原料樣品中檢測到的“軟毛青黴酸”物質含量最高。厚生勞動省等部門正在調查是否從外部混入黴菌等原因。
2024年4月6日,據日本媒體報導,日本厚生勞動省和大阪市政府相關部門工作人員當天前往小林製藥公司位於大阪市的總部,對紅曲成分問題保健品事件進行調查。
當地時間2024年3月26日,日本厚生勞動省圍繞小林製藥公司紅曲原料可能致使消費者健康受損問題,對小林製藥公司進行了聽證。
當地時間2024年3月27日,圍繞小林製藥公司生產的保健品致消費者健康受損事件,日本厚生勞動省、消費者廳等相關政府機構召開聯絡會議。農林水產省和國稅廳的代表也參加會議。會議討論針對小林製藥的產品以及使用了該公司紅曲原料相關產品的應對策略等內容。根據會議通報,使用小林製藥公司紅曲原料進行生產的企業超過170家。
當地時間2024年3月27日,日本大阪市政府命令小林製藥公司對“紅曲膽固醇顆粒”等三種產品進行召回。
2024年3月28日,日本厚生勞動省召開會議,公布小林製藥紅曲原料的批發商和最終購買商名單,要求這些企業自查是否存在健康危害並提交報告。從小林製藥採購紅曲原料的52家批發商須在4月29日前提交報告,而從這52家公司購買紅曲原料並在產品中使用的173家企業須在4月5日前提交報告。
2024年3月29日,針對近日小林製藥含紅曲成分保健品安全風波,日本厚生勞動大臣武見敬三表示,正在準備設定諮詢客服中心,以便服用該產品的消費者以及相關企業諮詢,同時將在厚生勞動省內設立“紅曲產品對策省廳間合作室”,以供相關部門之間實現信息共享。
當地時間2024年3月30日,日本厚生勞動省和大阪市當地政府部門工作人員進入小林製藥公司大阪工廠檢查。小林製藥公司相關負責人表示,小林製藥方面作為受檢單位,對詳細檢查項目並不知情。
當地時間2024年3月30日,據日本厚生勞動省訊息,圍繞小林製藥公司生產的含有紅曲成分的保健品引起消費者健康受損問題,厚生勞動省將於31日對該公司位於和歌山縣的工廠進行現場調查。
小林製藥
日期 | 處置情況 |
|---|
| 撤回備案 小林製藥公司已從日本消費者廳撤回8種紅曲保健品作為功能性標識食品的備案,其中包括3種已經召回的商品。 |
取消入職儀式 小林製藥公司宣布,決定取消原定於4月1日在大阪市內召開的新員工入職儀式。 |
| 對日本消費者賠償120元代金券 小林製藥在官網上發布訊息,將對相關消費者進行賠償。小林製藥公司公關部門工作人員表示:“針對日本國內,將根據商品種類和數量進行賠償,一件商品賠償2500日元的代金券。針對中國大陸方面的賠償問題,目前還在商議階段,具體的一些情況,我們目前還無法回答。 |
| 對購買該公司紅曲原料的商業夥伴進行賠款 日本小林製藥公司表示,計畫對購買該公司紅曲米作為原料的食品製造商等商業夥伴進行賠款。 |
| 開設退貨接待中心 日本小林製藥公司宣布開設退貨接待中心。根據購買方式不同,可通過電話或網際網路辦理手續,並提供退款,退款對象包括紅曲膽固醇顆粒等三種產品。 |
產品下架
據人民日報健康報導,2024年3月24日記者在多家電商平台搜尋發現,小林製藥官方電商平台沒有上述三款相關產品出售,但許多代購商家仍在出售涉事召回產品。
2024年3月27日,小林製藥在天貓、京東、拼多多的官方客服均表示已下架紅麴膽固醇顆粒,如果在店內購買過的消費者可申請退款退貨。
2024年3月,台灣食藥機構表示,島內業者主動通報121件使用小林製藥公司販賣的紅曲原料的產品。台灣“三合興”、“和司特”公司曾輸入紅曲原料,分別回收405.7公斤和3120公斤。台北市衛生機構截至3月27日已下架相關產品1.2萬盒,另有2萬多盒存放於代工廠。DHC公司宣布,用到小林紅曲原料的“DHC濃縮紅曲”將被全面回收並退款。高雄市衛生機構核查發現,高雄市7家相關商家已自主動通報購買或使用了小林製藥販賣的紅曲原料,並下架疑由這些原料製成的產品,截至3月28日共下架920.14公斤。
對策處理
2024年4月3日,針對日本小林製藥公司含紅曲成分保健品致消費者健康受損事件,公司總部所在的大阪市成立對策總部,負責推進原因調查和問題產品回收工作。對策總部當天召開首次會議,確認三款回收產品在日本全國約2.3萬家實體店鋪共銷售了約86萬個,加上網購等途徑,總計銷量約100萬個。問題保健品有售的129個地方的保健所正在加緊確認產品所在,預計回收完成可能需要幾個月時間。
當地時間2024年4月5日,日本小林製藥公司發布訊息稱,將從6日開始開通針對所有購買了該公司含紅曲成分保健品的網上退貨渠道。
2024年4月7日,據日本“ORICON NEWS”新聞網報導,關於小林製藥紅曲保健品健康安全問題,小林製藥的道歉廣告6日開播。報導稱,這則廣告沒有背景音樂,播音員的語調沉重,體現出問題的深刻程度。
事件回應
日本政府
2024年3月25日,據日本TBS電視台新聞網報導,日本消費者廳要求小林製藥公司提出相關報告,對其含紅曲成分保健品在消費者使用後出現腎病問題一事進行說明。
2024年3月26日,日本消費者擔當大臣自見英子稱,這是受到廣泛關注的、涉及功能食品(保健品)安全性的嚴重問題。
當地時間2024年3月28日,就小林製藥公司含紅曲成分保健品致消費者健康受損一事,日本首相岸田文雄表示,必須努力查明原因,並考慮採取一切必要對應措施。
2024年3月,據日本時事通信社報導,日本厚生勞動省已通知小林製藥公司總部所在的大阪市相關部門,基於《食品衛生法》對該公司相關產品採取廢棄等措施。
2024年3月29日,針對近日小林製藥含紅曲成分保健品安全風波,日本厚生勞動大臣武見敬三表示,正在準備設定諮詢客服中心,以便服用該產品的消費者以及相關企業諮詢,同時將在厚生勞動省內設立“紅曲產品對策省廳間合作室”,以供相關部門之間實現信息共享。
2024年3月29日,日本厚生勞動大臣武見敬三就小林製藥公司含紅曲成分保健品相關健康受損問題表示,將攜手地方政府對該公司的原料製造工廠進行入內檢查。
2024年4月5日,日本厚生勞動相武見敬三出席眾院厚勞委員會會議,就政府正在推進的原因調查和措施調整表示:“製造工序、安全管理等企業治理存在何種問題,將徹底調查,探討必要的規則。”為防止問題再次發生,武見敬三稱“若需法制化,將迅速辦理”,示意將探討諸如修改《食品衛生法》等相關法律。
2024年3月27日,日本內閣官房長官
林芳正在首相官邸召開的記者會上表示,“此次事件引發了對功能性標識食品安全性的憂慮,很嚴重。”
當地時間2024年3月28日,日本內閣官房長官林芳正表示,就小林製藥公司生產的含有紅曲原料的保健品引發服用者健康受損問題,正在向世界衛生組織以及其他國家和地區提供信息。
地時間2024年4月3日,據朝日電視台當報導,關於小林製藥公司含紅曲成分保健品導致消費者健康受損問題,大阪市當天上午成立對策總部,並召開了首次會議,確認了包括含紅曲成分產品的召回情況以及事件原因的調查進展。大阪市政府已根據《食品衛生法》命令該公司召回包含紅曲成分的3種產品。報導稱,相關產品已在日本129個地區約23000家店鋪中銷售了約860000份。目前各保健所正在確認相關商品的具體銷售情況。大阪市長決定成立由其領導的對策總部來應對此事。對策總部由健康局長等約10人組成。
2024年4月12日,大阪市市長橫山英幸稱,大阪市將繼續對小林製藥公司大阪工廠的衛生管理體系是否存在問題等情況展開調查。
日本機構
當地時間2024年4月1日,由日本相關領域醫生組成的日本腎臟學會發布了對小林製藥公司含紅曲保健品疑致消費者健康受損事件的獨立調查分析報告。
2024年4月1日,日本腎臟學會在官網公布了以47名健康受損消費者為對象的獨立調查報告,結果顯示約四分之三消費者停止服用問題保健品後症狀改善,還有四分之一接受了類固醇治療。
2024年4月8日訊息,日本政府和日本腎臟學會訊息顯示,小林製藥公布問題前,多例感到身體不適的消費者根據醫生診斷或自主判斷而停止攝入後恢復健康,也有人可能因停止服用而未發展成重症住院。健康受損的原因詳情據悉還在調查之中,但若能早日公開信息,也可能減少受害。小林製藥在認識到健康受損到公布訊息之間的約2個月中估計有持續服用的消費者,應對遲緩的問題或再度受到質疑。
2024年4月9日,日本腎臟學會公布調查結果,稱多數患者出現一個共同的病症,
范可尼綜合徵。即腎小管功能障礙疾病。這些患者的腎小管功能出現異常,無法回收多種人體需要的物質,而是將這些物質排出體外。
2024年4月4日,日本消費者廳公布的功能性標識食品資料庫顯示,小林製藥公司未能及時更新紅曲膽固醇顆粒的產品信息,在大約2021年11月前後出現了該商品銷售情況不明的情況。在一段時間內,應填寫“銷售中”或“銷售暫停中”的欄目顯示為空白。對此,小林製藥表示,他們曾經嘗試更新,但由於等待日本消費者廳的受理需要時間,因此未能及時完成更新。根據東京商工研究機構的調查結果,截至3月底,資料庫中約1600家公司的15%商品出現了類似的信息缺失問題。
小林製藥
2024年3月26日,小林製藥聲明稱,一名持續服用含有紅曲成分保健品的消費者因腎病死亡,正在調查該消費者死亡與服用產品的因果關係。
當地時間2024年3月27日,小林製藥公司發布訊息稱,圍繞該公司含紅曲成分保健品疑似致消費者健康受損問題,該公司社長小林章浩等人於3月29日下午在大阪市舉行記者會。
當地時間2024年3月27日,小林製藥公司總部所在地大阪市的政府部門舉行記者會。大阪市政府方面稱,小林製藥公司用於生產可能存在問題的紅曲原料的工廠位於大阪市淀川區,已於去年年底關閉,無法對現場衛生狀況等進行確認。目前該工廠中的設備等已轉移到和歌山縣,大阪市政府方面沒有許可權進行調查。大阪市政府表示,將就相關情況與和歌山縣政府展開協作,並將根據小林製藥公司提供的報告等,與厚生勞動省合作,儘快查明原因。
當地時間2024年3月28日據日本《讀賣新聞》報導,圍繞小林製藥公司生產的含紅曲成分保健品致消費者健康受損問題,由日本相關領域醫生組成的日本腎臟學會從27日開始,面向該學會在全日本範圍內的成員進行詢問調查,以確認各位醫生在接診過程中,是否遇到疑似因服用相關保健品等原因而出現腎臟疾病症狀的患者。
2024年3月29日,小林製藥公司向日本厚生勞動省報告,其紅曲產品中導致問題的成分可能為“軟毛青黴酸”(Puberulic Acid)。
當地時間4月1日,日本小林製藥公司宣布開設退貨接待中心。根據購買方式不同,可通過電話或網際網路辦理手續,並提供退款,退款對象包括紅曲膽固醇顆粒等三種產品。
當地時間2024年4月3日,據日本《朝日新聞》報導,日本小林製藥公司已決定停止面向2025年應屆畢業生的招聘。據悉,已申請應聘小林製藥公司的學生,在3月30日至31日已陸續收到了招聘計畫終止的通知。
中國
2024年3月29日,中國消費者協會就服用日本小林製藥公司生產的紅曲膽固醇顆粒等產品導致消費者死亡一事,發布消費提示,應立即停止服用有關產品,積極配合召回。經中消協與小林製藥(中國)有限公司客服中心電話溝通核實,中國消費者除通過跨境平台、境外實體店鋪或者海外代購等渠道購買外,日本小林製藥公司生產的紅曲膽固醇顆粒、納豆激酶顆粒以及降膽固醇健康輔助顆粒等產品未在中國大陸市場上銷售。
截至2024年3月31日13時,台灣地區食品藥物管理部門通報,共接到6例與小林製藥紅曲產品相關案例。這些案例將被送去相關部門進行進一步評估。據悉,台灣有若干企業輸入小林製藥的紅曲原料,製成紅曲膠囊售賣。食品藥物管理部門已預防性下架226種相關產品。
其他人員
人群 | 說明 | 圖片 |
|---|
| 這么大的企業還能出現這么嚴重的問題,真的很糟糕。 已經賣了這么多年的產品,怎么現在才報告有這樣的問題。長期服用的人已經攝入很多了,很多食品里也都用了這種原料,連味噌醬里也有。 | |
| 從多名服用者出現腎臟疾患需住院治療,以及出現死亡案例來看,推測是紅曲培養過程中產生了毒素,也不排除人為投毒的可能性。不確定致病物質就無法確定治療方法,應該回收哪些商品、今後如何防止同樣事件發生、誰來負責,目前還都是未知數。應該儘快確定致病物質,這非常重要。 |  唐木英明 |
| 這次的含紅曲成分保健品宣稱可以降膽固醇。也許有,但並沒有經過嚴格的科學驗證。降低膽固醇是為了降低腦梗和心梗等血管阻塞引起的疾病,這些效果根本沒有得到驗證,但在市場上銷售,讓消費者誤認為有效果。從醫務人員角度來看,是很不合適的。久住英二認為,小林製藥作為老牌製藥公司,發生這樣的事故,嚴重影響了公眾對製藥和食品行業的信任,恢復公眾信任將很艱難。 |  久住英二 |
| 2024年3月28日報導,中國台灣高雄一名陳姓男子向媒體表示,他70歲的太太2023年3月開始服用“大醫生技”的“紅曲膠囊”,才大概吃了2個月,就出現急性腎臟病,同年5月已經開始洗腎。小林製藥紅曲事件發生後,陳先生接到要求停止食用紅曲產品的信息,因此懷疑是小林的紅曲產品導致太太罹患腎病。 | |
涉事公司
小林製藥是一家以產品開發為主的企業,主要從事藥品、醫療器械、日用品、食品等的研發生產與銷售。該公司稱,紅曲是在蒸熟的大米中混入紅曲菌發酵後產生的原料。該公司宣傳這一成分有望降低低密度脂蛋白膽固醇值。1886年創立初期時名為“小林盛大堂”,當時總部位於日本名古屋。公司成立於1998年,產品不僅在日本國內銷售,還銷往美國、英國、東南亞等世界各地。上海小林日化有限公司是小林製藥在中國的獨資子公司。
小林製藥目前在中國國內銷售的品牌主要有一次性使用懷爐系列“暖寶寶”、退熱冷貼系列“冰寶貼”、芳香劑系列“爽花蕾”及“香居源”等。據小林製藥在其日本官網披露的最新業績,2023年上半年公司銷售額為736億日元(約合35億元人民幣),同比增長3.3%;營業利潤為104億日元(約合5億元人民幣),同比增長5.5%;當期淨利潤為78億日元(約合3.7億元人民幣),同比增長2.1%。
2024年3月25日,受紅曲原料問題影響,小林製藥公司的股價收跌16.51%。
事件影響
影響產品
小林製藥宣布緊急召回相關產品後,日本各食品、酒類製造商陸續宣布回收含有小林製藥生產的紅曲相關產品。
2024年3月24日,日本寶酒造公司發布訊息稱,因該公司生產的一款酒使用了由小林製藥公司提供的紅曲原料,決定對約9.6萬瓶該產品進行自主回收。目前沒有與寶酒造公司該產品相關的健康損害報告。酒企廠家表示,這款酒只出口到了新加坡和中國台灣,沒有流入中國大陸市場。

日本寶酒造公司宣布召回產品
截至當地時間2024年3月26日晚間,包括小林製藥公司在內,已有30家企業宣布自主回收使用了小林製藥公司紅曲原料的產品。
2024年4月,日本帝國資料庫公司一項最新調查結果顯示,小林製藥公司生產的問題紅曲原料最多恐波及日本國內3.3萬家企業,其中包括超過5000家食品和飲料零售商。日本功能性標識食品的市場占比很大。據《日經亞洲評論》報導,日本調查機構“富士經濟”的數據顯示,2020年功能性標識食品市場規模反超特定保健用食品,2023年同比增加19%,達到6865億日元。商品數量達到約6700種,是特定保健用食品數量的6倍。
2024年4月4日,日本多家媒體報導稱,小林製藥今年1月就已接到含紅曲成分保健品致消費者健康受損的報告,然而卻在兩個多月後才告知公司外部董事並宣布召回相關產品。
2024年4月12日,日本消費者廳說,受小林製藥公司含紅曲成分問題保健品事件影響,他們對數千種功能性標示食品實施了緊急檢查,發現上百例消費者健康受損案例。
2024年4月13日,據日本《朝日新聞》報導,日本消費者廳12日以6795種(1693家企業)申報為功能性食品的產品為對象進行調查。結果顯示,此前醫療從業人員曾向相關企業發出過涉及18種產品、共117例損害健康報告。報導稱,截至12日0時,有1395家企業(5551種產品)對上述調查作出回答。以產品來衡量的回答率為81.7%。其中有銷售歷史的產品為3914種產品。
經濟損失
小林製藥可能要承擔的經濟損失主要來自三個方面。
一是,對於服用小林製藥含有紅曲成分保健品的人群,同時包括住院案例和死亡案例的賠付;
二是,小林製藥三款產品的召回和下架帶來的經濟損失;
三是,紅曲原料所輻射的更多產品,其召回或下架會帶來的潛在影響。
社會評論
小林製藥在藥品和日用品領域打造了多款爆款產品。此次13人服用該公司銷售的功能性食品後患上腎臟疾病一事,損害了該公司的信譽並動搖了其管理層。在保健食品的需求不斷上升的如今,意外事故和副作用帶來的風險再次凸顯。(日本產經新聞 評)
作為消費者,應培養不迷信不盲從的消費觀念,堅持從個人實際需要出發理性消費。相關部門應強化對跨境電商平台的管理,引導平台企業壓實主體責任,對於跨境商品,特別是跨境保健品和藥品要選擇正規的品牌授權渠道進口,確保商品符合國家的質量和安全標準。電商平台在跨境保健品和藥品的宣傳上要真實完整,不誇大功效,不給消費者以不合理的預期,同時要做好信息同步和售後服務。一旦海外品牌出現問題,平台要同步通知國內消費者,並積極協助消費者做好維權工作。(經濟日報 評)





