《20(R)-人參皂苷Rg3藥用組合物水溶液及製備方法》是富力於2006年5月22日申請的專利,該專利的申請號為2006100466172,公布號為CN1883492,授權公布日為2006年12月27日,發明人是富力、赫瀾銘、劉紅、魯明明、魯岐。
一種20(R)-人參皂苷Rg3藥用組合物水溶液,其含原料0.5~10毫克/毫升,其製備方法:將0.1~5%的人參皂苷溶液加到溫度為40~100℃的0.1~30%輔料A、B①②⑤水溶液中,兩者重量比為1:1~300,減壓回收溶劑後加水;另一種含原料0.1~2毫克/毫升的20(R)-人參皂苷Rg3藥用組合物水溶液,其製備方法:將0.1~5%的人參皂苷溶液加到溫度為60~100℃的20~65%輔料B③④的水溶液中,兩者重量比為1:100~400,減壓回收溶劑後加水;上述20(R)-人參皂苷Rg3組合物水溶液及乾燥後所得水溶性粉末,用其製備注射、口服和外用藥物製劑的生物利用度較高,其具有抗腫瘤、合併放化療增效減毒、提高免疫功能、抗疲勞、改善記憶、消腫止痛及癒合傷口的作用。
2016年12月7日,《20(R)-人參皂苷Rg3藥用組合物水溶液及製備方法》獲得第十八屆中國專利優秀獎。
基本介紹
- 中文名:20(R)-人參皂苷Rg3藥用組合物水溶液及製備方法
- 公布號:CN1883492
- 授權日:2006年12月27日
- 申請號:2006100466172
- 申請日:2006年5月22日
- 申請人:富力
- 地址:遼寧省大連市大連開發區鐵山中路5號大連富生藥物公司
- 發明人:富力、赫瀾銘、劉紅、魯明明、魯岐
- Int.Cl.:A61K31/704(2006.01);A61K9/08(2006.01);A61K9/19(2006.01);A61P35/00(2006.01)
- 代理機構:大連萬友專利事務所
- 代理人:王麗英
- 類別:發明專利
專利背景
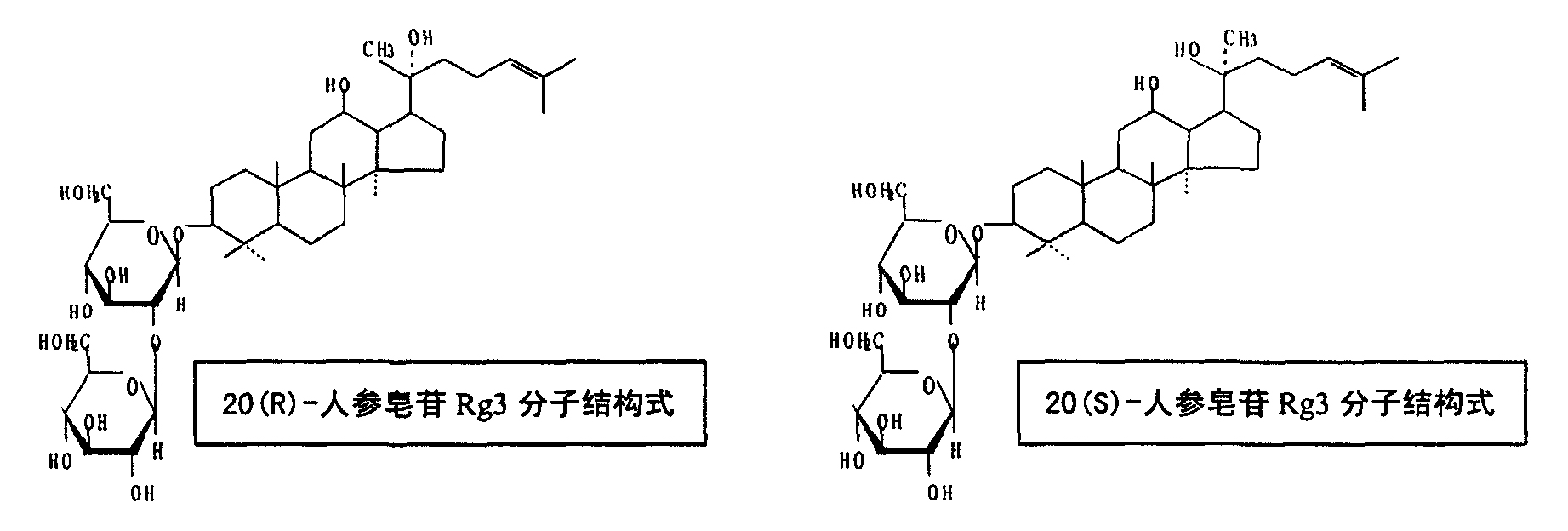
發明內容
專利目的
技術方案
乾燥方法 | 乾燥條件 |
真空乾燥 | 在30~60℃溫度,0.01~0.08兆帕壓力下,乾燥48小時。 |
噴霧乾燥 | 採用超音速射流技術,射流技術300~900米/秒,在30~60℃溫度,0.01~0.05兆帕壓力下,以超音速速度瞬時乾燥。 |
冷凍乾燥 | 先於-45℃預凍5小時;按程式升溫冷凍乾燥:-45~-15℃升華乾燥20小時,再於-15~30℃真空乾燥10小時。 |
改善效果
附圖說明
技術領域
權利要求
實施方式
- 實施例1
- 實施例2
- 實施例3
- 實施例4
- 實施例5~43
實施例 | 原料(克) | 溶解原料的混合有機溶劑(毫升) | 輔料(克) | 輔料溶液濃度% | 增溶反應溫度(℃) | 攪拌時間(小時) | 原料:輔料 | Rg3毫克/毫升 |
5 | 0.2 | 氯仿-乙酸乙酯-甲醇-水(25:45:30:15,下層)80 | 脫氧膽酸鈉0.2 | 0.1 | 40 | 0.1 | 1:1 | 0.5 |
6 | 1 | 氯仿-乙酸乙酯-甲醇-水(25:45:30:15,下層)800 | 脫氧膽酸100 | 10 | 60 | 3 | 1:100 | 10 |
7 | 1 | 氯仿-乙酸乙酯-甲醇-水(25:45:30:15,下層)800 | 脫氧膽酸50 | 30 | 60 | 0.5 | 1:100 | 10 |
8 | 1 | 乙醇-水(90:10)1000 | 十二烷基硫酸鈉5 | 5 | 50 | 2 | 1:5 | 5 |
9 | 10 | 乙腈-甲醇(70:30)1000 | 十二烷基磺酸鈉400 | 20 | 55 | 3 | 1:40 | 2 |
10 | 5 | 乙腈-甲醇(80:20)500 | 十二烷基磺酸鈉100 | 10 | 45 | 1.5 | 1:20 | 1 |
11 | 1 | 二甲基亞碸:水(90:10)50 | 精氨酸100 | 20 | 50 | 1 | 1:100 | 2 |
12 | 5 | 二甲基亞碸:水(80:20)250 | 精氨酸100 | 25 | 50 | 1 | 1:20 | 1 |
13 | 5 | 氯仿-甲醇-水(70:30:10,下層)5000 | 聚合環糊精納米粒500 | 30 | 100 | 5 | 1:100 | 1 |
14 | 2 | 氯仿-甲醇-水(60:40:10,下層)200 | 聚合環糊精納米粒200 | 10 | 80 | 2 | 1:100 | 2 |
15 | 1 | 乙醇-水(95:5)500 | 聚合環糊精100 | 20 | 65 | 2.3 | 1:100 | 0.5 |
16 | 1 | 乙醇-水(90:10)600 | 聚合環糊精150 | 30 | 85 | 2.6 | 1:150 | 0.8 |
17 | 0.5 | 甲醇-水(90:10)250 | 支鏈環糊精200 | 10 | 100 | 1 | 1:200 | 0.5 |
18 | 0.5 | 甲醇-水(85:15)200 | 支鏈環糊精300 | 15 | 95 | 0.8 | 1:300 | 0.9 |
19 | 1 | 乙腈-水(40:60)500 | β-環糊精150 | 30 | 65 | 1.3 | 1:150 | 1 |
20 | 300 | 二甲基亞碸:水(90:10)1000 | 2,6-二甲基-β-環糊精3000 | 30 | 100 | 3 | 1:10 | 1 |
21 | 5 | 二甲基亞碸:水(80:20)125 | 2,6-二甲基-β-環糊精800 | 25 | 95 | 3 | 1:160 | 2 |
22 | 1 | 乙腈-甲醇(70:30)200 | 納米基-β-環糊精90 | 0.5 | 60 | 0.7 | 1:90 | 0.5 |
23 | 3 | 乙腈-甲醇(80:20)3000 | 納米基β-環糊精150 | 30 | 60 | 3 | 1:50 | 2 |
24 | 2 | 乙腈-乙醇(70:30)200 | 磺丁醚β-環糊精140 | 25 | 75 | 1 | 1:70 | 0.5 |
25 | 2 | 乙腈-乙醇(80:20)400 | 磺丁醚β-環糊精180 | 15 | 95 | 3 | 1:90 | 1 |
26 | 1 | 丙二醇:乙醇:吐溫80:水(40:10:1:49)600 | 甲基-β-環糊精300 | 30 | 60 | 2 | 1:300 | 0.5 |
27 | 1 | 丙二醇:乙醇:吐溫80:水(50:20:1:29)40 | 甲基-β-環糊精150 | 25 | 65 | 1.2 | 1:150 | 1 |
28 | 1 | 丙二醇:甲醇:吐溫80:水(40:10:1:49)50 | 不定位甲基化-β-環糊精240 | 20 | 100 | 2.5 | 1:240 | 0.5 |
29 | 1 | 丙二醇:甲醇:吐溫80:水(50:20:1:29)65 | 不定位甲基化-β-環糊精300 | 30 | 95 | 1.2 | 1:300 | 0.8 |
302 | 2 | 二氯甲烷-甲醇-水(65:35:10,下層)200 | 2-羥丙基-β-環糊精200 | 40 | 60 | 1.3 | 1:100 | 2 |
31 | 2 | 二氯甲烷-甲醇-水(60:40:10,下層)350 | 2-羥丙基-β-環糊精600 | 60 | 65 | 4.8 | 1:300 | 0.1 |
32 | 1 | 二氯甲烷-乙醇-水(65:35:10,下層)300 | 3-羥丙基-β-環糊精120 | 65 | 70 | 0.9 | 1:120 | 2 |
33 | 1 | 二氯甲烷-乙醇-水(60:40:10,下層)500 | 3-羥丙基-β-環糊精300 | 65 | 80 | 1.3 | 1:300 | 0.8 |
34 | 2 | 氯仿-乙醇-水(70:30:10,下層)350 | 2,3-二羥丙基-β-環糊精200 | 50 | 60 | 1.5 | 1:100 | 1.5 |
35 | 2 | 氯仿-乙醇-水(60:40:10,下層)250 | 2,3-二羥丙基-β-環糊精400 | 50 | 70 | 2 | 1:200 | 0.6 |
36 | 5 | 二甲基亞碸:甲醇(80:20)25 | 2,3,6-三羥丙基-β-環糊精500 | 65 | 65 | 1.7 | 1:100 | 0.1 |
37 | 0.5 | 二甲基亞碸:乙醇(90:10)30 | 羥乙基-β-環糊精75 | 30 | 80 | 0.45 | 1:150 | 0.5 |
38 | 0.5 | 二甲基亞碸:乙醇(80:20)400 | 羥乙基-β-環糊精175 | 60 | 85 | 0.5 | 1:350 | 0.2 |
39 | 1 | 氯仿-乙酸乙酯-甲醇-水(25:45:30:15,下層)500 | β-環糊精與2-羥丙基-β-環糊精混合物(1:1)150 | 25 | 60 | 1.7 | 1:150 | 2 |
40 | 1 | 氯仿-甲醇-水(70:30:10,下層)330 | 2-羥丙基-β-環糊精與3-羥丙基-β-環糊精混合物(1:5)400 | 20 | 70 | 2.6 | 1:400 | 1 |
41 | 1 | 乙腈-乙醇(70:30)100 | 聚合環糊精納米粒、β-環糊精混合物、磺丁醚β-環糊精混合物(1:1:1)90 | 50 | 95 | 1.4 | 1:90 | 0.5 |
42 | 2 | 二甲基亞碸:甲醇(80:20)100 | 2-羥丙基-β-環糊精、3-羥丙基-β-環糊精與2,3,6-三羥丙-基-β-環糊精混合物(1:5:10)480 | 60 | 80 | 1.5 | 1:240 | 2 |
43 | 0.5 | 丙二醇:乙醇:吐溫80:水(40:10:1:49)200 | β-環糊精、聚合環糊精與2-羥丙基-β-環糊精混合物(2:5:5)200 | 45 | 85 | 1.1 | 1:400 | 2 |
- 實施例44
- 實施例45
- 實施例46 20(R)-人參皂苷Rg3組合物顆粒劑體內提高生物利用度的試驗
- 實施例47 20(R)-人參皂苷Rg3組合物凍乾粉針劑抗腫瘤藥效學試驗
樣品 | 劑量毫克/千克/次 | 給藥方案 | 給藥總劑量(毫克) | 動物數(只)始/終 | 動物體重(g)開始 | 平均生存(d)X±SD | 生命延長率T/C×% |
Rg3粉針劑 | 1.5 | iv×14bid | 42 | 6/0 | 22.3 | 29.60±2.4*** | 135.16 |
Rg3粉針劑 | 0.75 | iv×14bid | 21 | 6/0 | 21.7 | 28.50±3.3*** | 130.14 |
Rg3膠囊劑 | 3 | ig×14qd | 84 | 6/0 | 22 | 28.80±2.8*** | 131.51 |
CTX | 30 | ip×7qd | 210 | 6/0 | 21.7 | 34.50±4.0*** | 157.53 |
陰性對照組 | 相應輔料 | iv×14bid | 84 | 12/0 | 21.8 | 21.90±2.35 |
樣品 | 劑量毫克/千克/天 | 給藥方案 | 給藥總劑量(毫克) | 動物數(只)始/終 | 動物體重(g)始/終 | 肺克隆數(只)X±SD | 抗轉移率% |
Rg3粉針劑 | 1.5 | iv×14bid | 42 | 10/10 | 20.1/24.7 | 20.6±6.8*** | 55.33 |
Rg3粉針劑 | 0.3 | iv×14bid | 8.4 | 10/10 | 19.8/25.3 | 26.5±6.1*** | 42.54 |
Rg3膠囊劑 | 6 | ig×10qd | 60 | 10/10 | 19.8/24.8 | 22.8±6.7*** | 50.56 |
Rg3膠囊劑 | 3 | ig×10qd | 30 | 10/10 | 19.9/25.2 | 27.5±7.7*** | 40.37 |
CTX | 100 | ip×2qod | 200 | 10/10 | 19.8/22.6 | 3.5±3.7*** | 92.41 |
陰性對照組 | 相應輔料 | iv×14bid | 42 | 20/20 | 19.7/25.3 | 46.12±12.46 |
樣品 | 劑量毫克/千克/天 | 給藥方案 | 給藥總劑量(毫克) | 動物數(只)始/終 | 動物體重(g)開始 | 平均生存(d)X±SD | 生命延長率T/C×% |
Rg3粉針劑 | 3 | v×14bid | 42 | 6/0 | 21.5 | 21.88±5.8*** | 160.88 |
Rg3粉針劑 | 1.5 | iv×14bid | 8.4 | 6/0 | 22.7 | 21.72±3.1*** | 159.71 |
Rg3粉針劑 | 0.75 | iv×14bid | 60 | 6/0 | 22.4 | 20.30±4.7*** | 149.26 |
Rg3粉針劑 | 0.375 | iv×14bid | 30 | 6/0 | 21.9 | 17.95±3.5*** | 131.98 |
CTX | 30 | ip×7qd | 200 | 6/1 | 22.2 | 29.20±4.8*** | 214.71 |
陰性對照組 | 相應輔料 | iv×14bid | 42 | 12/12 | 21.1 | 13.60±2.39 |
樣品 | 劑量毫克/千克/天 | 給藥方案 | 給藥總劑量(毫克) | 動物數(只)始/終 | 動物體重(g)開始 | 平均生存(d)X±SD | 生命延長率T/C×% |
Rg3粉針劑 | 3 | iv×14bid | 42 | 6/0 | 21.2 | 36.88±3.0*** | 162.04 |
Rg3粉針劑 | 1.5 | iv×14bid | 8.4 | 6/0 | 21.1 | 35.71±3.1*** | 156.9 |
Rg3粉針劑 | 0.75 | iv×14bid | 60 | 6/0 | 20.5 | 33.15±3.6*** | 145.65 |
Rg3粉針劑 | 0.375 | iv×14bid | 30 | 6/0 | 20.4 | 29.32±4.7*** | 128.82 |
CTX | 30 | ip×7qd | 200 | 6/2 | 21.8 | 41.20±3.8*** | 181.02 |
陰性對照組 | 相應輔料 | iv×14bid | 42 | 12/0 | 20.7 | 22.76±2.14 |
樣品 | 劑量毫克/千克/天 | 給藥方案 | 動物數(只)始/終 | 動物體重(g)始/終 | 平均生存(d)X±SD | 抗轉移率% |
Rg3粉針劑 | 3 | iv×14bid | 10/10 | 20.3/25.3 | 19.1±7.9*** | 62.03 |
Rg3粉針劑 | 1.5 | iv×14bid | 10/10 | 20.5/25.2 | 22.4±6.9*** | 55.47 |
Rg3粉針劑 | 0.75 | iv×14bid | 10/10 | 19.5/24.7 | 27.3±8.7*** | 45.73 |
Rg3粉針劑 | 0.375 | iv×14bid | 10/10 | 20.4/25.2 | 30.2±7.3*** | 39.96 |
Rg3+CTX | 3.0+15 | iv×14bid+ip×7qd | 10/10 | 19.8/23.8 | 14.1±3.6*** | 71.97 |
Rg3+CTX | 1.5+15 | iv×14bid+ip×7qd | 10/10 | 19.1/24.5 | 16.3±6.1*** | 67.59 |
Rg3+CTX | 0.75+15 | iv×14bid+ip×7qd | 10/10 | 19.9/24.1 | 19.2±4.7*** | 61.83 |
Rg3+CTX | 0.375+15 | iv×14bid+ip×7qd | 10/10 | 19.6/24.2 | 21.9±7.6*** | 56.46 |
CTX | 15 | ip×7qd | 10/10 | 20.2/24.7 | 26.1±5.2*** | 48.11 |
CTX | 30 | ip×7qd | 10/10 | 19.9/22.6 | 3.30±2.6** | 93.44 |
陰性對照組 | 相應輔料 | iv×14bid | 20/20 | 20.1/25.5 | *50.3±13.1 |
組別 | 劑量(毫克/千克) | 平均瘤重(g,X±SD)) | 抑瘤率(%) | WBC(10/L) | Hb(g/L) | RBC(10/L) | |
H2O(對照) | 1.5×8 | 1.84±0.85 | 6.3±0.8 | 93±2.5 | 3.2±0.1 | ||
Rg3 | 1.5×8 | 0.69±0.14** | 62.5 | 8.1±0.2** | 109±6.0** | 3.7±0.4** | |
化療藥 | CTX | 10×3 | 0.89±0.29** | 56.52 | 3.2±0.5** | 82±8.4** | 2.8±0.3** |
5FU | 25×3 | 1.08±0.34** | 41.3 | 3.9±0.3** | 90±13.0 | 3.1±0.4 | |
MTX | 5×3 | 0.27±0.01** | 85.32 | 1.6±0.1** | 51±1.0** | 1.8±0.1** | |
PDD | 1×3 | 1.09±0.30** | 40.76 | 6.0±0.2 | 90±6.0 | 3.1+0.2 | |
Rg3粉針劑+CTX | (1.5×8+10×3) | 0.48±0.12** | 73.91 | 7.1±0.3** | 85±3.6 | 2.8±0.8 | |
Rg3粉針劑+5FU | (1.5×3+25×3) | 0.95±0.17** | 48.37 | 7.8±0.3** | 87±14.0 | 2.8±0.8 | |
Rg3粉針劑+MTX | (1.5×8+5×3) | 0.20±0.04** | 89.13 | 5.2±0.8* | 91±10.0 | 3.1±1.0 | |
Rg3粉針劑+PDD | (1.5×8+1×3) | 1.03±0.28** | 44.02 | 6.6±0.8* | 103±18.0* | 3.6±0.5* | |
組別 | 劑量(毫克/千克) | 給藥方案 | OD值(X) | NK活性(%) |
Rg3粉針劑 | 3 | po×10qod | 0.387 | 42.29** |
0.6 | po×10qod | 0.351 | 46.41** | |
0.12 | po×10qod | 0.368 | 43.82** | |
對照組 | 100 | po×10qod | 0.381 | 41.83** |
人參總皂甙 | 相應混懸劑 | po×10qd | 0.525 | 19.84 |
0.655 |
組別 | 劑量(毫克/千克) | 給藥方案 | 動物數(只) | IL-2活性/cpm(X±SD) |
Rg3粉針劑 | 3 | po×10qod | 6 | 2836±326** |
0.6 | po×10qod | 6 | 3122±735** | |
0.12 | po×10qod | 6 | 2414±539** | |
人參總皂甙 | 100 | po×10qod | 6 | 2785±255** |
對照組 | 相應混懸劑 | po×10qod | 10 | 1351±127 |
組別 | 劑量(毫克/千克) | 給藥方案 | 吞噬活性(X+SD) | |
吞噬百分比 | 吞噬指數 | |||
Rg3粉針劑 | 3 | po×10qod | 31.80土10.00** | 0.55±0.11** |
0.6 | po×10qod | 32.80士10.30** | 0.58±0.14** | |
0.12 | po×10qod | 28.70士7.40** | 0.50士0.11** | |
人參總皂甙 | 100 | po×10qod | 29.60±10.00** | 0.55土0.11** |
對照組 | 相應混懸劑 | po×10qod | 20.90土5.80 | 0.34±0.10 |
- 實施例48 20(R)-人參皂苷Rg3組合物膠囊劑抗疲勞試驗
組數 | 動物數(只) | 初始體重(g) | 中期體重(g) | 結束體重(g) |
陰性對照 | 57 | 20.58±1.51 | 30.04±3.44 | 34.04±4.21 |
低劑量組 | 59 | 20.61±1.43 | 28.34±2.95 | 33.08±3.88 |
中劑量組 | 58 | 20.71±1.41 | 29.90±3.12 | 32.83±3.65 |
高劑量組 | 58 | 20.62±1.48 | 28.36±2.77 | 32.34±3.29 |
組別 | 動物數(只) | 游泳時間(秒) | P值* |
陰性對照 | 14 | 387±239 | |
低 | 14 | 703±597 | <0.05 |
中 | 14 | 519±167 | >0.05 |
高 | 14 | 707±430 | <0.05 |
組別 | 動物數(只) | 爬桿時間(秒) | P值* |
陰性對照 | 13 | 172±115 | |
低 | 13 | 340±153 | <0.05 |
中 | 13 | 332±337 | <0.05 |
高 | 13 | 183±84 | >0.05 |
組別 | 動物數(只) | 血清尿素氮含量(毫克/分升) | P值* |
陰性對照 | 12 | 27.95±3.32 | |
低 | 12 | 26.66±4.24 | >0.05 |
中 | 12 | 24.89±3.70 | <0.05 |
高 | 12 | 22.92±2.25 | <0.05 |
組別 | 動物數(只) | 肝糖原含量(毫克/分升) | P值* |
陰性對照 | 15 | 1817.07±1076.76 | |
低 | 14 | 2327.14±1075.33 | >0.05 |
中 | 15 | 1942.53±761.87 | >0.05 |
高 | 14 | 2611.78±1049.64 | <0.05 |
組別 | 動物數(只) | 乳酸含量(毫摩爾/升) | P值* | ||
運動前(A) | 運動後0分鐘(B) | 差值(B-A) | |||
陰性對照 | 10 | 2.70±1.50 | 5.25±1.22 | 2.56±1.90 | |
低 | 13 | 3.23±1.20 | 5.68±1.42 | 2.45±1.57 | >0.05 |
中 | 14 | 2.90±1.01 | 5.15±1.14 | 2.25±1.12 | >0.05 |
高 | 13 | 2.91±0.82 | 5.60±1.43 | 2.69±1.49 | >0.05 |
組別 | 動物數(只) | 乳酸含量(毫摩爾/升) | P值* | ||
運動後(B) | 運動後0分鐘(C) | 差值(B-C) | |||
陰性對照 | 10 | 5.25±1.22 | 1.58±0.47 | 3.68±0.91 | |
低 | 13 | 5.68±1.42 | 1.83±0.97 | 3.85±1.24 | >0.05 |
中 | 14 | 5.15±1.14 | 1.92±0.43 | 3.23±1.14>0.05 | |
高 | 13 | 5.60±1.43 | 1.78±0.61 | 3.82±1.31 | >0.05 |
- 實施例49 20(R)-人參皂苷Rg3組合物膠囊劑改善記憶試驗
組別 | 劑量(毫克/千克) | n | 錯誤反應次數 |
正常對照組 | 12 | 0.37±0.22** | |
東莨菪鹼模型對照組 | 12 | 3.8±2.35 | |
憶恆顆粒對照組 | 121.65 | 12 | 0.96±0.73* |
Rg3組合物顆粒 | 2.16 | 12 | 0.88±0.69* |
6.48 | 12 | 0.70±0.36* | |
12.96 | 12 | 0.44±0.23** |
組別 | 劑量(毫克/千克) | n | 第2天 | 第3天 | 第4天 |
正常對照組 | 12 | 33.11±24.10 | 42.23±22.14 | 52.08±31.31 | |
東莨菪鹼模型對照組 | 12 | 8.75±7.21 | 13.45±8.74 | 26.582±6.52 | |
憶恆顆粒對照組 | 121.65 | 12 | 10.88±6.64 | 17.95±17.23 | 27.96±26.47 |
Rg3組合物顆粒 | 2.16 | 12 | 10.98±5.12 | 25.87±14.52 | 52.71+29.46 |
6.48 | 12 | 19.25±15.34 | 35.26±15.49 | 55.789±23.56 | |
12.96 | 12 | 27.98±17.68 | 59.80±26.41 | 61.58±34.64 |
- 實施例50 20(R)-人參皂苷Rg3組合物消腫止痛癒合傷口試驗
組數 | 例數 | 舔創面 | 所肢反應 | 抖動 |
生理對照組 | 10 | 1.30±1.50 | 0.70±1.11 | 5.30±3.16 |
雲南白藥組 | 10 | 9.00±2.16 | 9.40±2.59 | 10.70±1.33 |
Rg3組合物顆粒 | 10 | 11.20±0.92 | 11.40±0.84 | 10.40±1.43 |
組別 | 感染傷口數 | 未感染傷口數 | 合計 |
生理對照組 | 1 | 19 | 20 |
雲南白藥組 | 17 | 3 | 20 |
Rg3組合物顆粒 | 8 | 12 | 20 |

