黑姆荷茲自由能是Helmholtz free energy英文的音譯,也譯為亥姆霍茲自由能(在物理學中也常直接簡稱為自由能),是一個重要的熱力學參數,常用F或A表示,它的定義是:F=U-TS,其中U是系統的內能,T是溫度,S是熵。
基本介紹
- 中文名:黑姆荷茲自由能
- 外文名:Helmholtz free energy
- 別稱:亥姆霍茲自由能
- 意義:重要的熱力學參數
- 表示:F或A
- 定義:F=U-TS
簡介,表示方法,主要套用,
簡介
自由能可以被理解成是系統內能的一部分,這部分在可逆等溫過程中被轉化成功。在粒子數不變的等溫過程中,系統對外界所做的功一定只能小於或者等於其自由能的減少,也就是說,系統自由能的減少就是等溫過程中系統對外界所做的最大功。
表示方法
自由能常用F或A表示,其被定義為:
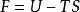
其中U是系統的內能,T是溫度,S是熵。
自由能的微分形式是:
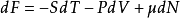
其中P是壓強,V是體積,μ是化學勢。
主要套用
某過程的自髮狀態及平衡條件的判斷
用熵增原理來判別一個過程的自發方向及平衡條件時,系統必須是隔離的,否則必須考慮環境的熵變。亦就是說,對非隔離系統,要判斷一個過程是否能夠進行,應該把系統和環境的總體看成一個新的隔離系統,並把系統的熵變和環境的熵變的總和計算出來,才能得到普遍性的熵判據。因為,通常反應總是在等溫、等溫等壓或等溫等容條件下的封閉系統內進行的,這時利用熵判據來判別過程的方向時,除了考慮系統的熵變,還得考慮環境的熵變,很不方便。為此亥姆霍茲(VonHelmholz H L P,1821~1984,德國人)和吉布斯(GibbsJ W,1839~1903,美國人)又定義了兩個狀態函式—亥姆霍茲自由能和吉布斯自由能。用這兩個輔助函式的變化值作判據,只考慮系統自身性質的變化便可達到目的,再無需考慮環境的影響了。

