鹽酸阿扎司瓊氯化鈉注射液,適應症為用於細胞毒類藥物化療引起的嘔吐。
基本介紹
- 藥品名稱:鹽酸阿扎司瓊氯化鈉注射液
- 藥品類型:處方藥
- 用途分類:5-HT3受體阻斷藥
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,
成份
本品主要成份為:鹽酸阿扎司瓊。
化學名稱:(±)N-(1-氮雜雙環[2,2,2]-3-辛基)-6-氯-3,4-二氫-4-甲基-3-氧代-2H-1,4-苯並噁嗪-8-甲醯胺單鹽酸鹽。
化學結構式:
化學名稱:(±)N-(1-氮雜雙環[2,2,2]-3-辛基)-6-氯-3,4-二氫-4-甲基-3-氧代-2H-1,4-苯並噁嗪-8-甲醯胺單鹽酸鹽。
化學結構式:
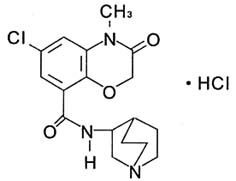
分子式:C17H20ClN303.HCl
分子量:386.28
輔料為氯化鈉。
性狀
本品為無色或幾乎無色的澄明液體。
適應症
用於細胞毒類藥物化療引起的嘔吐。
規格
100ml:鹽酸阿扎司瓊10mg與氯化鈉0.9g。
用法用量
每日一次10ml(一次1瓶),於化療前30分鐘靜脈滴注。
不良反應
部分病人出現口渴、便秘、頭痛、頭暈、腹部不適等。上述反應輕微,無須特殊處理。嚴重者曾有發生過過敏性休克的報導。故使用本品時應密切觀察病人的反應,如發生異常應立即停藥,並給予適當處理。
禁忌
1.對本類藥物(5-HT3受體阻斷劑)及本品過敏者禁用。
2.胃腸道梗阻者禁用。
2.胃腸道梗阻者禁用。
注意事項
本品遇光易分解,注意避光。
孕婦及哺乳期婦女用藥
1.孕婦除非必須外,不宜使用。
2.哺乳期婦女慎用,使用本品時應停止哺乳。
2.哺乳期婦女慎用,使用本品時應停止哺乳。
兒童用藥
尚未確定小兒用藥的安全性。
老年用藥
本品主要從腎臟排泄,由於高齡患者多見腎功能降低,會持續血中高濃度,並可能出現頭痛等副作用。因此應根據患者狀態給藥。出現副作用時應減量(例如5mg)。
藥物相互作用
1、本品與鹼性藥液(如呋喃苯胺酸、甲氨蝶呤、氟尿嘧啶、吡咯他尼等注射液)或鬼臼乙叉苷注射液配伍會發生渾濁或結晶析出。故不宜與上述藥物同時套用。
2、本品與氟氧頭孢鈉注射液配伍使用可能會使本品的含量降低,故應在配製後6小時內使用。
3、本品與地西泮注射液配伍會出現渾濁或產生沉澱,應避免與之配伍使用。
2、本品與氟氧頭孢鈉注射液配伍使用可能會使本品的含量降低,故應在配製後6小時內使用。
3、本品與地西泮注射液配伍會出現渾濁或產生沉澱,應避免與之配伍使用。
藥物過量
未進行該項試驗且無可靠參考文獻。
藥理毒理
1.藥理作用
鹽酸阿扎司瓊為選擇性5-HT3受體拮抗劑,對順鉑等抗癌藥引起的噁心及嘔吐有明顯抑制作用。動物研究表明,鹽酸阿扎司瓊對大鼠大腦皮質5-HT3受體親和力比甲氧氯普胺約強410倍,為恩丹西酮的2倍,與格拉司瓊基本相同。
2.毒理研究
重複給藥毒性:本品大鼠靜脈注射給藥,10mg/kg和60mg/kg組動物出現進食量和體重增加,可逆性的心臟、肝臟、腦和腎上腺重量加大。狗連續靜脈注射給藥3個月,劑量達30mg/kg時,給藥後即刻出現嘔吐和流涎等症狀。
生殖毒性:大鼠妊娠前及妊娠初期給藥劑量60mg/kg時,對母體動物的生殖功能及胎仔發育未見明顯影響。大鼠器官形成期靜脈注射劑量達100mg/kg時,出現胎盤重量(F1)減少及雄性新生鼠(F1)的腎臟及腎上腺重量增加,但對母體、胎仔(F1和F2)及新生鼠(F1)的發育和功能均未表現出明顯影響。家兔靜脈注射給藥劑量達0.3mg/kg時,出現母體動物攝食量減少,劑量達3.0mg/kg出現胎仔發育輕度抑制,達30mg/kg時出現胎仔死亡率輕度增加,但未出現致畸性。大鼠圍產期靜脈注射給藥達100mg/kg時,對母體動物無明顯影響,但雄性仔鼠出現肝臟重量稍減輕。動物研究結果已表明,本品可經大鼠乳汁分泌,故哺乳期婦女在本品用藥期間應中止授乳。
遺傳毒性:本品Ames試驗和小鼠微核試驗結果均為陰性,但體外培養細胞染色體畸變試驗結果出現染色體結構異常。
鹽酸阿扎司瓊為選擇性5-HT3受體拮抗劑,對順鉑等抗癌藥引起的噁心及嘔吐有明顯抑制作用。動物研究表明,鹽酸阿扎司瓊對大鼠大腦皮質5-HT3受體親和力比甲氧氯普胺約強410倍,為恩丹西酮的2倍,與格拉司瓊基本相同。
2.毒理研究
重複給藥毒性:本品大鼠靜脈注射給藥,10mg/kg和60mg/kg組動物出現進食量和體重增加,可逆性的心臟、肝臟、腦和腎上腺重量加大。狗連續靜脈注射給藥3個月,劑量達30mg/kg時,給藥後即刻出現嘔吐和流涎等症狀。
生殖毒性:大鼠妊娠前及妊娠初期給藥劑量60mg/kg時,對母體動物的生殖功能及胎仔發育未見明顯影響。大鼠器官形成期靜脈注射劑量達100mg/kg時,出現胎盤重量(F1)減少及雄性新生鼠(F1)的腎臟及腎上腺重量增加,但對母體、胎仔(F1和F2)及新生鼠(F1)的發育和功能均未表現出明顯影響。家兔靜脈注射給藥劑量達0.3mg/kg時,出現母體動物攝食量減少,劑量達3.0mg/kg出現胎仔發育輕度抑制,達30mg/kg時出現胎仔死亡率輕度增加,但未出現致畸性。大鼠圍產期靜脈注射給藥達100mg/kg時,對母體動物無明顯影響,但雄性仔鼠出現肝臟重量稍減輕。動物研究結果已表明,本品可經大鼠乳汁分泌,故哺乳期婦女在本品用藥期間應中止授乳。
遺傳毒性:本品Ames試驗和小鼠微核試驗結果均為陰性,但體外培養細胞染色體畸變試驗結果出現染色體結構異常。
藥代動力學
據文獻報導,健康男性志願者靜注本品10mg後,3分鐘的血漿中原型藥的濃度為190.5μg/ml,其藥動學是線性的。本品呈雙向消除,α相和β相的半衰期分別為0.13h和4.3h。對接受順鉑治療的惡性腫瘤患者,靜注本品10mg後,終末半衰期為7.3±1.2h,較健康人長。原型藥24h由尿排泄量為劑量的64.3±15%。
貯藏
遮光、密閉保存。
包裝
包裝材質為玻璃輸液瓶,100ml/瓶。
有效期
18個月。
執行標準
國家食品藥品監督管理局標準 YBH11782004。
