鹽酸格拉司瓊片,適應症為用於預防和治療由放療、細胞毒類藥物化療所致的噁心和嘔吐。
基本介紹
- 藥品名稱:鹽酸格拉司瓊片
- 藥品類型:處方藥、醫保工傷用藥
- 用途分類:5-HT3受體阻斷藥
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,
成份
本品主要成份為鹽酸格拉司瓊。
化學名稱:1-甲基-N-[9-甲基-橋-9-氮雜雙環(3,3,1)壬烷-3-基]-1H-吲唑-3-甲醯胺鹽酸鹽。
其結構式為:
分子式:C18H24N40·HCl
分子量:348.88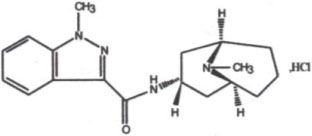
化學名稱:1-甲基-N-[9-甲基-橋-9-氮雜雙環(3,3,1)壬烷-3-基]-1H-吲唑-3-甲醯胺鹽酸鹽。
其結構式為:
分子式:C18H24N40·HCl
分子量:348.88

性狀
本品為白色或類白色片。
適應症
用於預防和治療由放療、細胞毒類藥物化療所致的噁心和嘔吐。
規格
1mg(以C18H24N4O計)
用法用量
口服。通常成人用量為1mg/次,2次/日,首次給藥於化療和放療前1小時服用,第二次於第一次服藥後12小時服用。老年人和肝、腎功能不全患者無需調整劑量。
日最大用量:24小時內不超過9 mg。
日最大用量:24小時內不超過9 mg。
不良反應
常見的不良反應僅為頭痛、便秘、無力、腹瀉、腹痛、消化不良,但多數為輕至中度,一般無需特殊處理。偶有過敏反應,個別較重(如過敏性休克)。其它過敏反應還包括出現輕微皮疹,臨床試驗中還發現肝轉氨酶一過性升高。
禁忌
1.對本品或有關化合物過敏者禁用。
2.胃腸道梗阻者禁用。
2.胃腸道梗阻者禁用。
注意事項
1.由於本品可減慢消化道運動,故消化道運動障礙患者,使用本品時應嚴密觀察。
2.高血壓未控制的患者,日劑量不宜超過10 mg,以免引起血壓進一步升高。
3.與食物同時服用時吸收略有延遲。
2.高血壓未控制的患者,日劑量不宜超過10 mg,以免引起血壓進一步升高。
3.與食物同時服用時吸收略有延遲。
孕婦及哺乳期婦女用藥
多個體外或體內評估試驗證實本藥對哺乳類動物細胞無遺傳毒性。動物試驗無致畸胎性。尚無孕婦使用本品經驗,也缺乏在母乳中分泌及排泄資料,因此,應當遵循以下原則:
1.孕婦除非必需外,不宜使用。
2.哺乳期婦女需慎用,若使用本品時應停止哺乳。
1.孕婦除非必需外,不宜使用。
2.哺乳期婦女需慎用,若使用本品時應停止哺乳。
兒童用藥
尚無兒童用藥經驗,不推薦使用。
老年用藥
老年人無需調整劑量。
藥物相互作用
對健康受試者研究表明,本品與西咪替丁或氯羥安定問沒有明顯的藥物相互作用。臨床研究中亦未觀察到明顯的藥物相互作用。
對已麻醉患者雖未進行特殊的藥物相互作用的研究,但常規劑量下本品與麻醉劑或與止痛劑合用是安全的。此外,對體外人微粒體研究表明本品對細胞色素P450的亞型3A4(參與一些主要的麻醉止痛藥物的代謝)的作用沒有影響。
與利福平或其他肝酶誘導藥物同時使用,本品血藥濃度減低,應適當增加劑量。
對已麻醉患者雖未進行特殊的藥物相互作用的研究,但常規劑量下本品與麻醉劑或與止痛劑合用是安全的。此外,對體外人微粒體研究表明本品對細胞色素P450的亞型3A4(參與一些主要的麻醉止痛藥物的代謝)的作用沒有影響。
與利福平或其他肝酶誘導藥物同時使用,本品血藥濃度減低,應適當增加劑量。
藥物過量
一例患者服用推薦劑量10倍之後,僅出現輕微頭痛,無其他後遺症報導。本品無特殊的解毒藥,假如服藥過量,應採取對症治療。
藥理毒理
藥理作用
本品是一種高選擇性的5HL3受體拮抗劑,對因放療、化療及手術引起的噁心和嘔吐具有良好的預防和治療作用。放療、化療及外科手術等因素可引起腸嗜鉻細胞釋放5HT,並激活中樞或迷走神經的5HT3受體而引起嘔吐反射。本品控制噁心和嘔吐的機理是通過拮抗中樞化學感受區及外周迷走神經末梢的5HT3受體,抑制噁心、嘔吐的發生。本品選擇性較高,無錐體外系反應和過度鎮靜等副作用。
毒理研究
遺傳毒性:本品Ames試驗、小鼠淋巴瘤細胞正向突變試驗、小鼠微核試驗及體內、外大鼠肝細胞程式外DNA合成(UDS)試驗結果均未表現出致突變作用,但在Hela細胞體外試驗中出現UDS明顯增加。體外人淋巴細胞染色體畸變試驗中可見多倍體細胞的數量明顯增加。
生殖毒性:經口給予本品劑量達100 mg/kg/天(600 mg/m[sup]2[/sup]/天,按體表面積算,相當於人用推薦劑量的405倍)時,對雌、雄大鼠的生育力和生殖行為無影響。妊娠的大鼠和家兔經口給予本品劑量分別為125 mg/kg/天(750 mg/m[sup]2[/sup]/天,按體表面積算,相當於人用推薦劑量的507倍)及32 mg/kg/天(378 mg/m[sup]2[/sup]/天,按體表面積算,相當於人用推薦劑量的255倍)時,均未表現出對動物生育力和胎兒發育的影響,但尚無本品充分和嚴格對照的妊娠婦女給藥的臨床研究。由於動物試驗並不總能預測藥物對人體的影響,故只有在確實必需時,才可在妊娠期間服用本品。
目前尚不清楚本品是否通過乳汁分泌。因為許多藥物可以經乳汁分泌,故哺乳婦女服用本品時應慎重考慮其對後代的影響。
致癌性:在給藥兩年的致癌性試驗中,大鼠經口給予本品的劑量分別為1、5、50 mg/kg(6、30、300 mg/m[sup]2[/sup]/天),其中高劑量組在第59周時因毒性反應將劑量降至25 mg/kg。結果顯示,5 mg/kg/天以上組(包括該劑量組)雄性大鼠和25 mg/kg/天組雌性大鼠(以體表面積計算,其劑量分別相當於人用推薦劑量的20倍以上和101倍)的肝細胞癌和腺瘤的發生率顯著增加,而1mg/kg組雄性大鼠和5 mg/kg組雌性大鼠(以體表面積算,分別為臨床推薦劑量的4倍和20倍)的肝腫瘤發生率未見增加。在12個月的試驗中,經口給予本品100 mg/kg/天組(600 mg/m[sup]2[/sup]/天,以體表面積計算,相當於人用推薦劑量的405倍)的雌、雄大鼠均發生肝細胞腺瘤,而空白對照組未出現。本品給藥24個月的小鼠致癌性試驗結果顯示,腫瘤的發生率未顯示明顯的統計學意義增加,但該試驗並非最後結論。由於在大鼠致癌性研究中出現腫瘤,故本品應在說明書所推薦的劑量下和適應症的範圍內套用。
本品是一種高選擇性的5HL3受體拮抗劑,對因放療、化療及手術引起的噁心和嘔吐具有良好的預防和治療作用。放療、化療及外科手術等因素可引起腸嗜鉻細胞釋放5HT,並激活中樞或迷走神經的5HT3受體而引起嘔吐反射。本品控制噁心和嘔吐的機理是通過拮抗中樞化學感受區及外周迷走神經末梢的5HT3受體,抑制噁心、嘔吐的發生。本品選擇性較高,無錐體外系反應和過度鎮靜等副作用。
毒理研究
遺傳毒性:本品Ames試驗、小鼠淋巴瘤細胞正向突變試驗、小鼠微核試驗及體內、外大鼠肝細胞程式外DNA合成(UDS)試驗結果均未表現出致突變作用,但在Hela細胞體外試驗中出現UDS明顯增加。體外人淋巴細胞染色體畸變試驗中可見多倍體細胞的數量明顯增加。
生殖毒性:經口給予本品劑量達100 mg/kg/天(600 mg/m[sup]2[/sup]/天,按體表面積算,相當於人用推薦劑量的405倍)時,對雌、雄大鼠的生育力和生殖行為無影響。妊娠的大鼠和家兔經口給予本品劑量分別為125 mg/kg/天(750 mg/m[sup]2[/sup]/天,按體表面積算,相當於人用推薦劑量的507倍)及32 mg/kg/天(378 mg/m[sup]2[/sup]/天,按體表面積算,相當於人用推薦劑量的255倍)時,均未表現出對動物生育力和胎兒發育的影響,但尚無本品充分和嚴格對照的妊娠婦女給藥的臨床研究。由於動物試驗並不總能預測藥物對人體的影響,故只有在確實必需時,才可在妊娠期間服用本品。
目前尚不清楚本品是否通過乳汁分泌。因為許多藥物可以經乳汁分泌,故哺乳婦女服用本品時應慎重考慮其對後代的影響。
致癌性:在給藥兩年的致癌性試驗中,大鼠經口給予本品的劑量分別為1、5、50 mg/kg(6、30、300 mg/m[sup]2[/sup]/天),其中高劑量組在第59周時因毒性反應將劑量降至25 mg/kg。結果顯示,5 mg/kg/天以上組(包括該劑量組)雄性大鼠和25 mg/kg/天組雌性大鼠(以體表面積計算,其劑量分別相當於人用推薦劑量的20倍以上和101倍)的肝細胞癌和腺瘤的發生率顯著增加,而1mg/kg組雄性大鼠和5 mg/kg組雌性大鼠(以體表面積算,分別為臨床推薦劑量的4倍和20倍)的肝腫瘤發生率未見增加。在12個月的試驗中,經口給予本品100 mg/kg/天組(600 mg/m[sup]2[/sup]/天,以體表面積計算,相當於人用推薦劑量的405倍)的雌、雄大鼠均發生肝細胞腺瘤,而空白對照組未出現。本品給藥24個月的小鼠致癌性試驗結果顯示,腫瘤的發生率未顯示明顯的統計學意義增加,但該試驗並非最後結論。由於在大鼠致癌性研究中出現腫瘤,故本品應在說明書所推薦的劑量下和適應症的範圍內套用。
藥代動力學
健康受試者單次空腹口服鹽酸格拉司瓊片1mg後,血漿峰濃度值約為3.63ng/ml,達峰時間約為1.180小時,虹漿清除半衰期為6.23小時,癌症患者半衰期顯著延長,為9.8-11.6小時。在體內廣泛分布,分布容積約3.94L/kg,服藥後48小時,大約12%的劑量以原形藥的形式在尿中排泄,餘下的劑量以代謝物的形式排泄,尿、糞排泄率分別為48%和38%。鹽酸格拉司瓊的代謝由肝微粒體酶P-4503A介導,主要代謝途徑為N-去甲基化及芳香環氧化後再與葡萄糖醛酸結合。血清蛋白結合率約為65%。
貯藏
遮光,密封保存。
包裝
鋁鋁包裝。2片/盒,4片/盒,8片/盒。
有效期
24個月。
執行標準
《中國藥典》2010年版二部。
