鹽酸度洛西汀腸溶膠囊,適應症為用於治療抑鬱症。
基本介紹
- 藥品名稱:鹽酸度洛西汀腸溶膠囊
- 藥品類型:處方藥、醫保工傷用藥
- 用途分類:其他抗抑鬱藥
警示語,成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,臨床試驗,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,
警示語
警告
兒童青少年的自殺—在兒童青少年抑鬱症和其他精神疾病中的短期研究提示,抗抑鬱藥增加自殺觀念和自殺行為(自殺)的風險,如果考慮在兒童青少年中使用度洛西汀或任何其他抗抑鬱藥,必須權衡這個風險與臨床需要。已經開始治療的患者,應密切觀察其是否有臨床症狀惡化、自殺或異常的行為改變。應該建議家庭成員及照料者加強對患者的密切觀察,並和處方醫生加強溝通。度洛西汀未被批准用於兒童患者(見警告和注意事項,兒童用藥)。
病情惡化和自殺風險—成年、兒童抑鬱症患者, 無論是否接受抗抑鬱藥物治療,都可能發生抑鬱症狀惡化和/或出現自殺觀念與自殺行為(自殺)或行為的異常改變,在病情顯著緩解前這種風險將持續存在。長期以來認為在某些特定人群中,抗抑鬱藥物可能會誘發抑鬱症狀惡化或導致自殺。在關於兒童青少年抑鬱症和其他精神疾病的短期臨床研究中,抗抑鬱藥增加自殺觀念和自殺行為(自殺)的風險。
綜合分析急性期安慰劑對照試驗(總計24個試驗包括4400例患者),9種抗抑鬱藥(SSRIs和其它抗抑鬱藥)治療兒童青少年抑鬱症、強迫症或其他精神障礙,結果顯示這些接受抗抑鬱藥治療的兒童青少年,在治療的前幾個月內,自殺觀念和自殺行為(自殺)這樣的不良事件風險明顯增加。在接受抗抑鬱藥治療的患者中,這些不良事件的平均風險為4%,是安慰劑治療者風險(2%)的兩倍。這些試驗中未發生自殺事件。藥物間的風險雖不相同,幾乎所有的藥物都可能增加這種風險。在對抑鬱症的試驗中觀察到的自殺風險極其相似,在其他精神疾病(強迫性障礙和社交焦慮障礙)中進行的一些臨床試驗也發現了風險增高的徵兆。這些臨床試驗中未發生自殺事件。目前不清楚是否兒童患者中的自殺風險持續至長期治療,如超過數月。也不清楚是否自殺風險波及成人。
因任何適應症接受抗抑鬱藥治療的兒童患者應當密切觀察是否有臨床症狀惡化、自殺或異常行為改變,尤其是在藥物治療的開始幾個月,或者是劑量改變時,如加藥或減藥。密切觀察包括:在開始治療的前4周內,至少每周一次與患者或其家人、或照料者的當面接觸;之後的4周每兩周接觸一次;治療12周時、以及12周以後如果臨床需要,和患者進行當面接觸。當面接觸期間,可能還需要另外的電話訪談。
接受抗抑鬱藥治療的成人抑鬱症患者,或共病抑鬱症和其他精神疾病者也同樣需要密切觀察,是否有臨床症狀惡化和自殺,尤其是在開始藥物治療的前幾個月,或者改變劑量時,如加量或減量。
抗抑鬱藥物在治療成年、兒童抑鬱症和其它適應症無論是精神病性或非精神病性障礙時,下列症狀均曾有報導:焦慮,興奮,驚恐發作,失眠,易怒,敵對(攻擊性),衝動,激越(精神運動性興奮),輕躁狂和躁狂。雖然尚未證實上述症狀的出現與抑鬱惡化和/或導致自殺之間存在因果關係,這些症狀可能是發生自殺的先兆。
當遇到抑鬱症狀持續惡化或出現自殺、或出現抑鬱惡化或自殺的前兆症狀,尤其當這些症狀非常嚴重、突然發生或出現了新症狀時,需考慮改變治療方案,包括可能終止治療。如果決定終止治療,藥物應儘可能快的逐漸減量,但是驟然停藥會出現一些症狀。(見注意事項,用法用量,終止度洛西汀治療風險的描述)。
使用抗抑鬱藥物治療的抑鬱症和其它適應症的兒童患者,包括精神病性和非精神病性障礙,患者的家人和照料者應該警惕,需要對監測患者出現的激越,易怒、行為異常改變、出現自殺以及上面提及的其他症狀進行監測,一旦出現這些症狀立即向衛生保健機構提供信息,這些監測也應包括家人或照料者的每日觀察。度洛西汀腸溶膠囊處方時應予以治療劑量的最小量,以減少過量的風險。接受抗抑鬱藥治療的成人,給其家人或照料者同樣的建議。
篩查雙相障礙患者—抑鬱發作可能是雙相障礙的早期表現。通常認為(雖然未經對照研究證實),單用抗抑鬱藥物治療抑鬱發作可能會增加雙相障礙患者的混合/躁狂發作。雖然無法預測會出現以上提及的哪一項症狀,但是,在抗抑鬱藥物治療前,應對抑鬱患者進行適當地篩查,確定是否患有雙相障礙的風險。篩查方法包括詳細地詢問精神病病史,有無自殺、雙相障礙和抑鬱的家族史。應注意度洛西汀尚未批准用於治療雙相抑鬱。
單胺氧化酶抑制劑(MAOI)—據報導,五羥色胺再攝取抑制劑與單胺氧化酶抑制劑合用時會出現嚴重的不良反應,例如,高熱、強直、肌陣攣、坐立不安,生命體徵迅速波動,精神狀況改變,包括極度興奮到譫妄、昏迷,嚴重時可致死。近期停用五羥色胺再攝取抑制劑,換用單胺氧化酶抑制劑時也可能出現上述反應。有時臨床表現與精神藥物導致的惡性綜合症的特徵類似。在人體和動物中未評價度洛西汀與單胺氧化酶抑制劑聯合套用的後果。因此,度洛西汀作為一種五羥色胺和去甲腎上腺素再攝取抑制劑,不推薦與單胺氧化酶抑制劑聯合使用,或者,一種單胺氧化酶抑制劑停用14天內不能使用度洛西汀。根據度洛西汀的半衰期考慮,在開始一種單胺氧化酶抑制劑治療前,度洛西汀至少停用5天。
兒童青少年的自殺—在兒童青少年抑鬱症和其他精神疾病中的短期研究提示,抗抑鬱藥增加自殺觀念和自殺行為(自殺)的風險,如果考慮在兒童青少年中使用度洛西汀或任何其他抗抑鬱藥,必須權衡這個風險與臨床需要。已經開始治療的患者,應密切觀察其是否有臨床症狀惡化、自殺或異常的行為改變。應該建議家庭成員及照料者加強對患者的密切觀察,並和處方醫生加強溝通。度洛西汀未被批准用於兒童患者(見警告和注意事項,兒童用藥)。
病情惡化和自殺風險—成年、兒童抑鬱症患者, 無論是否接受抗抑鬱藥物治療,都可能發生抑鬱症狀惡化和/或出現自殺觀念與自殺行為(自殺)或行為的異常改變,在病情顯著緩解前這種風險將持續存在。長期以來認為在某些特定人群中,抗抑鬱藥物可能會誘發抑鬱症狀惡化或導致自殺。在關於兒童青少年抑鬱症和其他精神疾病的短期臨床研究中,抗抑鬱藥增加自殺觀念和自殺行為(自殺)的風險。
綜合分析急性期安慰劑對照試驗(總計24個試驗包括4400例患者),9種抗抑鬱藥(SSRIs和其它抗抑鬱藥)治療兒童青少年抑鬱症、強迫症或其他精神障礙,結果顯示這些接受抗抑鬱藥治療的兒童青少年,在治療的前幾個月內,自殺觀念和自殺行為(自殺)這樣的不良事件風險明顯增加。在接受抗抑鬱藥治療的患者中,這些不良事件的平均風險為4%,是安慰劑治療者風險(2%)的兩倍。這些試驗中未發生自殺事件。藥物間的風險雖不相同,幾乎所有的藥物都可能增加這種風險。在對抑鬱症的試驗中觀察到的自殺風險極其相似,在其他精神疾病(強迫性障礙和社交焦慮障礙)中進行的一些臨床試驗也發現了風險增高的徵兆。這些臨床試驗中未發生自殺事件。目前不清楚是否兒童患者中的自殺風險持續至長期治療,如超過數月。也不清楚是否自殺風險波及成人。
因任何適應症接受抗抑鬱藥治療的兒童患者應當密切觀察是否有臨床症狀惡化、自殺或異常行為改變,尤其是在藥物治療的開始幾個月,或者是劑量改變時,如加藥或減藥。密切觀察包括:在開始治療的前4周內,至少每周一次與患者或其家人、或照料者的當面接觸;之後的4周每兩周接觸一次;治療12周時、以及12周以後如果臨床需要,和患者進行當面接觸。當面接觸期間,可能還需要另外的電話訪談。
接受抗抑鬱藥治療的成人抑鬱症患者,或共病抑鬱症和其他精神疾病者也同樣需要密切觀察,是否有臨床症狀惡化和自殺,尤其是在開始藥物治療的前幾個月,或者改變劑量時,如加量或減量。
抗抑鬱藥物在治療成年、兒童抑鬱症和其它適應症無論是精神病性或非精神病性障礙時,下列症狀均曾有報導:焦慮,興奮,驚恐發作,失眠,易怒,敵對(攻擊性),衝動,激越(精神運動性興奮),輕躁狂和躁狂。雖然尚未證實上述症狀的出現與抑鬱惡化和/或導致自殺之間存在因果關係,這些症狀可能是發生自殺的先兆。
當遇到抑鬱症狀持續惡化或出現自殺、或出現抑鬱惡化或自殺的前兆症狀,尤其當這些症狀非常嚴重、突然發生或出現了新症狀時,需考慮改變治療方案,包括可能終止治療。如果決定終止治療,藥物應儘可能快的逐漸減量,但是驟然停藥會出現一些症狀。(見注意事項,用法用量,終止度洛西汀治療風險的描述)。
使用抗抑鬱藥物治療的抑鬱症和其它適應症的兒童患者,包括精神病性和非精神病性障礙,患者的家人和照料者應該警惕,需要對監測患者出現的激越,易怒、行為異常改變、出現自殺以及上面提及的其他症狀進行監測,一旦出現這些症狀立即向衛生保健機構提供信息,這些監測也應包括家人或照料者的每日觀察。度洛西汀腸溶膠囊處方時應予以治療劑量的最小量,以減少過量的風險。接受抗抑鬱藥治療的成人,給其家人或照料者同樣的建議。
篩查雙相障礙患者—抑鬱發作可能是雙相障礙的早期表現。通常認為(雖然未經對照研究證實),單用抗抑鬱藥物治療抑鬱發作可能會增加雙相障礙患者的混合/躁狂發作。雖然無法預測會出現以上提及的哪一項症狀,但是,在抗抑鬱藥物治療前,應對抑鬱患者進行適當地篩查,確定是否患有雙相障礙的風險。篩查方法包括詳細地詢問精神病病史,有無自殺、雙相障礙和抑鬱的家族史。應注意度洛西汀尚未批准用於治療雙相抑鬱。
單胺氧化酶抑制劑(MAOI)—據報導,五羥色胺再攝取抑制劑與單胺氧化酶抑制劑合用時會出現嚴重的不良反應,例如,高熱、強直、肌陣攣、坐立不安,生命體徵迅速波動,精神狀況改變,包括極度興奮到譫妄、昏迷,嚴重時可致死。近期停用五羥色胺再攝取抑制劑,換用單胺氧化酶抑制劑時也可能出現上述反應。有時臨床表現與精神藥物導致的惡性綜合症的特徵類似。在人體和動物中未評價度洛西汀與單胺氧化酶抑制劑聯合套用的後果。因此,度洛西汀作為一種五羥色胺和去甲腎上腺素再攝取抑制劑,不推薦與單胺氧化酶抑制劑聯合使用,或者,一種單胺氧化酶抑制劑停用14天內不能使用度洛西汀。根據度洛西汀的半衰期考慮,在開始一種單胺氧化酶抑制劑治療前,度洛西汀至少停用5天。
成份
主要組成成分鹽酸度洛西汀。
化學名稱:(+)-(S)-N-甲基-γ-(1-萘基氧)-2-噻吩丙醇胺鹽酸鹽
化學結構式:
化學名稱:(+)-(S)-N-甲基-γ-(1-萘基氧)-2-噻吩丙醇胺鹽酸鹽
化學結構式:
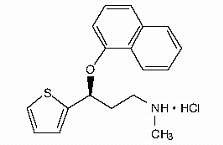
分子式:C18H19NOS·HCl
分子量:333.88
性狀
本品內容物為白色或類白色球狀腸溶顆粒。
30mg*膠囊:不透明白色囊體和藍色囊帽,囊體殼上印“30mg”。
60mg*膠囊:不透明綠色囊體和藍色囊帽,囊體殼上印“60mg”。
30mg*膠囊:不透明白色囊體和藍色囊帽,囊體殼上印“30mg”。
60mg*膠囊:不透明綠色囊體和藍色囊帽,囊體殼上印“60mg”。
適應症
用於治療抑鬱症。
規格
(1)30mg;(2)60mg(以度洛西汀計)。
用法用量
起始治療
推薦本品的起始劑量為40mg/日(20mg一日二次)至60mg/日(一日一次或30mg一日二次),不考慮進食情況。
現有的臨床研究數據未證實劑量超過60mg/日將增加療效。
維持/繼續/長期治療
一般認為抑鬱症的急性發作需要數月或更長時間的藥物治療,但尚沒有充足的試驗資料來確定患者應該連續服用度洛西汀治療達多長時間。對此類患者,應對其接受維持治療的必要性以及相應所需的劑量作定期評估。
特殊人群
腎臟功能受損患者的用量-對於晚期腎臟疾病(需要透析的)患者,或有嚴重腎臟功能損害(估計肌酐清除率<30 mL/min的)患者,建議不用本品(見藥理毒理)。
肝功能不全的患者的用量-建議有任何肝功能不全的患者避免服用本品(見藥理毒理 和 注意事項)
老年患者的用量-對於老年患者,建議不必根據年齡調整劑量。與任何藥物一樣,治療老年患者時應該慎重。在老年患者中個體化調整劑量時,增加劑量時應該額外小心。
對妊娠後三個月的女性患者的治療-在妊娠後三個月內接觸SSRIs或SNRIs(五羥色胺和去甲腎上腺素再攝取抑制劑)的新生兒,產生的併發症會導致住院時間延長、需要呼吸支持和管道餵食(見注意事項 )。當孕期女性用度洛西汀治療時,在妊娠後三個月,醫生應對治療的潛在風險和獲益進行認真的評價。醫生應考慮在妊娠晚期逐漸減度洛西汀的用量。
度洛西汀停藥
已有報導本品及其他SSRIs和SNRIs藥物的停藥反應(見注意事項)。停藥時應對這些症狀進行監測。建議儘可能的逐漸減藥,而不是驟停藥物。由於減少藥物劑量或停藥而引起了無法耐受的症狀時,可以考慮恢復使用以往的處方劑量。隨後再以更慢的速度減藥。
與單胺氧化酶抑制劑(MAOI)間的換藥
MAOI停藥後至少14天才可開始本品的治療。本品停藥後至少5天才可以開始MAOI的治療(見禁忌和警告)。
推薦本品的起始劑量為40mg/日(20mg一日二次)至60mg/日(一日一次或30mg一日二次),不考慮進食情況。
現有的臨床研究數據未證實劑量超過60mg/日將增加療效。
維持/繼續/長期治療
一般認為抑鬱症的急性發作需要數月或更長時間的藥物治療,但尚沒有充足的試驗資料來確定患者應該連續服用度洛西汀治療達多長時間。對此類患者,應對其接受維持治療的必要性以及相應所需的劑量作定期評估。
特殊人群
腎臟功能受損患者的用量-對於晚期腎臟疾病(需要透析的)患者,或有嚴重腎臟功能損害(估計肌酐清除率<30 mL/min的)患者,建議不用本品(見藥理毒理)。
肝功能不全的患者的用量-建議有任何肝功能不全的患者避免服用本品(見藥理毒理 和 注意事項)
老年患者的用量-對於老年患者,建議不必根據年齡調整劑量。與任何藥物一樣,治療老年患者時應該慎重。在老年患者中個體化調整劑量時,增加劑量時應該額外小心。
對妊娠後三個月的女性患者的治療-在妊娠後三個月內接觸SSRIs或SNRIs(五羥色胺和去甲腎上腺素再攝取抑制劑)的新生兒,產生的併發症會導致住院時間延長、需要呼吸支持和管道餵食(見注意事項 )。當孕期女性用度洛西汀治療時,在妊娠後三個月,醫生應對治療的潛在風險和獲益進行認真的評價。醫生應考慮在妊娠晚期逐漸減度洛西汀的用量。
度洛西汀停藥
已有報導本品及其他SSRIs和SNRIs藥物的停藥反應(見注意事項)。停藥時應對這些症狀進行監測。建議儘可能的逐漸減藥,而不是驟停藥物。由於減少藥物劑量或停藥而引起了無法耐受的症狀時,可以考慮恢復使用以往的處方劑量。隨後再以更慢的速度減藥。
與單胺氧化酶抑制劑(MAOI)間的換藥
MAOI停藥後至少14天才可開始本品的治療。本品停藥後至少5天才可以開始MAOI的治療(見禁忌和警告)。
不良反應
所有適應症的不良反應
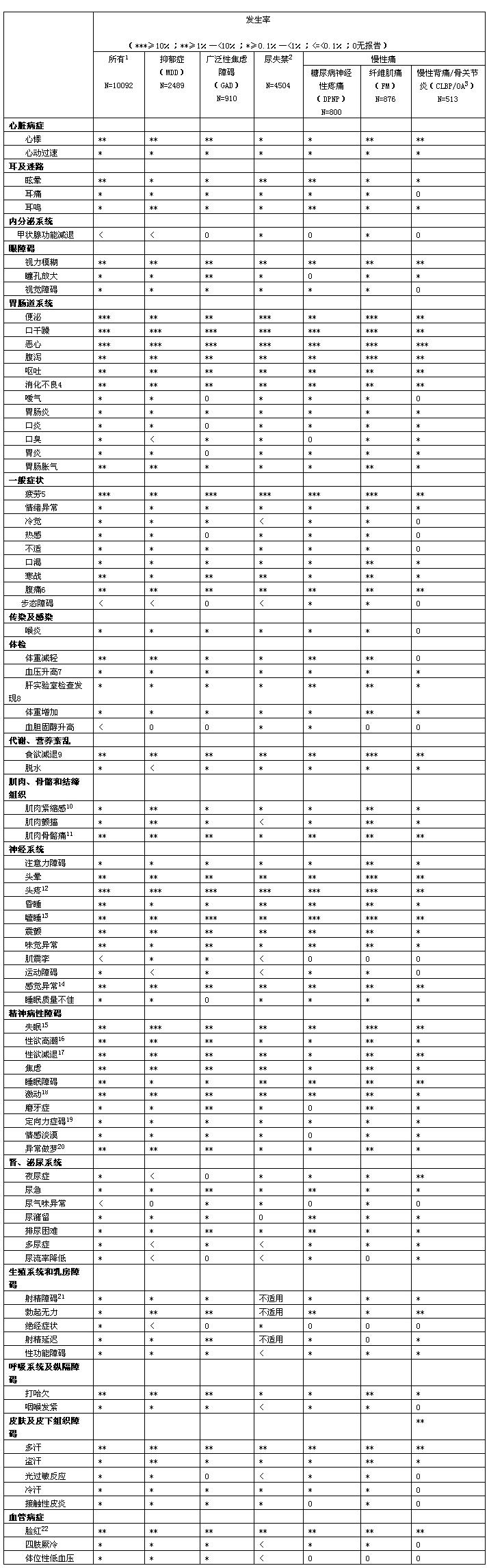
註解:1.此數據來源於2008年3月12日前安慰劑對照的資料庫,包括已批准的適應症及其它條件下已完成的臨床研究。2.包括應激性、急迫性、和混合性尿失禁。3.包括慢性背痛和骨關節炎。4.胃部不適。5.無力。6.上腹部疼痛、下腹部疼痛、腹部壓痛、腹部不適、胃腸道疼痛。7.收縮壓和舒張壓升高。8.谷丙轉氨酶升高、肝酶升高AST/GOT試驗升高、肝功能測試異常、g-氨基丁酸轉氨酶升高、血鹼性磷酸酶升高、血膽紅素升高。9.厭食症。10.肌肉骨骼僵硬。11.肌痛、頸痛。12.安慰劑組發生率大於度洛西汀組(僅限於抑鬱症)。13.睡眠過渡、鎮靜。14.包含感覺減退,面部感覺減退,口腔感覺異常。15.中段失眠、早醒、初段失眠。16.快感缺失。17.性慾缺乏。18.緊張不安感、坐立不安、緊張、精神運動性激越。19.意識模糊狀態。20.夢魘。21.射精失敗、射精異常。22.包括熱潮紅。
一般不良反應頭暈、噁心、頭疼,也見於度洛西汀停藥後,發生率≥ 5%。在安慰劑對照的臨床試驗中,度洛西汀治療伴隨小的ALT、AST、CPK從基線至終點平均值升高;與對照組相比,度洛西汀治療的病人可有罕見的、暫時的異常值。
血糖調整―在3項治療糖尿病性神經痛的臨床試驗中,平均糖尿病持續時間為12年,平均空腹血糖基線值為176mg/dL,平均血紅蛋白(HbA1c)基線值為7.81%。在這3項試驗的最初12周急性治療期,度洛西汀治療組病人的空腹血糖可見小幅升高。HbA1c在度洛西汀治療組和安慰劑對照組均穩定。在治療持續到52周時,度洛西汀治療組和安慰劑組均出現HbA1c升高,度洛西汀治療組平均增高值比安慰劑組高0.3%。儘管常規治療組病人顯示輕度降低,但空腹血糖和總膽固醇顯示小幅增高。
停藥後,有報告停藥後症狀,最常見報告的症狀包括下列臨床試驗中突然停服或逐漸停服度洛西汀,有頭暈、噁心、頭疼、感覺異常、疲勞、嘔吐、興奮、夢魘、失眠、腹瀉、焦慮、多汗和眩暈。
上市後使用度洛西汀治療出現的自發不良反應報告
下列不良反應發生率(<0.01%):
心臟疾患:室上性心律失常。
耳及迷路障礙:治療終止後耳鳴
內分泌失調:不良反應包括抗利尿激素分泌過多綜合症。
眼疾:青光眼。
肝膽管疾患:肝炎、黃膽。
免疫系統紊亂:過敏反應、超敏反應。
實驗室檢查:谷丙轉氨酶升高、鹼性磷酸酶升高、AST/GOT升高、膽紅素升高。
代謝、營養障礙:低鈉血症、高血糖(尤其是糖尿病病人)。
骨骼、結締組織疾病:牙關緊閉症。
神經系統障礙:錐體外系綜合症、不寧腿綜合徵、5-HT綜合症、癲癇發作、停藥後癲癇發作。
精神病性障礙:躁狂症、攻擊和發怒(尤其在治療早期或治療停止後)。
皮膚及皮下組織症狀:血管神經性水腫、暗傷、瘀斑、Stevens-Johnson綜合症、蕁麻疹。
血管病症:直立性低血壓(尤其在開始治療時)、暈厥(尤其在開始治療時)、高血壓危象。
生殖系統和乳腺障礙:婦產科出血。
下列不良反應發生率(≥0.01%-[0.1%):
精神病性障礙:幻覺。
腎、泌尿系統紊亂:尿瀦留。
皮膚及皮下組織症狀:皮疹。
禁忌
過敏
度洛西汀腸溶膠囊禁用於已知對度洛西汀腸溶膠囊或產品中任何非活性成分過敏的患者。
單胺氧化酶抑制劑
禁止與單胺氧化酶抑制劑(MAOIs)聯用。(見警告)
未經治療的窄角型青光眼
臨床試驗顯示,度洛西汀有增加瞳孔散大的風險,因此,未經治療的窄角型青光眼患者應避免使用度洛西汀。
度洛西汀腸溶膠囊禁用於已知對度洛西汀腸溶膠囊或產品中任何非活性成分過敏的患者。
單胺氧化酶抑制劑
禁止與單胺氧化酶抑制劑(MAOIs)聯用。(見警告)
未經治療的窄角型青光眼
臨床試驗顯示,度洛西汀有增加瞳孔散大的風險,因此,未經治療的窄角型青光眼患者應避免使用度洛西汀。
注意事項
一般注意事項
肝臟毒性-度洛西汀有增加血清轉氨酶水平的風險。肝臟轉氨酶升高導致0.4%(31/8454) 度洛西汀治療的患者中斷治療。這些患者出現轉氨酶升高的時間中位數為2個月。在抑鬱症患者中進行的對照試驗中,0.9%(8/930)用度洛西汀治療的患者ALT升高超過正常上限3倍以上,而安慰劑組中為0.3%(2/652)。所有安慰劑對照研究中,度洛西汀組中有1% (39/3732)的患者ALT升高超過正常上限3倍以上,而安慰劑組中為0.2%(6/2568)。固定劑量的安慰劑對照研究中,有證據顯示ALT升高超過正常上限3倍和AST升高超過正常上限5倍,與藥物劑量有量效關係。上市後監測還報導出現腹痛、肝腫大、伴有或無黃疸的轉氨酶升高超過正常值上限20倍的肝炎病例,反映了混合性或肝細胞性損傷,也有出現轉氨酶無明顯升高的膽汁鬱積型黃疸病例的報導。
在排除梗阻的情況下,通常認為轉氨酶升高伴有膽紅素升高,是嚴重肝臟損害的重要指標。國外臨床試驗中,3名服用度洛西汀的患者,出現轉氨酶、膽紅素和鹼性磷酸酶升高,提示存在梗阻情況。上述患者有嚴重的過度飲酒的情況,這可能是出現上述異常指標的原因所在。兩名安慰劑治療的患者也出現了轉氨酶、膽紅素升高的情況。上市後報告顯示轉氨酶、膽紅素和鹼性磷酸酶升高也可以發生在患有慢性肝病或肝硬化患者中。因為度洛西汀和酒精的相互作用可能引起肝損害或者加劇已有的肝病惡化,所以度洛西汀通常不用於有習慣性飲酒和慢性肝病患者的治療。
在臨床試驗過程中觀察到有些病人肝酶升高,這些現象通常是一過性的和自限性的,或者在停藥恢復。嚴重肝酶升高(>正常值上限的10倍)或肝損傷伴膽汁鬱積,或混合型肝病罕有報導,有些病例與酒精濫用或既往肝病有關。在酒精使用患者或既往有肝病史的患者中,度洛西汀應慎用。
對血壓的影響-與安慰劑相比,度洛西汀治療引起血壓升高,平均升高:收縮壓2 mm Hg, 舒張壓0.5 mm Hg ,偶爾有至少一次測量的收縮壓大於140 mm Hg。治療開始前應測量血壓,治療後應定期測量。(見不良反應 ,生命體徵變化)
轉為躁狂/輕躁狂-在MDD安慰劑對照試驗中,據報導,度洛西汀組中有0.1%(1/1139)的患者轉為躁狂/輕躁狂,安慰劑組為0.1% (1/777)。據報導,用其他已經上市對MDD有效藥物治療的一小部分患者轉為躁狂/輕躁狂。因此,與其他抗抑鬱藥一樣,既往有躁狂史的患者慎用度洛西汀。
癲癇-還未系統評價度洛西汀在癲癇障礙患者中的療效,這些患者從臨床試驗中排除了。在抑鬱症患者的安慰劑對照臨床試驗中,度洛西汀組中有0.1%(1/1139)的患者出現癲癇發作,而安慰劑組為0% (0/777)。既往有癲癇發作史的患者慎用度洛西汀。
治療已得到控制的窄角性青光眼-臨床試驗顯示,度洛西汀有增加瞳孔散大的風險,因此,度洛西汀慎用於已穩定的窄角型青光眼患者(見禁忌,禁用未經治療的閉角性青光眼)。
停藥-已對度洛西汀的停藥症狀做過系統研究。在抑鬱症患者中進行的為期9周的安慰劑對照試驗中,驟停藥物,觀察到度洛西汀治療的患者發生率 2%或明顯高於驟停安慰劑的症狀包括:頭暈,噁心,頭痛,感覺異常,疲勞、嘔吐,興奮、夢魘、失眠、腹瀉、焦慮、多汗和眩暈。
其他SSRIs 和SNRIs(五羥色胺和去甲腎上腺素再攝取抑制劑)上市以來,經常報導因為停用上述藥物而引起的藥物不良反應,尤其是驟停藥物後出現的,包括:惡劣心境,易怒,興奮,頭暈,感覺紊亂(感覺異常和電擊感),焦慮,意識模糊,頭痛,情感脆弱,乏力,失眠,輕躁狂,耳鳴,癲癇等等。雖然上述不良反應具有自限性,但有些很嚴重。
停用度洛西汀後應注意觀察患者有無上述症狀的出現。建議儘可能的逐漸減藥,而不是驟停藥物。由於減少藥物劑量或停藥而引起了無法耐受的症狀時,可以考慮套用以往的處方劑量。然後,臨床醫生再以一個更慢的速度減藥(見用法用量)。
患者合併軀體疾病-度洛西汀治療合併軀體疾病患者的臨床經驗有限。尚無胃動力改變對度洛西汀腸溶包衣的穩定性影響的資料。由於度洛西汀在酸性媒介中迅速水解成萘酚, 有胃排空減緩的患者注意避免使用度洛西汀(如一些糖尿病患者)。
度洛西汀還未在近期有心肌梗塞或不穩定性冠狀動脈疾病患者中進行系統評估。藥物上市前的臨床研究中,上述患者常作為排除者,未能進入研究中。不過,在MDD安慰劑對照試驗中,321名服度洛西汀患者的心電圖與基線時正常心電圖比較,度洛西汀不會增加有臨床意義的心電圖異常(見不良反應,心電圖改變)。
終末期腎病(需要透析)和嚴重腎功能不全(Cr清除率<30ml/min)患者使用度洛西汀其血藥濃度會增加,尤其是它的代謝產物。因此,不推薦終末期腎病患者使用度洛西汀 (見 藥理毒理和用法用量)。
肝功能不全患者使用度洛西汀其血藥濃度會明顯增加,因此不推薦此類患者服用度洛西汀(見藥理毒理和用法用量)。
患者信息
醫生和其他衛生專業人員應告知患者、家屬及照料者度洛西汀治療的獲益和風險,建議他們合理用藥。有給患者提供的"在兒童青少年中使用抗抑鬱藥的用藥指南",醫生和衛生專業人員應向患者、家屬或照料者介紹閱讀用藥指南,協助他們了解其中的內容。應當給患者討論用藥指南的機會,並能就患者提出的問題給出回答。本文結尾附著用藥指南的全文。
應當告誡患者注意以下問題,並且要求患者服用度洛西汀時,如果發生了這些問題,及時向醫生報告。
症狀惡化和自殺風險-患者、家屬及其照料者應當對下列問題提高警惕:焦慮、激越、驚恐發作、失眠、易怒、敵視、攻擊、衝動、靜坐不能(精神運動性不安)、輕躁狂、躁狂、行為異常改變、抑鬱加重、輕生觀念,尤其是在抗抑鬱藥治療早期,和上調或下調劑量時。由於這些改變常突然發生,應告誡患者家屬和照料者每天觀察這些症狀。應當向患者的醫生或衛生專業人員報告這些症狀,尤其是當這些症狀極其嚴重、突然發生、或不是患者平時的症狀表現時。可能導致自殺觀念和行為風險升高的這些症狀需要密切監測,甚至可能改變治療。
度洛西汀腸溶膠囊應整體吞服,既不能嚼碎或壓碎,也不能灑在食物上或混在飲料中,因為這樣有可能影響腸溶包衣。
任何精神活性藥物都會損害判斷力、思維或運動能力。儘管在對照研究中並未發現度洛西汀會損害精神運動表現、認知功能或記憶力,但由於度洛西汀的可能引起鎮靜作用和頭暈,在操作危險機械包括機動車應加以注意。除非患者能確定度洛西汀對其該方面的能力沒有影響。
由於藥物之間的相互作用,建議患者如果正在或計畫服用其他處方或非處方藥物時,要告知其醫生。
儘管度洛西汀並不增加酒精導致的精神和運動技能的損害,但度洛西汀伴隨大量的酒精攝入時會導致嚴重的肝損害。因此,對於大量酒精飲用的患者,通常不建議使用度洛西汀。
應提醒患者,如果在治療期間懷孕或準備懷孕,應當告知其醫生,處在哺乳期同樣如此。
在治療的1-4周內度洛西汀治療的抑鬱症患者的病情會改善,但要建議患者維持治療。
肝臟毒性-度洛西汀有增加血清轉氨酶水平的風險。肝臟轉氨酶升高導致0.4%(31/8454) 度洛西汀治療的患者中斷治療。這些患者出現轉氨酶升高的時間中位數為2個月。在抑鬱症患者中進行的對照試驗中,0.9%(8/930)用度洛西汀治療的患者ALT升高超過正常上限3倍以上,而安慰劑組中為0.3%(2/652)。所有安慰劑對照研究中,度洛西汀組中有1% (39/3732)的患者ALT升高超過正常上限3倍以上,而安慰劑組中為0.2%(6/2568)。固定劑量的安慰劑對照研究中,有證據顯示ALT升高超過正常上限3倍和AST升高超過正常上限5倍,與藥物劑量有量效關係。上市後監測還報導出現腹痛、肝腫大、伴有或無黃疸的轉氨酶升高超過正常值上限20倍的肝炎病例,反映了混合性或肝細胞性損傷,也有出現轉氨酶無明顯升高的膽汁鬱積型黃疸病例的報導。
在排除梗阻的情況下,通常認為轉氨酶升高伴有膽紅素升高,是嚴重肝臟損害的重要指標。國外臨床試驗中,3名服用度洛西汀的患者,出現轉氨酶、膽紅素和鹼性磷酸酶升高,提示存在梗阻情況。上述患者有嚴重的過度飲酒的情況,這可能是出現上述異常指標的原因所在。兩名安慰劑治療的患者也出現了轉氨酶、膽紅素升高的情況。上市後報告顯示轉氨酶、膽紅素和鹼性磷酸酶升高也可以發生在患有慢性肝病或肝硬化患者中。因為度洛西汀和酒精的相互作用可能引起肝損害或者加劇已有的肝病惡化,所以度洛西汀通常不用於有習慣性飲酒和慢性肝病患者的治療。
在臨床試驗過程中觀察到有些病人肝酶升高,這些現象通常是一過性的和自限性的,或者在停藥恢復。嚴重肝酶升高(>正常值上限的10倍)或肝損傷伴膽汁鬱積,或混合型肝病罕有報導,有些病例與酒精濫用或既往肝病有關。在酒精使用患者或既往有肝病史的患者中,度洛西汀應慎用。
對血壓的影響-與安慰劑相比,度洛西汀治療引起血壓升高,平均升高:收縮壓2 mm Hg, 舒張壓0.5 mm Hg ,偶爾有至少一次測量的收縮壓大於140 mm Hg。治療開始前應測量血壓,治療後應定期測量。(見不良反應 ,生命體徵變化)
轉為躁狂/輕躁狂-在MDD安慰劑對照試驗中,據報導,度洛西汀組中有0.1%(1/1139)的患者轉為躁狂/輕躁狂,安慰劑組為0.1% (1/777)。據報導,用其他已經上市對MDD有效藥物治療的一小部分患者轉為躁狂/輕躁狂。因此,與其他抗抑鬱藥一樣,既往有躁狂史的患者慎用度洛西汀。
癲癇-還未系統評價度洛西汀在癲癇障礙患者中的療效,這些患者從臨床試驗中排除了。在抑鬱症患者的安慰劑對照臨床試驗中,度洛西汀組中有0.1%(1/1139)的患者出現癲癇發作,而安慰劑組為0% (0/777)。既往有癲癇發作史的患者慎用度洛西汀。
治療已得到控制的窄角性青光眼-臨床試驗顯示,度洛西汀有增加瞳孔散大的風險,因此,度洛西汀慎用於已穩定的窄角型青光眼患者(見禁忌,禁用未經治療的閉角性青光眼)。
停藥-已對度洛西汀的停藥症狀做過系統研究。在抑鬱症患者中進行的為期9周的安慰劑對照試驗中,驟停藥物,觀察到度洛西汀治療的患者發生率 2%或明顯高於驟停安慰劑的症狀包括:頭暈,噁心,頭痛,感覺異常,疲勞、嘔吐,興奮、夢魘、失眠、腹瀉、焦慮、多汗和眩暈。
其他SSRIs 和SNRIs(五羥色胺和去甲腎上腺素再攝取抑制劑)上市以來,經常報導因為停用上述藥物而引起的藥物不良反應,尤其是驟停藥物後出現的,包括:惡劣心境,易怒,興奮,頭暈,感覺紊亂(感覺異常和電擊感),焦慮,意識模糊,頭痛,情感脆弱,乏力,失眠,輕躁狂,耳鳴,癲癇等等。雖然上述不良反應具有自限性,但有些很嚴重。
停用度洛西汀後應注意觀察患者有無上述症狀的出現。建議儘可能的逐漸減藥,而不是驟停藥物。由於減少藥物劑量或停藥而引起了無法耐受的症狀時,可以考慮套用以往的處方劑量。然後,臨床醫生再以一個更慢的速度減藥(見用法用量)。
患者合併軀體疾病-度洛西汀治療合併軀體疾病患者的臨床經驗有限。尚無胃動力改變對度洛西汀腸溶包衣的穩定性影響的資料。由於度洛西汀在酸性媒介中迅速水解成萘酚, 有胃排空減緩的患者注意避免使用度洛西汀(如一些糖尿病患者)。
度洛西汀還未在近期有心肌梗塞或不穩定性冠狀動脈疾病患者中進行系統評估。藥物上市前的臨床研究中,上述患者常作為排除者,未能進入研究中。不過,在MDD安慰劑對照試驗中,321名服度洛西汀患者的心電圖與基線時正常心電圖比較,度洛西汀不會增加有臨床意義的心電圖異常(見不良反應,心電圖改變)。
終末期腎病(需要透析)和嚴重腎功能不全(Cr清除率<30ml/min)患者使用度洛西汀其血藥濃度會增加,尤其是它的代謝產物。因此,不推薦終末期腎病患者使用度洛西汀 (見 藥理毒理和用法用量)。
肝功能不全患者使用度洛西汀其血藥濃度會明顯增加,因此不推薦此類患者服用度洛西汀(見藥理毒理和用法用量)。
患者信息
醫生和其他衛生專業人員應告知患者、家屬及照料者度洛西汀治療的獲益和風險,建議他們合理用藥。有給患者提供的"在兒童青少年中使用抗抑鬱藥的用藥指南",醫生和衛生專業人員應向患者、家屬或照料者介紹閱讀用藥指南,協助他們了解其中的內容。應當給患者討論用藥指南的機會,並能就患者提出的問題給出回答。本文結尾附著用藥指南的全文。
應當告誡患者注意以下問題,並且要求患者服用度洛西汀時,如果發生了這些問題,及時向醫生報告。
症狀惡化和自殺風險-患者、家屬及其照料者應當對下列問題提高警惕:焦慮、激越、驚恐發作、失眠、易怒、敵視、攻擊、衝動、靜坐不能(精神運動性不安)、輕躁狂、躁狂、行為異常改變、抑鬱加重、輕生觀念,尤其是在抗抑鬱藥治療早期,和上調或下調劑量時。由於這些改變常突然發生,應告誡患者家屬和照料者每天觀察這些症狀。應當向患者的醫生或衛生專業人員報告這些症狀,尤其是當這些症狀極其嚴重、突然發生、或不是患者平時的症狀表現時。可能導致自殺觀念和行為風險升高的這些症狀需要密切監測,甚至可能改變治療。
度洛西汀腸溶膠囊應整體吞服,既不能嚼碎或壓碎,也不能灑在食物上或混在飲料中,因為這樣有可能影響腸溶包衣。
任何精神活性藥物都會損害判斷力、思維或運動能力。儘管在對照研究中並未發現度洛西汀會損害精神運動表現、認知功能或記憶力,但由於度洛西汀的可能引起鎮靜作用和頭暈,在操作危險機械包括機動車應加以注意。除非患者能確定度洛西汀對其該方面的能力沒有影響。
由於藥物之間的相互作用,建議患者如果正在或計畫服用其他處方或非處方藥物時,要告知其醫生。
儘管度洛西汀並不增加酒精導致的精神和運動技能的損害,但度洛西汀伴隨大量的酒精攝入時會導致嚴重的肝損害。因此,對於大量酒精飲用的患者,通常不建議使用度洛西汀。
應提醒患者,如果在治療期間懷孕或準備懷孕,應當告知其醫生,處在哺乳期同樣如此。
在治療的1-4周內度洛西汀治療的抑鬱症患者的病情會改善,但要建議患者維持治療。
孕婦及哺乳期婦女用藥
妊娠:
妊娠分類C-在動物生殖研究中,發現度洛西汀對胚胎/胎兒和出生後的發育有不良影響。
大鼠和家兔在胚胎的器官發生期口服度洛西汀,劑量達45mg/kg/日時(大鼠劑量為7倍於[MRHD,60mg/kg/日],4倍於按照體重/體表面積指數計算的人體劑量120mg/日;家兔的劑量為15倍於[MRHD],7倍於按照體重/體表面積指數計算的人體劑量120mg/日),未發現有致畸作用。這個劑量時,胎兒體重降低。無效應劑量為10mg/kg/日(在大鼠為2倍於[MRHD],約1倍於按照體重/體表面積指數計算的人體劑量120mg/日;家兔的劑量為3倍於[MRHD],約2倍於按照體重/體表面積指數計算的人體劑量120mg/日)。
妊娠大鼠在整個孕期和哺乳期予以口服度洛西汀,在劑量30 mg/kg/日時(5倍於[MRHD],2倍於按照體重/體表面積指數mg/m2計算的人體劑量120mg/日),幼兒出生後存活1天、出生時和哺乳期的體重下降;無效應劑量為10 mg/kg/日。而且,母體使用度洛西汀的劑量達到30 mg/kg/日時,幼兒的行為表現與反應性的增高一致,如對噪音的驚詫反應增強,自主活動的習慣性降低。但母體使用度洛西汀對子代斷奶後的生長和生殖行為沒有負面影響。
由於缺乏足夠的、設計良好的孕期女性對照研究,因此,只有在權衡對胎兒潛在的受益超過風險時,才考慮在母孕期使用度洛西汀。近期服用度洛西汀的母親,其新生兒可能發生如下停藥症狀,包括肌張力下降、震顫、緊張不安、餵養困難、呼吸窘迫和癲癇發作。
非致畸效應-新生兒在妊娠中期三個月暴露於SSRIs或SNRIs(五羥色胺和去甲腎上腺素再攝取抑制劑)後,產生的併發症會導致住院時間延長、需要呼吸支持和管道餵食。這些併發症在出生後會立刻發生。已有的臨床發現包括呼吸窘迫、紫紺、呼吸暫停、癲癇發作和體溫不穩、餵養困難、嘔吐、低血糖症、肌張力不全、肌張力增高、反射亢進、震顫、反應過度、易怒、哭鬧不止。這些情況或者是SSRIs 和 SNRIs的直接毒性作用所致或者可能是藥物的戒斷反應。應當注意的是,在某些病例中,其臨床表現與五羥色胺綜合徵一致(見警告,單胺氧化酶抑制劑)。當妊娠女性在妊娠晚期三個月接受度洛西汀治療時,醫生應對治療的潛在風險和獲益進行認真地評價(見用法用量)。
分娩:
度洛西汀對於人類分娩的影響尚不明確。因此,只有證實度洛西汀對於胎兒的潛在獲益超過風險時才考慮在分娩期套用。
哺乳:
度洛西汀可通過哺乳期婦女乳汁分泌。估計嬰兒得到的日劑量大約為母親服藥劑量的0.14%(mg/kg)。由於度洛西汀對嬰兒的作用不明,因此服用度洛西汀的病人不推薦母乳餵養。
妊娠分類C-在動物生殖研究中,發現度洛西汀對胚胎/胎兒和出生後的發育有不良影響。
大鼠和家兔在胚胎的器官發生期口服度洛西汀,劑量達45mg/kg/日時(大鼠劑量為7倍於[MRHD,60mg/kg/日],4倍於按照體重/體表面積指數計算的人體劑量120mg/日;家兔的劑量為15倍於[MRHD],7倍於按照體重/體表面積指數計算的人體劑量120mg/日),未發現有致畸作用。這個劑量時,胎兒體重降低。無效應劑量為10mg/kg/日(在大鼠為2倍於[MRHD],約1倍於按照體重/體表面積指數計算的人體劑量120mg/日;家兔的劑量為3倍於[MRHD],約2倍於按照體重/體表面積指數計算的人體劑量120mg/日)。
妊娠大鼠在整個孕期和哺乳期予以口服度洛西汀,在劑量30 mg/kg/日時(5倍於[MRHD],2倍於按照體重/體表面積指數mg/m2計算的人體劑量120mg/日),幼兒出生後存活1天、出生時和哺乳期的體重下降;無效應劑量為10 mg/kg/日。而且,母體使用度洛西汀的劑量達到30 mg/kg/日時,幼兒的行為表現與反應性的增高一致,如對噪音的驚詫反應增強,自主活動的習慣性降低。但母體使用度洛西汀對子代斷奶後的生長和生殖行為沒有負面影響。
由於缺乏足夠的、設計良好的孕期女性對照研究,因此,只有在權衡對胎兒潛在的受益超過風險時,才考慮在母孕期使用度洛西汀。近期服用度洛西汀的母親,其新生兒可能發生如下停藥症狀,包括肌張力下降、震顫、緊張不安、餵養困難、呼吸窘迫和癲癇發作。
非致畸效應-新生兒在妊娠中期三個月暴露於SSRIs或SNRIs(五羥色胺和去甲腎上腺素再攝取抑制劑)後,產生的併發症會導致住院時間延長、需要呼吸支持和管道餵食。這些併發症在出生後會立刻發生。已有的臨床發現包括呼吸窘迫、紫紺、呼吸暫停、癲癇發作和體溫不穩、餵養困難、嘔吐、低血糖症、肌張力不全、肌張力增高、反射亢進、震顫、反應過度、易怒、哭鬧不止。這些情況或者是SSRIs 和 SNRIs的直接毒性作用所致或者可能是藥物的戒斷反應。應當注意的是,在某些病例中,其臨床表現與五羥色胺綜合徵一致(見警告,單胺氧化酶抑制劑)。當妊娠女性在妊娠晚期三個月接受度洛西汀治療時,醫生應對治療的潛在風險和獲益進行認真地評價(見用法用量)。
分娩:
度洛西汀對於人類分娩的影響尚不明確。因此,只有證實度洛西汀對於胎兒的潛在獲益超過風險時才考慮在分娩期套用。
哺乳:
度洛西汀可通過哺乳期婦女乳汁分泌。估計嬰兒得到的日劑量大約為母親服藥劑量的0.14%(mg/kg)。由於度洛西汀對嬰兒的作用不明,因此服用度洛西汀的病人不推薦母乳餵養。
兒童用藥
對於兒童患者的療效和安全性尚不清楚(見警告)。如果考慮在兒童青少年中使用度洛西汀,必須權衡潛在的風險和臨床需要。
老年用藥
在度洛西汀治療抑鬱症(MDD)臨床研究的2418例患者中,5.9%(143)為65歲以上年齡的患者。這些患者和年輕患者間未觀察到安全性和療效方面的顯著差異,其他臨床方面的報告也沒有發現老年人群和年輕人之間的明顯差異,但不能排除某些老年患者的敏感性增高。
藥物相互作用
可能影響度洛西汀的其他藥物
度洛西汀的代謝與CYP1A2和CYP2D6有關
CYP1A2抑制劑-度洛西汀與氟伏沙明(強CYP1A2抑制劑)聯合套用於男性受試者(n=14)時,度洛西汀 AUC增加超過5倍,Cmax增加約2.5倍,T1/2增加約3倍。其他對CYP1A2代謝有抑制作用的藥物包括:西米替丁,喹諾酮類抗生素例如環丙沙星, 依諾沙星。
CYP2D6抑制劑-由於CYP2D6參與度洛西汀的代謝,所以合併使用度洛西汀和強CYP2D6抑制劑時,鹽酸度洛西汀的藥物濃度將會增加,(見[注意事項]項下藥物相互作用)。
度洛西汀可能影響的其他藥物
通過CYP1A2代謝的藥物-體外藥物相互作用研究顯示:度洛西汀對CYP1A2活性無誘導作用。因此,雖然未進行有關酶誘導作用的臨床研究,預計不會因為酶誘導作用而使CYP1A2底物(例如茶鹼、咖啡因)的代謝增加。雖然體外研究顯示度洛西汀是CYP1A2抑制劑,但是度洛西汀(60 mg 每日兩次給藥)與作為CYP1A2底物的茶鹼聯合使用時,茶鹼的藥代動力學沒有明顯變化。因此,度洛西汀對CYP1A2底物的代謝不可能產生具有臨床意義的明顯影響。
通過CYP2D6代謝的藥物-度洛西汀是CYP2D6中度抑制劑,能夠增加經CYP2D6代謝藥物的AUC和Cmax。(見[注意事項])。因而聯合使用度洛西汀和其他主要經該酶代謝,並且治療劑量範圍狹窄的藥物時,應該謹慎(見[注意事項]項下藥物相互作用)。
通過CYP2C9代謝的藥物-體外研究顯示度洛西汀對CYP2C9酶的活性無抑制作用。因而,雖然未進行相關的臨床研究,預計度洛西汀對CYP2C9酶底物的代謝無抑制作用。
通過CYP3A代謝的藥物-體外研究結果顯示度洛西汀對CYP3A酶的活性無抑制或誘導作用。因而,雖然未進行相關的臨床研究,預計CYP3A酶底物(例如口服避孕藥和其他甾體藥物)不會因為酶誘導或抑制而產生代謝增強或抑制。
通過CYP2C19代謝的藥物-體外研究結果顯示治療濃度的度洛西汀對CYP2C19酶活性無抑制作用。因而,雖然未進行相關的臨床研究,預計度洛西汀對CYP2C19酶底物的代謝無抑制作用。
聯合套用苯二氮卓類藥物的研究
勞拉西泮-穩態濃度的度洛西汀(60mg Q 12 hrs)與勞拉西泮(2mg Q 12hrs)合用時,勞拉西泮的藥代動力學不受聯合治療的影響。
替馬西泮-穩態濃度的度洛西汀(20mg qhs)與替馬西泮 (30mg qhs)合用時,替馬西泮的藥代動力學不受聯合治療的影響。
高血漿蛋白結合的藥物-因為度洛西汀與血漿蛋白高度結合,正接受其他高血漿蛋白結合藥物治療的患者,服用度洛西汀時,可能會增加其他藥物的游離濃度,由此可能導致發生藥物不良反應。
中樞神經系統藥物—當度洛西汀與其它中樞作用類藥物合用時,尤其與那些作用機理類似的藥物合用(包括酒精),應慎用。與5-羥色胺能藥物合用(e.g.SNRIs,選擇性5-羥色胺再吸收抑制劑,阿米替林,曲馬多)可引起5-HT綜合症。
度洛西汀的代謝與CYP1A2和CYP2D6有關
CYP1A2抑制劑-度洛西汀與氟伏沙明(強CYP1A2抑制劑)聯合套用於男性受試者(n=14)時,度洛西汀 AUC增加超過5倍,Cmax增加約2.5倍,T1/2增加約3倍。其他對CYP1A2代謝有抑制作用的藥物包括:西米替丁,喹諾酮類抗生素例如環丙沙星, 依諾沙星。
CYP2D6抑制劑-由於CYP2D6參與度洛西汀的代謝,所以合併使用度洛西汀和強CYP2D6抑制劑時,鹽酸度洛西汀的藥物濃度將會增加,(見[注意事項]項下藥物相互作用)。
度洛西汀可能影響的其他藥物
通過CYP1A2代謝的藥物-體外藥物相互作用研究顯示:度洛西汀對CYP1A2活性無誘導作用。因此,雖然未進行有關酶誘導作用的臨床研究,預計不會因為酶誘導作用而使CYP1A2底物(例如茶鹼、咖啡因)的代謝增加。雖然體外研究顯示度洛西汀是CYP1A2抑制劑,但是度洛西汀(60 mg 每日兩次給藥)與作為CYP1A2底物的茶鹼聯合使用時,茶鹼的藥代動力學沒有明顯變化。因此,度洛西汀對CYP1A2底物的代謝不可能產生具有臨床意義的明顯影響。
通過CYP2D6代謝的藥物-度洛西汀是CYP2D6中度抑制劑,能夠增加經CYP2D6代謝藥物的AUC和Cmax。(見[注意事項])。因而聯合使用度洛西汀和其他主要經該酶代謝,並且治療劑量範圍狹窄的藥物時,應該謹慎(見[注意事項]項下藥物相互作用)。
通過CYP2C9代謝的藥物-體外研究顯示度洛西汀對CYP2C9酶的活性無抑制作用。因而,雖然未進行相關的臨床研究,預計度洛西汀對CYP2C9酶底物的代謝無抑制作用。
通過CYP3A代謝的藥物-體外研究結果顯示度洛西汀對CYP3A酶的活性無抑制或誘導作用。因而,雖然未進行相關的臨床研究,預計CYP3A酶底物(例如口服避孕藥和其他甾體藥物)不會因為酶誘導或抑制而產生代謝增強或抑制。
通過CYP2C19代謝的藥物-體外研究結果顯示治療濃度的度洛西汀對CYP2C19酶活性無抑制作用。因而,雖然未進行相關的臨床研究,預計度洛西汀對CYP2C19酶底物的代謝無抑制作用。
聯合套用苯二氮卓類藥物的研究
勞拉西泮-穩態濃度的度洛西汀(60mg Q 12 hrs)與勞拉西泮(2mg Q 12hrs)合用時,勞拉西泮的藥代動力學不受聯合治療的影響。
替馬西泮-穩態濃度的度洛西汀(20mg qhs)與替馬西泮 (30mg qhs)合用時,替馬西泮的藥代動力學不受聯合治療的影響。
高血漿蛋白結合的藥物-因為度洛西汀與血漿蛋白高度結合,正接受其他高血漿蛋白結合藥物治療的患者,服用度洛西汀時,可能會增加其他藥物的游離濃度,由此可能導致發生藥物不良反應。
中樞神經系統藥物—當度洛西汀與其它中樞作用類藥物合用時,尤其與那些作用機理類似的藥物合用(包括酒精),應慎用。與5-羥色胺能藥物合用(e.g.SNRIs,選擇性5-羥色胺再吸收抑制劑,阿米替林,曲馬多)可引起5-HT綜合症。
藥物過量
臨床試驗中迅速吞下3000mg,單獨或與其它藥物一起,未報導有致死性事件發生。然而,上市後有急性藥物過量致死的報告,主要是混合性藥物過量,也有單獨服用度洛西汀約1000mg的。過量的體徵和症狀(單獨服用度洛西汀或與其它藥物混合服用)包括瞌睡、昏迷、血清素綜合症、癲癇發作、嘔吐和心動過速。
藥物過量的處理
度洛西汀無特異拮抗劑,如發生血清素綜合症,要考慮特異療法(如:抗組胺藥和/或溫度控制)。
保持氣道通暢、吸氧和通風,監測心率和生命體徵,不推薦催吐,對服藥不久或仍有症狀者如需要可在適當氣道保護下插大孔胃管。
活性炭可用於減少度洛西汀在胃腸道吸收,已有研究顯示活性炭可以減少AUC和Cmax,,減少幅度約1/3。由於本品分布容積大,強制利尿、透析、輸血、交換輸液效果不明顯。
處理藥物過量時應考慮可能服用多種藥物,特別注意正在或最近服用度洛西汀的患者攝入過量TCA,這類患者的三環類及其活性代謝產物累積可能加重臨床症狀,需要延長密切觀察時間(見注意事項,藥物相互作用)。如有治療藥物過量之外的表現,醫生應考慮與中毒控制中心聯繫醫生手冊中列有註冊中毒控制中心的聯繫電話。
藥物過量的處理
度洛西汀無特異拮抗劑,如發生血清素綜合症,要考慮特異療法(如:抗組胺藥和/或溫度控制)。
保持氣道通暢、吸氧和通風,監測心率和生命體徵,不推薦催吐,對服藥不久或仍有症狀者如需要可在適當氣道保護下插大孔胃管。
活性炭可用於減少度洛西汀在胃腸道吸收,已有研究顯示活性炭可以減少AUC和Cmax,,減少幅度約1/3。由於本品分布容積大,強制利尿、透析、輸血、交換輸液效果不明顯。
處理藥物過量時應考慮可能服用多種藥物,特別注意正在或最近服用度洛西汀的患者攝入過量TCA,這類患者的三環類及其活性代謝產物累積可能加重臨床症狀,需要延長密切觀察時間(見注意事項,藥物相互作用)。如有治療藥物過量之外的表現,醫生應考慮與中毒控制中心聯繫醫生手冊中列有註冊中毒控制中心的聯繫電話。
臨床試驗
4個隨機、雙盲、安慰劑對照、固定劑量的臨床研究評估了本品治療抑鬱障礙的療效。入組對象為成年門診病人,年齡18-83歲,均符合DSM-IV關於重度抑鬱障礙的診斷標準。在其中2項研究中,患者被隨機分入鹽酸度洛西汀膠囊組60mg每日一次(分別為123例和128例)或安慰劑組(分別為122例和139例)治療9周;第3項研究中,患者被隨機分入鹽酸度洛西汀膠囊組20mg或40mg每日二次(分別為86 例和91例)或安慰劑組(89例)治療8周;第4項研究中,患者被隨機分入鹽酸度洛西汀膠囊組40mg或60mg每日二次(分別為95例和93例)或安慰劑組(93例)治療8周。沒有證據表明鹽酸度洛西汀膠囊日劑量超過60mg時有更多益處。
在上述4項研究中,本品在改善HAMD17項因子總分方面優於安慰劑組。
分析年齡、性別、種族等人口學特性與治療結果的相關性,未發現因為上述人口學特性的差異而有不同療效。
在上述4項研究中,本品在改善HAMD17項因子總分方面優於安慰劑組。
分析年齡、性別、種族等人口學特性與治療結果的相關性,未發現因為上述人口學特性的差異而有不同療效。
藥理毒理
藥理作用
度洛西汀是一種選擇性的5-羥色胺與去甲腎上腺素再攝取抑制劑(SSNRI)。度洛西汀抗抑鬱與中樞鎮痛作用的確切機制尚未明確,但認為與其增強中樞神經系統5-羥色胺能與去甲腎上腺素能功能有關。臨床前研究結果顯示,度洛西汀是神經元5-羥色胺與去甲腎上腺素再攝取的強抑制劑,對多巴胺再攝取的抑制作用相對較弱。體外研究結果顯示,度洛西汀與多巴胺能受體、腎上腺素能受體、膽鹼能受體、組胺能受體、阿片受體、谷氨酸受體、GABA受體無明顯親和力。度洛西汀不抑制單胺氧化酶。
毒理研究
遺傳毒性:
度洛西汀Ames試驗、小鼠淋巴瘤細胞正向基因突變試驗、大鼠肝細胞程式外DNA合成(UDS)試驗、中國倉鼠骨髓細胞姊妹染色單體交換試驗、小鼠微核試驗結果均為陰性。
生殖毒性:
雌性或雄性大鼠在交配前和交配中經口給予度洛西汀劑量達45mg/kg/天(根據mg/m2推算,相對於人最大推薦劑量60 mg/天[MRHD]的7倍),未見對交配或生育力的影響。
大鼠和家兔致畸敏感期經口給予度洛西汀達45mg/kg/天(根據mg/m2推算,大鼠和家兔分別相當於MRHD的7倍和15倍),可見胎仔體重降低,未見致畸作用。無影響劑量為10mg/kg/天(根據mg/m2推算,大鼠和家兔分別相當於MRHD的2倍和3倍)。
大鼠圍產期經口給予度洛西汀30 mg/kg/天(根據mg/m2推算,大鼠相當於MRHD的5倍)時,幼仔出生後1天存活率、出生時和哺乳期體重下降,無影響劑量為10 mg/kg/天。在劑量為30 mg/kg/天時,幼仔出現行為改變,表現為反應性增高,如對噪音驚嚇反應增強、自主活動減少。子代斷奶後的生長和生殖行為未見不良影響。
致癌性:
大鼠和小鼠摻食法給予度洛西汀2年。雌性小鼠在度洛西汀劑量為140mg/kg/天(根據mg/m2推算,相當於MRHD的11倍)時,可見肝細胞腺瘤和肝細胞癌的發生率增加,無影響劑量為50mg/kg/天(根據mg/m2推算,相當於MRHD的4倍)。雄性小鼠在度洛西汀劑量為100mg/kg/天(根據mg/m2推算,相當於MRHD的8倍)時,未見腫瘤發生率增加。雌性大鼠和雄性大鼠在劑量分別為27和36mg/kg/天(根據mg/m2推算,分別相當於MRHD的4和6倍)時,未見腫瘤發生率增加。
度洛西汀是一種選擇性的5-羥色胺與去甲腎上腺素再攝取抑制劑(SSNRI)。度洛西汀抗抑鬱與中樞鎮痛作用的確切機制尚未明確,但認為與其增強中樞神經系統5-羥色胺能與去甲腎上腺素能功能有關。臨床前研究結果顯示,度洛西汀是神經元5-羥色胺與去甲腎上腺素再攝取的強抑制劑,對多巴胺再攝取的抑制作用相對較弱。體外研究結果顯示,度洛西汀與多巴胺能受體、腎上腺素能受體、膽鹼能受體、組胺能受體、阿片受體、谷氨酸受體、GABA受體無明顯親和力。度洛西汀不抑制單胺氧化酶。
毒理研究
遺傳毒性:
度洛西汀Ames試驗、小鼠淋巴瘤細胞正向基因突變試驗、大鼠肝細胞程式外DNA合成(UDS)試驗、中國倉鼠骨髓細胞姊妹染色單體交換試驗、小鼠微核試驗結果均為陰性。
生殖毒性:
雌性或雄性大鼠在交配前和交配中經口給予度洛西汀劑量達45mg/kg/天(根據mg/m2推算,相對於人最大推薦劑量60 mg/天[MRHD]的7倍),未見對交配或生育力的影響。
大鼠和家兔致畸敏感期經口給予度洛西汀達45mg/kg/天(根據mg/m2推算,大鼠和家兔分別相當於MRHD的7倍和15倍),可見胎仔體重降低,未見致畸作用。無影響劑量為10mg/kg/天(根據mg/m2推算,大鼠和家兔分別相當於MRHD的2倍和3倍)。
大鼠圍產期經口給予度洛西汀30 mg/kg/天(根據mg/m2推算,大鼠相當於MRHD的5倍)時,幼仔出生後1天存活率、出生時和哺乳期體重下降,無影響劑量為10 mg/kg/天。在劑量為30 mg/kg/天時,幼仔出現行為改變,表現為反應性增高,如對噪音驚嚇反應增強、自主活動減少。子代斷奶後的生長和生殖行為未見不良影響。
致癌性:
大鼠和小鼠摻食法給予度洛西汀2年。雌性小鼠在度洛西汀劑量為140mg/kg/天(根據mg/m2推算,相當於MRHD的11倍)時,可見肝細胞腺瘤和肝細胞癌的發生率增加,無影響劑量為50mg/kg/天(根據mg/m2推算,相當於MRHD的4倍)。雄性小鼠在度洛西汀劑量為100mg/kg/天(根據mg/m2推算,相當於MRHD的8倍)時,未見腫瘤發生率增加。雌性大鼠和雄性大鼠在劑量分別為27和36mg/kg/天(根據mg/m2推算,分別相當於MRHD的4和6倍)時,未見腫瘤發生率增加。
藥代動力學
度洛西汀腸溶膠囊消除半衰期大約為 12小時(變化範圍為8-17小時),在治療範圍之內其藥代動力學參數與劑量成正比。一般於服藥3天后達到穩態血藥濃度。度洛西汀主要經肝臟代謝,涉及兩種P450酶:CYP2D6和CYP1A2。
吸收與分布-口服鹽酸度洛西汀腸溶膠囊吸收完全。平均滯後2小時,藥物開始被吸收(Tlag),口服 6小時後度洛西汀達到最大血漿濃度(Cmax)。進食不影響Cmax,但是將延遲達峰時間 6~10小時,略微降低吸收程度,約10% 。晚間一次服藥與晨間一次服藥相比,度洛西汀的吸收滯後3小時,表觀清除增加1/3。
表觀分布容積平均為 1640升。度洛西汀與人體血漿蛋白有高度親和性(>90%),主要與白蛋白和α1-酸性糖蛋白結合。目前還未評價度洛西汀和其他高蛋白結合藥物之間是否有藥物相互作用,肝或腎功能不全不影響度洛西汀的血漿蛋白結合。
代謝和排泄-口服C14標記的度洛西汀以確定其人體內生物轉化和降解。血漿中的度洛西汀僅占總放射標記物的3%,提示度洛西汀代謝廣泛,代謝產物多。度洛西汀主要的生物轉化途徑包括結合後萘基環氧化以及進一步氧化。體外試驗中CYP2D6和CYPIA2都可催化萘基環氧化,血漿中的代謝產物包括葡萄糖醛酸結合的4-羥基度洛西汀、硫酸結合的5-羥基6-甲氧基度洛西汀。尿中分離出多種其他代謝產物,有些僅出現在小的消除代謝旁路中。尿液中僅有少量未經代謝的鹽酸度洛西汀原形(約占口服劑量的1%),大部分(約占口服劑量的70%)以鹽酸度洛西汀代謝產物形式經尿液排出,大約20%經糞便排出。
特殊人群
性別-度洛西汀在男性、女性中的半衰期相似,不同性別無需調整劑量。
年齡-比較健康老年女性(65-77歲)與健康中年女性(32-50歲)單次口服40mg度洛西汀後的藥代動力學,其Cmax無差異,但老年女性的血藥濃度-時間曲線下面積(AUC)稍高(約25%),並且半衰期延長4小時。人群藥代動力學分析提示:從 25至75歲中,年齡每增加 1歲,藥物清除率下降約1% 。但是年齡作為一個預測因素,僅能解釋患者間個體變異的很小部分。無須根據年齡調整劑量(見用法用量)。
吸菸-吸菸者鹽酸度洛西汀的生物利用度(AUC)減少約1/3。不推薦吸菸者調整劑量。
種族-尚未進行專門的藥代動力學研究,探討不同種族的藥代動力學特徵。
腎功能不全-關於度洛西汀對終末期腎臟疾病(ESRD)患者影響的數據非常有限。單次口服60mg度洛西汀後,接受長期間歇性血液透析的終末期腎病患者,其Cmax和 AUC值比腎功能正常的人群增加約100%,然而兩者消除半衰期近似。大部分經尿液排出的主要循環代謝產物為葡萄糖醛酸結合的4-羥基度洛西汀、硫酸結合的5-羥基6-甲氧基度洛西汀,其AUC大約升高7-9倍,預計多次口服藥物後增加會更明顯。因此,不推薦終末期腎病的患者(需要透析者),或嚴重腎功能損害(估計肌酐清除率[CrCL]<30mL/min)者,使用度洛西汀腸溶膠囊(見[用法用量])。人群藥代動力學分析顯示,輕度到中度腎功能障礙(肌酐清除率[CrCL]30-80 ml/min)者,對度洛西汀的表觀清除無顯著影響。
肝功能不全-臨床上明顯的肝功能不全患者,度洛西汀的代謝和清除均下降。單次口服20mg度洛西汀後,6名中度肝功能不全肝硬化的患者(Child-Pugh B級)與年齡、性別相當的健康人群相比,平均血漿清除率為後者的15%,平均AUC較後者增加5倍。雖然肝硬化患者的Cmax與肝功能正常者近似,但是,前者半衰期延長3倍(見[注意事項])。不推薦度洛西汀用於治療有任何肝功能不全的患者(見[用法用量])。
吸收與分布-口服鹽酸度洛西汀腸溶膠囊吸收完全。平均滯後2小時,藥物開始被吸收(Tlag),口服 6小時後度洛西汀達到最大血漿濃度(Cmax)。進食不影響Cmax,但是將延遲達峰時間 6~10小時,略微降低吸收程度,約10% 。晚間一次服藥與晨間一次服藥相比,度洛西汀的吸收滯後3小時,表觀清除增加1/3。
表觀分布容積平均為 1640升。度洛西汀與人體血漿蛋白有高度親和性(>90%),主要與白蛋白和α1-酸性糖蛋白結合。目前還未評價度洛西汀和其他高蛋白結合藥物之間是否有藥物相互作用,肝或腎功能不全不影響度洛西汀的血漿蛋白結合。
代謝和排泄-口服C14標記的度洛西汀以確定其人體內生物轉化和降解。血漿中的度洛西汀僅占總放射標記物的3%,提示度洛西汀代謝廣泛,代謝產物多。度洛西汀主要的生物轉化途徑包括結合後萘基環氧化以及進一步氧化。體外試驗中CYP2D6和CYPIA2都可催化萘基環氧化,血漿中的代謝產物包括葡萄糖醛酸結合的4-羥基度洛西汀、硫酸結合的5-羥基6-甲氧基度洛西汀。尿中分離出多種其他代謝產物,有些僅出現在小的消除代謝旁路中。尿液中僅有少量未經代謝的鹽酸度洛西汀原形(約占口服劑量的1%),大部分(約占口服劑量的70%)以鹽酸度洛西汀代謝產物形式經尿液排出,大約20%經糞便排出。
特殊人群
性別-度洛西汀在男性、女性中的半衰期相似,不同性別無需調整劑量。
年齡-比較健康老年女性(65-77歲)與健康中年女性(32-50歲)單次口服40mg度洛西汀後的藥代動力學,其Cmax無差異,但老年女性的血藥濃度-時間曲線下面積(AUC)稍高(約25%),並且半衰期延長4小時。人群藥代動力學分析提示:從 25至75歲中,年齡每增加 1歲,藥物清除率下降約1% 。但是年齡作為一個預測因素,僅能解釋患者間個體變異的很小部分。無須根據年齡調整劑量(見用法用量)。
吸菸-吸菸者鹽酸度洛西汀的生物利用度(AUC)減少約1/3。不推薦吸菸者調整劑量。
種族-尚未進行專門的藥代動力學研究,探討不同種族的藥代動力學特徵。
腎功能不全-關於度洛西汀對終末期腎臟疾病(ESRD)患者影響的數據非常有限。單次口服60mg度洛西汀後,接受長期間歇性血液透析的終末期腎病患者,其Cmax和 AUC值比腎功能正常的人群增加約100%,然而兩者消除半衰期近似。大部分經尿液排出的主要循環代謝產物為葡萄糖醛酸結合的4-羥基度洛西汀、硫酸結合的5-羥基6-甲氧基度洛西汀,其AUC大約升高7-9倍,預計多次口服藥物後增加會更明顯。因此,不推薦終末期腎病的患者(需要透析者),或嚴重腎功能損害(估計肌酐清除率[CrCL]<30mL/min)者,使用度洛西汀腸溶膠囊(見[用法用量])。人群藥代動力學分析顯示,輕度到中度腎功能障礙(肌酐清除率[CrCL]30-80 ml/min)者,對度洛西汀的表觀清除無顯著影響。
肝功能不全-臨床上明顯的肝功能不全患者,度洛西汀的代謝和清除均下降。單次口服20mg度洛西汀後,6名中度肝功能不全肝硬化的患者(Child-Pugh B級)與年齡、性別相當的健康人群相比,平均血漿清除率為後者的15%,平均AUC較後者增加5倍。雖然肝硬化患者的Cmax與肝功能正常者近似,但是,前者半衰期延長3倍(見[注意事項])。不推薦度洛西汀用於治療有任何肝功能不全的患者(見[用法用量])。
貯藏
15~30℃室溫保存
包裝
鋁塑泡罩包裝,7粒/盒,14粒/盒,28粒/盒
有效期
36個月
執行標準
進口藥品註冊標準 JX20050132
