金喜素(注射用鹽酸托泊替康),適應症為1.小細胞肺癌。2.晚期轉移性卵巢癌經一線化療失敗者。
基本介紹
- 藥品名稱:金喜素
- 藥品類型:處方藥、醫保工傷用藥
- 用途分類:細胞毒性藥物
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,批准文號,生產企業,核准日期,
成份
本品主要成份為鹽酸托泊替康,輔料:酒石酸、甘露醇、氫氧化鈉。
化學名稱:(S)-10-二甲基氨基甲基-4-乙基-4,9-二羥基-1氫-吡喃酮[3’,4’:6,7]中氮茚[1,2-b]喹諾啉-3,14(4H,12H)-二酮鹽酸鹽。
化學結構式:
分子式:C23H23N3O5.HCI
分子量:457.91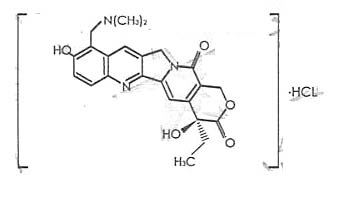
化學名稱:(S)-10-二甲基氨基甲基-4-乙基-4,9-二羥基-1氫-吡喃酮[3’,4’:6,7]中氮茚[1,2-b]喹諾啉-3,14(4H,12H)-二酮鹽酸鹽。
化學結構式:
分子式:C23H23N3O5.HCI
分子量:457.91

性狀
本品為淡黃色至黃色或淡黃綠色的疏鬆塊狀物或粉末。
適應症
1.小細胞肺癌。
2.晚期轉移性卵巢癌經一線化療失敗者。
2.晚期轉移性卵巢癌經一線化療失敗者。
規格
(1)2mg(按C23H23N3O5計);
(2)4mg(按C23H23N3O5計)。
(2)4mg(按C23H23N3O5計)。
用法用量
1.劑量:推薦劑量為1.2mg/m[sup]2[/sup]/日,靜脈輸注30分鐘。持續5天,21天為一療程,治療中嚴重的中性粒細胞減少症患者,在其後的療程中劑量減少0.2 mg/m[sup]2[/sup]或與G-CSF同時使用。使用從第6天開始,即在持續5天使用本品後24小時後再用G-CSF。
2.注射液配製:用無菌注射用水1ml溶解本品1mg比例溶解本品,按1.2mg/m[sup]2[/sup]/日劑量抽取藥液,用0.9%氯化鈉或5%葡萄糖注射液稀釋後靜脈輸注。
3.特殊人群的劑量調整
肝功能不全者:肝功能不全(血漿膽紅素1.5~10mg/d1)患者,血漿清除率降低,但一般不需劑量調整。
腎功能不全者:對輕微腎功能不全(CLcr40~60ml/分鐘)一般不需劑量調整,中度腎功能不全(CLcr20~39ml/分鐘)劑量調為0.6mg/m[sup]2[/sup],沒有足夠資料可證明在嚴重腎功能不全者可否使用。
4.老年人:除非腎功能不全,一般不作劑量調整。
2.注射液配製:用無菌注射用水1ml溶解本品1mg比例溶解本品,按1.2mg/m[sup]2[/sup]/日劑量抽取藥液,用0.9%氯化鈉或5%葡萄糖注射液稀釋後靜脈輸注。
3.特殊人群的劑量調整
肝功能不全者:肝功能不全(血漿膽紅素1.5~10mg/d1)患者,血漿清除率降低,但一般不需劑量調整。
腎功能不全者:對輕微腎功能不全(CLcr40~60ml/分鐘)一般不需劑量調整,中度腎功能不全(CLcr20~39ml/分鐘)劑量調為0.6mg/m[sup]2[/sup],沒有足夠資料可證明在嚴重腎功能不全者可否使用。
4.老年人:除非腎功能不全,一般不作劑量調整。
不良反應
1.血液系統:有白細胞減少、血小板減少、貧血等反應。骨髓抑制(主要是中性粒細胞)是本品的劑量限制性毒性,治療期間要監測外周血象,在治療中中性粒細胞恢復至]1500個/mm[sup]3[/sup],血小板恢復至100000個/mm[sup]3[/sup],血紅蛋白恢復至9.0g/d1方可繼續使用(必要時可使用G-CSF或輸注成分血)。與其它細胞毒藥物聯合套用時可加重骨髓抑制。
2.消化系統:噁心、嘔吐、腹瀉、便秘、腸梗阻、腹痛、口腔炎、厭食。
3.皮膚及附屬檔案:脫髮、偶見嚴重的皮炎及搔癢。
4.神經肌肉:頭痛、關節痛、肌肉痛、全身痛、感覺異常。
5.呼吸系統:可致呼吸困難。雖然尚不能肯定是否會因此造成死亡,但應引起醫生的重視。
6.肝臟:有時出現肝功能異常,轉氨酶升高。
7.全身:乏力、不適、發熱。
8.局部:靜脈注射時,若藥液漏在血管外局部可產生局部刺激、紅腫。
9.過敏反應:罕見過敏反應及血管神經性水腫。
2.消化系統:噁心、嘔吐、腹瀉、便秘、腸梗阻、腹痛、口腔炎、厭食。
3.皮膚及附屬檔案:脫髮、偶見嚴重的皮炎及搔癢。
4.神經肌肉:頭痛、關節痛、肌肉痛、全身痛、感覺異常。
5.呼吸系統:可致呼吸困難。雖然尚不能肯定是否會因此造成死亡,但應引起醫生的重視。
6.肝臟:有時出現肝功能異常,轉氨酶升高。
7.全身:乏力、不適、發熱。
8.局部:靜脈注射時,若藥液漏在血管外局部可產生局部刺激、紅腫。
9.過敏反應:罕見過敏反應及血管神經性水腫。
禁忌
1.對喜樹鹼類藥物或其任何成份過敏者。
2.嚴重骨髓抑制,中性粒細胞[1500個/mm[sup]3[/sup]者。
3.妊娠、哺乳期婦女。
2.嚴重骨髓抑制,中性粒細胞[1500個/mm[sup]3[/sup]者。
3.妊娠、哺乳期婦女。
注意事項
1.本品必須在對癌症化學治療有經驗的專科醫師的特別觀察下使用,對可能出現的併發症必須具有明確的診斷和適當處理的設施與條件。
2.由於可能發生嚴重的骨髓抑制,出現中性粒細胞減少,可導致患者感染甚至死亡,因此,治療期間要監測外周血常規,並密切觀察患者有無感染、出血傾向的臨床症狀,如有異常作減藥、停藥等適當處理。
3.本品是一種細胞抗癌藥,打開包裝及注射液的配製應穿隔離衣,戴手套,在垂直層流罩中進行。如不小心沾染在皮膚上,立即用肥皂和清水清洗,如沾染在黏膜或角膜上,用水徹底沖洗。
4.本品在避光包裝內,溫度攝氏20~25℃時保持穩定,由於藥內無抗菌成份,故開瓶後須立即使用,稀釋後在攝氏20~25℃可保存24小時。
2.由於可能發生嚴重的骨髓抑制,出現中性粒細胞減少,可導致患者感染甚至死亡,因此,治療期間要監測外周血常規,並密切觀察患者有無感染、出血傾向的臨床症狀,如有異常作減藥、停藥等適當處理。
3.本品是一種細胞抗癌藥,打開包裝及注射液的配製應穿隔離衣,戴手套,在垂直層流罩中進行。如不小心沾染在皮膚上,立即用肥皂和清水清洗,如沾染在黏膜或角膜上,用水徹底沖洗。
4.本品在避光包裝內,溫度攝氏20~25℃時保持穩定,由於藥內無抗菌成份,故開瓶後須立即使用,稀釋後在攝氏20~25℃可保存24小時。
孕婦及哺乳期婦女用藥
妊娠、哺乳期婦女禁用。
兒童用藥
目前尚缺乏兒童套用本藥的安全性資料。
老年用藥
老年人除非腎功能不全,一般不作劑量調整。
藥物相互作用
尚不明確。
藥物過量
目前尚不清楚本品過量的解毒方法,過量的主要併發症是骨髓抑制。
藥理毒理
1.抗腫瘤活性:本藥顯示了很強的抗腫瘤活性和廣泛的抗癌譜,臨床前的體內抑瘤試驗中對P388及L121白血病、B16黑色素瘤、B16/F10黑色素瘤亞株、Lew's肺癌、ADJ-PC6漿細胞瘤、M5076卵巢肉瘤、乳腺癌16/c、結腸腺癌38及51、Wadison肺癌等動物移植性腫瘤療效顯著。
2.作用方式:本藥為拓撲異構酶I的抑制劑。拓撲異構酶I可誘導DNA單鏈可逆性斷裂,使DNA螺旋鏈松解,本藥可與拓撲異構酶I-DNA複合物結合併阻止這些單股斷鏈的重新連線,其細胞毒作用是在DNA的合成中,是S期細胞周期特異性藥物。本藥與拓撲異構酶I和DNA形成的三元複合物與複製酶相互作用時產生雙股DNA的損傷。而哺乳動物的細胞不能有效地修復這些雙股DNA鏈的中斷。
2.作用方式:本藥為拓撲異構酶I的抑制劑。拓撲異構酶I可誘導DNA單鏈可逆性斷裂,使DNA螺旋鏈松解,本藥可與拓撲異構酶I-DNA複合物結合併阻止這些單股斷鏈的重新連線,其細胞毒作用是在DNA的合成中,是S期細胞周期特異性藥物。本藥與拓撲異構酶I和DNA形成的三元複合物與複製酶相互作用時產生雙股DNA的損傷。而哺乳動物的細胞不能有效地修復這些雙股DNA鏈的中斷。
藥代動力學
對癌症患者以1.5mg/m[sup]2[/sup]的劑量30分鐘靜脈滴注,在體內呈二室模型,分布非常快,很容易分布到肝、腎等血流灌注好的組織,其t1/2α為4.1~8.1分鐘。代謝產物內酯式托泊替康的t1/2β為1.7~8.4分鐘,總托泊替康t1/2β為2.3~4.3小時,與血漿蛋白結合率為6.6%~21.3%,藥物可進入腦脊液中,在腦脊液中有蓄積,大部分(26%~80%)經腎臟排泄,其中90%在用藥後12小時排泄,小部分經膽汁排泄。腎功能不全的病人對本藥的清除率低,其MTD亦降低,肝功能不全病人對本藥的代謝和毒性與正常人無明顯差異。
貯藏
遮光,密閉,在陰涼(不超過20℃)乾燥處保存。
包裝
中性西林瓶。(1)2mg(按C23H23N3O5計)/瓶/盒;
(2)4mg(按C23H23N3O5計)/瓶/盒。
(2)4mg(按C23H23N3O5計)/瓶/盒。
有效期
24個月。
執行標準
國家藥品標準WS1-(X-373)-2004Z
批准文號
(1)國藥準字H20000428
(2)國藥準字H20000429
(2)國藥準字H20000429
生產企業
貴州漢方製藥有限公司
核准日期
2006年10月18日
