適利達(拉坦前列素滴眼液),適應症為降低開角型青光眼和高眼壓症病人升高的眼壓。
基本介紹
- 藥品名稱:適利達
- 藥品類型:處方藥、外用藥、醫保工傷用藥
- 用途分類:其他眼科用藥
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,生產企業,核准日期,修訂日期,
成份
主要成份及其化學名稱:拉坦前列素,(Z)-7-[(1R,2R,3R,5S)3,5-二羥基-2-[(3R)-3-羥基-5-苯基-1-戊基]環戊基]-5-庚烯酸異丙酯。
其結構式:
分子式:C26H40O5
分子量;432.58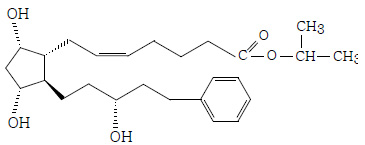
其結構式:
分子式:C26H40O5
分子量;432.58

性狀
本品為無色澄明液體。
適應症
降低開角型青光眼和高眼壓症病人升高的眼壓。
規格
1ml:50μg
2.5ml:125μg
2.5ml:125μg
用法用量
成人推薦劑量(包括老年人):
每次一滴,每天一次,滴於患眼。晚間使用效果最好。
本品不可超過每天使用一次,因為用藥次數增加會削弱降眼壓效果。
如果忘記用藥,在下次用藥時仍應按常規用藥。
與其它滴眼液相同,每次滴眼後應立即按壓內眼角處淚囊 1 分鐘以減少全身性吸收(閉塞淚點)。
不推薦聯合使用兩種或兩種以上前列腺素、前列腺素類似物(包括拉坦前列素)。有報導顯示,每天使用此類藥物一次以上,可能會降低拉坦前列素的降眼壓效果,引起反常的眼壓升高。
使用本品滴眼前應摘除角膜接觸鏡(隱形眼鏡),並在使用15 分鐘後才可重新佩戴。
如果還需使用其他眼用藥物,至少應間隔5分鐘用藥。
與其它滴眼液相同,每次滴眼後應按壓眼角處淚囊1分鐘以減少全身性吸收(閉塞淚點)。
兒童:見【兒童用藥】。
每次一滴,每天一次,滴於患眼。晚間使用效果最好。
本品不可超過每天使用一次,因為用藥次數增加會削弱降眼壓效果。
如果忘記用藥,在下次用藥時仍應按常規用藥。
與其它滴眼液相同,每次滴眼後應立即按壓內眼角處淚囊 1 分鐘以減少全身性吸收(閉塞淚點)。
不推薦聯合使用兩種或兩種以上前列腺素、前列腺素類似物(包括拉坦前列素)。有報導顯示,每天使用此類藥物一次以上,可能會降低拉坦前列素的降眼壓效果,引起反常的眼壓升高。
使用本品滴眼前應摘除角膜接觸鏡(隱形眼鏡),並在使用15 分鐘後才可重新佩戴。
如果還需使用其他眼用藥物,至少應間隔5分鐘用藥。
與其它滴眼液相同,每次滴眼後應按壓眼角處淚囊1分鐘以減少全身性吸收(閉塞淚點)。
兒童:見【兒童用藥】。
不良反應
觀察到的絕大多數不良事件均在眼部。在一項5 年的開放性的拉坦前列素安全性研究中,33%的病人出現虹膜色素沉著(見【注意事項】)。其他的眼部不良事件一般都是短暫的且只在用藥時發生。
依據發生頻率,不良事件可分為:很常見(≥1/10),常見(≥1/100 且 [1/10),少見(≥1/1000且[1/100),罕見(≥1/10,000 且[1/1000),非常罕見([1/10,000)。未知(無法從已有數據中估測)。
感染和侵染
未知:皰疹性角膜炎
眼
[u]很常見[/u]:虹膜色素沉著、輕至中度結膜充血、眼刺激(灼燒感、有砂礫感、瘙癢、刺痛和異物感)、睫毛和毳毛變化(變長、變粗、色素沉著、睫毛數量增加)(大多數為日本的患者)。
[u]常見[/u]:暫時性點狀上皮糜爛(大多無症狀)、瞼炎、眼痛、畏光。
[u]少見[/u]:眼瞼水腫、乾眼、角膜炎、視物模糊、結膜炎。
[u]罕見[/u]:虹膜炎/葡萄膜炎(許多病人具有伴隨的誘因)、黃斑水腫、有症狀的角膜水腫和糜爛、眶周水腫,倒睫毛有時引起眼刺激,在瞼板腺腺體開口處雙排睫毛(雙行睫毛)。
[u]未知[/u]:虹膜囊腫、眶周和眼瞼的變化導致眼瞼溝加深。
神經系統
未知:頭疼,頭暈。
心臟
非常罕見:加重心臟病患者的心絞痛。
未知:心悸。
呼吸、胸和縱隔
罕見:哮喘、哮喘加重和呼吸困難。
皮膚和皮下組織
少見:皮疹。
罕見:眼瞼局部皮膚反應,眼瞼皮膚變暗。
未知:中毒性表皮壞死松解症。
骨骼肌肉和結締組織
未知:肌痛,關節疼痛。
全身及給藥部位
非常罕見:胸痛。
兒童
兒童患者中進行的兩個短期臨床試驗( 12 周,共入組93 例,受試者分別為25 例和68 例)顯示兒童的安全性與成人類似,沒有出現新的不良事件。在不同年齡的兒童亞群中,安全性也類似。與成人相比,在兒童中出現較為頻繁的不良事件是鼻咽炎和發熱。
依據發生頻率,不良事件可分為:很常見(≥1/10),常見(≥1/100 且 [1/10),少見(≥1/1000且[1/100),罕見(≥1/10,000 且[1/1000),非常罕見([1/10,000)。未知(無法從已有數據中估測)。
感染和侵染
未知:皰疹性角膜炎
眼
[u]很常見[/u]:虹膜色素沉著、輕至中度結膜充血、眼刺激(灼燒感、有砂礫感、瘙癢、刺痛和異物感)、睫毛和毳毛變化(變長、變粗、色素沉著、睫毛數量增加)(大多數為日本的患者)。
[u]常見[/u]:暫時性點狀上皮糜爛(大多無症狀)、瞼炎、眼痛、畏光。
[u]少見[/u]:眼瞼水腫、乾眼、角膜炎、視物模糊、結膜炎。
[u]罕見[/u]:虹膜炎/葡萄膜炎(許多病人具有伴隨的誘因)、黃斑水腫、有症狀的角膜水腫和糜爛、眶周水腫,倒睫毛有時引起眼刺激,在瞼板腺腺體開口處雙排睫毛(雙行睫毛)。
[u]未知[/u]:虹膜囊腫、眶周和眼瞼的變化導致眼瞼溝加深。
神經系統
未知:頭疼,頭暈。
心臟
非常罕見:加重心臟病患者的心絞痛。
未知:心悸。
呼吸、胸和縱隔
罕見:哮喘、哮喘加重和呼吸困難。
皮膚和皮下組織
少見:皮疹。
罕見:眼瞼局部皮膚反應,眼瞼皮膚變暗。
未知:中毒性表皮壞死松解症。
骨骼肌肉和結締組織
未知:肌痛,關節疼痛。
全身及給藥部位
非常罕見:胸痛。
兒童
兒童患者中進行的兩個短期臨床試驗( 12 周,共入組93 例,受試者分別為25 例和68 例)顯示兒童的安全性與成人類似,沒有出現新的不良事件。在不同年齡的兒童亞群中,安全性也類似。與成人相比,在兒童中出現較為頻繁的不良事件是鼻咽炎和發熱。
禁忌
已知對本品滴眼液中任何成份過敏者。
注意事項
本品可能會增加虹膜棕色色素的數量而逐漸引起眼睛顏色改變。決定治療前應告知病人眼睛顏色改變的可能性。單側治療可導致永久性的眼睛不對稱。
眼睛顏色改變主要在虹膜混合顏色的病人中觀察到,如藍-棕、灰-棕、綠-棕和黃-棕混合色。顏色改變通常在治療的頭8個月內開始發生,但少數病人也可稍後發生。根據連續攝影獲得的證據,臨床研究中治療期超過4年的病人30%可發生此作用。
多數病人虹膜顏色改變輕微,通常臨床上觀察不到。虹膜混合色病人顏色改變的發生率從7%到85%不等,黃-棕混合色發生率最高。
純藍色眼睛未觀察到顏色改變,純灰、綠或棕色眼睛僅觀察到極少病人顏色改變。
顏色改變是因為虹膜基底的黑素細胞中黑色素含量增加,而非黑素細胞數量本身增加。典型特徵為瞳孔周圍棕色色素沉著呈向心性向四周分布,但整個虹膜或部分虹膜呈更深的棕色。一旦停藥,虹膜棕色色素不會再進一步加深。到目前為止,在臨床研究中,這種改變不伴有任何症狀或病理改變。
治療不會影響虹膜的痣或斑點。小梁網或前房其它部位色素積聚未在臨床研究中觀察到。已獲得的大於5年的長期用藥經驗顯示虹膜色素沉著無任何不良的臨床作用或影響,有虹膜色素沉著的病人仍可繼續使用本品。但病人應定期檢查,視臨床狀況,如需要可停用本品治療。
本品用於慢性閉角型青光眼、植入人工晶體的開角型青光眼和色素性青光眼僅有有限經驗。本品尚無用於炎性和新生血管性青光眼以及炎症性眼睛疾病的經驗。本品對瞳孔無作用或作用很小,但本品尚無用於閉角型青光眼急性發作的經驗。所以,在獲得更多經驗以前,建議在以上情況時應慎用本品。
本品用於白內障手術圍手術期的研究數據有限,應慎用於此類患者。
有皰疹性角膜炎病史的患者慎用本品,對於炎症活動期單純皰疹性角膜炎的患者和有復發性皰疹性角膜炎病史的患者應避免本品,尤其和其他前列腺素類似物合用。
在無晶狀體、人工晶體伴晶狀體後囊袋撕裂或植入前房人工晶體、或者已知有黃斑囊樣水腫危險因素的病人(如糖尿病視網膜病變和視網膜靜脈閉塞)中已有的黃斑水腫病例的報告(見【不良反應】)。
故本品應慎用於無晶狀體、人工晶體伴晶狀體後囊袋撕裂或植入型前房人工晶體、或者已知有黃斑囊樣水腫危險因素的患者。
已知有虹膜炎/葡萄膜炎易患危險因素的病人可使用本品,但應謹慎。
哮喘患者使用本品經驗有限,目前有一些上市後使用本品出現哮喘和/或呼吸困難惡化的報告。所以,在獲得足夠經驗以前,這些患者應慎用(見【不良反應】)。
觀察到眶周皮膚顏色改變,多數為日本人群的報導。目前的經驗表明,眶周皮膚顏色改變不是永久性的,有些病人繼續使用本品治療後此改變消失。
拉坦前列素可能會逐漸改變被治療眼的眼瞼和毳毛及其周圍區域,這些變化包括變長、變粗、變深、睫毛或體毛數量增加和倒睫毛。睫毛的變化在停藥後是可逆的。
本品含有苯扎氯銨,苯扎氯銨在滴眼劑中用作防腐劑。有報告說苯扎氯銨會導致點狀角膜病和/或毒性潰瘍性角膜病,可能會導致眼刺激,並且會使隱形眼鏡脫色。乾眼病人或角膜免疫功能低下的患者需要長期或者頻繁使用本品時應密切關注。隱形眼鏡可能會吸收苯扎氯銨,故在使用本品前應先摘除,並在使用15 分鐘之後才可佩戴(見【用法用量】)。
對駕駛及操作機器能力的影響
本品對駕駛及操作機器的能力有輕微或中度影響。
與其它眼部用藥相似,滴入藥液可能引起一過性視力模糊。建議患者在症狀消失後再駕駛及操作機器。
眼睛顏色改變主要在虹膜混合顏色的病人中觀察到,如藍-棕、灰-棕、綠-棕和黃-棕混合色。顏色改變通常在治療的頭8個月內開始發生,但少數病人也可稍後發生。根據連續攝影獲得的證據,臨床研究中治療期超過4年的病人30%可發生此作用。
多數病人虹膜顏色改變輕微,通常臨床上觀察不到。虹膜混合色病人顏色改變的發生率從7%到85%不等,黃-棕混合色發生率最高。
純藍色眼睛未觀察到顏色改變,純灰、綠或棕色眼睛僅觀察到極少病人顏色改變。
顏色改變是因為虹膜基底的黑素細胞中黑色素含量增加,而非黑素細胞數量本身增加。典型特徵為瞳孔周圍棕色色素沉著呈向心性向四周分布,但整個虹膜或部分虹膜呈更深的棕色。一旦停藥,虹膜棕色色素不會再進一步加深。到目前為止,在臨床研究中,這種改變不伴有任何症狀或病理改變。
治療不會影響虹膜的痣或斑點。小梁網或前房其它部位色素積聚未在臨床研究中觀察到。已獲得的大於5年的長期用藥經驗顯示虹膜色素沉著無任何不良的臨床作用或影響,有虹膜色素沉著的病人仍可繼續使用本品。但病人應定期檢查,視臨床狀況,如需要可停用本品治療。
本品用於慢性閉角型青光眼、植入人工晶體的開角型青光眼和色素性青光眼僅有有限經驗。本品尚無用於炎性和新生血管性青光眼以及炎症性眼睛疾病的經驗。本品對瞳孔無作用或作用很小,但本品尚無用於閉角型青光眼急性發作的經驗。所以,在獲得更多經驗以前,建議在以上情況時應慎用本品。
本品用於白內障手術圍手術期的研究數據有限,應慎用於此類患者。
有皰疹性角膜炎病史的患者慎用本品,對於炎症活動期單純皰疹性角膜炎的患者和有復發性皰疹性角膜炎病史的患者應避免本品,尤其和其他前列腺素類似物合用。
在無晶狀體、人工晶體伴晶狀體後囊袋撕裂或植入前房人工晶體、或者已知有黃斑囊樣水腫危險因素的病人(如糖尿病視網膜病變和視網膜靜脈閉塞)中已有的黃斑水腫病例的報告(見【不良反應】)。
故本品應慎用於無晶狀體、人工晶體伴晶狀體後囊袋撕裂或植入型前房人工晶體、或者已知有黃斑囊樣水腫危險因素的患者。
已知有虹膜炎/葡萄膜炎易患危險因素的病人可使用本品,但應謹慎。
哮喘患者使用本品經驗有限,目前有一些上市後使用本品出現哮喘和/或呼吸困難惡化的報告。所以,在獲得足夠經驗以前,這些患者應慎用(見【不良反應】)。
觀察到眶周皮膚顏色改變,多數為日本人群的報導。目前的經驗表明,眶周皮膚顏色改變不是永久性的,有些病人繼續使用本品治療後此改變消失。
拉坦前列素可能會逐漸改變被治療眼的眼瞼和毳毛及其周圍區域,這些變化包括變長、變粗、變深、睫毛或體毛數量增加和倒睫毛。睫毛的變化在停藥後是可逆的。
本品含有苯扎氯銨,苯扎氯銨在滴眼劑中用作防腐劑。有報告說苯扎氯銨會導致點狀角膜病和/或毒性潰瘍性角膜病,可能會導致眼刺激,並且會使隱形眼鏡脫色。乾眼病人或角膜免疫功能低下的患者需要長期或者頻繁使用本品時應密切關注。隱形眼鏡可能會吸收苯扎氯銨,故在使用本品前應先摘除,並在使用15 分鐘之後才可佩戴(見【用法用量】)。
對駕駛及操作機器能力的影響
本品對駕駛及操作機器的能力有輕微或中度影響。
與其它眼部用藥相似,滴入藥液可能引起一過性視力模糊。建議患者在症狀消失後再駕駛及操作機器。
孕婦及哺乳期婦女用藥
生育:
在動物研究中未發現拉坦前列素對雄性和雌性動物生育力有影響。(見【藥理毒理】)
孕婦:
本品對人類妊娠安全性的影響尚未建立,但它對妊娠過程,胎兒及新生兒可能存在潛在的藥理學影響,所以,孕婦不應使用本品。
哺乳期:
拉坦前列素及其代謝物可能會進入乳汁,故哺乳婦女不應使用本品,或者停止哺乳。
在動物研究中未發現拉坦前列素對雄性和雌性動物生育力有影響。(見【藥理毒理】)
孕婦:
本品對人類妊娠安全性的影響尚未建立,但它對妊娠過程,胎兒及新生兒可能存在潛在的藥理學影響,所以,孕婦不應使用本品。
哺乳期:
拉坦前列素及其代謝物可能會進入乳汁,故哺乳婦女不應使用本品,或者停止哺乳。
兒童用藥
兒童用藥的安全性與有效性尚未建立。本品不推薦用於兒童。
老年用藥
參見【用法用量】。
藥物相互作用
尚不明確。
目前出現了同時使用兩種前列腺素類似物滴眼液出現眼內壓升高的報告。所以,不推薦同時使用兩種或多種前列腺素、前列腺素類似物或前列腺素衍生物。
目前出現了同時使用兩種前列腺素類似物滴眼液出現眼內壓升高的報告。所以,不推薦同時使用兩種或多種前列腺素、前列腺素類似物或前列腺素衍生物。
藥物過量
本品過量滴眼,除了眼睛刺激和結膜充血外,尚未發現其它眼部副作用。
若意外誤服本品,請注意以下信息:每瓶滴眼液含拉坦前列素125微克,90%以上的拉坦前列素首過肝臟時即被代謝。健康志願者靜脈注射拉坦前列素3μg/kg無任何症狀,但5.5-10μg/kg可引起噁心,腹痛,頭暈,疲乏,臉潮熱和出汗。猴靜脈輸注拉坦前列素高達500μg/kg也無明顯的心血管系統作用。
猴靜脈給予拉坦前列素可引起短暫的支氣管收縮。但中度支氣管哮喘病人眼部使用本品劑量達臨床劑量7倍時也無拉坦前列素所致的支氣管收縮。
若發生藥物過量,請對症治療。
若意外誤服本品,請注意以下信息:每瓶滴眼液含拉坦前列素125微克,90%以上的拉坦前列素首過肝臟時即被代謝。健康志願者靜脈注射拉坦前列素3μg/kg無任何症狀,但5.5-10μg/kg可引起噁心,腹痛,頭暈,疲乏,臉潮熱和出汗。猴靜脈輸注拉坦前列素高達500μg/kg也無明顯的心血管系統作用。
猴靜脈給予拉坦前列素可引起短暫的支氣管收縮。但中度支氣管哮喘病人眼部使用本品劑量達臨床劑量7倍時也無拉坦前列素所致的支氣管收縮。
若發生藥物過量,請對症治療。
藥理毒理
藥理作用:
活性成份拉坦前列素為前列腺素F2α的類似物,是一種選擇性前列腺素FP受體激動劑,能通過增加房水流出而降低眼壓。在人類,降低眼壓約從給藥後3-4小時開始,8-12小時達到最大作用。降眼壓作用至少可維持24小時。動物和人類的研究均顯示藥物主要作用機制為增加房水的葡萄膜鞏膜旁道流出,雖然在人類也有報導增加了房水流出的便利度(減少引流阻力)。
主要的臨床研究證明本品單藥治療有效。雖然未進行明確的聯合用藥臨床研究,但一項為期3個月的研究顯示拉坦前列素與β-腎上腺素阻斷劑(噻嗎洛爾)合用有效。短期研究(1或2周)顯示拉坦前列素與腎上腺素激動劑(dipivalyl epinephrine),口服碳酸酐酶抑制劑(乙醯唑2胺)合用效果疊加,與膽鹼激動劑(毛果芸香鹼)合用效果至少部分疊加。
臨床研究還顯示拉坦前列素對房水的產生無明顯影響,對血液-房水屏障無任何作用。
按臨床劑量使用以及在猴子的研究中,拉坦前列素對眼內的血循環無影響或影響可忽略不計。但局部用藥可能發生輕至中度的結膜或鞏膜充血。
行囊外晶體摘除的猴子長期使用拉坦前列素,用螢光血管造影術確定不會影響視網膜血管。
拉坦前列素短期治療不會引起後房人工晶體螢光素滲漏。
臨床治療劑量的拉坦前列素對心血管或呼吸系統未發現有明顯的藥理作用。
毒理研究:
用數種動物進行了拉坦前列素的眼部和全身毒性作用研究。總的來說,拉坦前列素可很好地耐受,安全範圍很大,臨床眼用劑量和全身毒性劑量至少相差1000倍。未經麻醉的猴子靜脈注射高劑量拉坦前列素(約為臨床劑量/公斤體重的100倍),觀察到呼吸頻率增加,可能反映了短暫的支氣管收縮。動物試驗中未發現拉坦前列素有致敏性的特性。
在家兔和猴子,拉坦前列素劑量達100mcg/眼/天時也未觀察到眼部毒性作用(臨床劑量為1.5mcg/眼/天)。但拉坦前列素引起猴子虹膜色素增加。
色素增加的機制似乎是刺激了虹膜黑素細胞內黑色素的產生,但未觀察到增殖性改變。虹膜色素改變可能是永久性的。
在長期眼毒性研究中,給予拉坦前列素6mcg/眼/天還引起瞼裂加大,該作用可逆並只在劑量高於臨床劑量時發生。這一作用在人類未觀察到。
拉坦前列素在細菌突變逆轉試驗,小鼠淋巴瘤的基因突變試驗和小鼠微核試驗中均呈陰性。體外人淋巴細胞試驗中觀察到染色體異常。前列腺素F2α,一種正常情況下存在的前列腺素,也觀察到類似作用,表明該作用為這一類物質所共有。
關於致突變試驗,進行了大鼠體內和體外的不定期DNA合成研究,結果呈陰性,表明拉坦前列素無致突變作用。小鼠和大鼠的致癌試驗也呈陰性。
動物試驗中未發現拉坦前列素對雄性和雌性生育力有任何影響。在大鼠胚胎毒性研究中,拉坦前列素靜脈給藥劑量5、50和250μg/kg/天未觀察到任何胚胎毒性。但在家兔,拉坦前列素劑量5μg/kg/天或以上時可引起胚胎死亡。
劑量5μg/kg/天(約為臨床劑量的100倍)可引起明顯的胚胎胎兒毒性,表現為晚期吸收和流產發生率增加以及胎兒重量降低。
未發現任何致畸作用。
活性成份拉坦前列素為前列腺素F2α的類似物,是一種選擇性前列腺素FP受體激動劑,能通過增加房水流出而降低眼壓。在人類,降低眼壓約從給藥後3-4小時開始,8-12小時達到最大作用。降眼壓作用至少可維持24小時。動物和人類的研究均顯示藥物主要作用機制為增加房水的葡萄膜鞏膜旁道流出,雖然在人類也有報導增加了房水流出的便利度(減少引流阻力)。
主要的臨床研究證明本品單藥治療有效。雖然未進行明確的聯合用藥臨床研究,但一項為期3個月的研究顯示拉坦前列素與β-腎上腺素阻斷劑(噻嗎洛爾)合用有效。短期研究(1或2周)顯示拉坦前列素與腎上腺素激動劑(dipivalyl epinephrine),口服碳酸酐酶抑制劑(乙醯唑2胺)合用效果疊加,與膽鹼激動劑(毛果芸香鹼)合用效果至少部分疊加。
臨床研究還顯示拉坦前列素對房水的產生無明顯影響,對血液-房水屏障無任何作用。
按臨床劑量使用以及在猴子的研究中,拉坦前列素對眼內的血循環無影響或影響可忽略不計。但局部用藥可能發生輕至中度的結膜或鞏膜充血。
行囊外晶體摘除的猴子長期使用拉坦前列素,用螢光血管造影術確定不會影響視網膜血管。
拉坦前列素短期治療不會引起後房人工晶體螢光素滲漏。
臨床治療劑量的拉坦前列素對心血管或呼吸系統未發現有明顯的藥理作用。
毒理研究:
用數種動物進行了拉坦前列素的眼部和全身毒性作用研究。總的來說,拉坦前列素可很好地耐受,安全範圍很大,臨床眼用劑量和全身毒性劑量至少相差1000倍。未經麻醉的猴子靜脈注射高劑量拉坦前列素(約為臨床劑量/公斤體重的100倍),觀察到呼吸頻率增加,可能反映了短暫的支氣管收縮。動物試驗中未發現拉坦前列素有致敏性的特性。
在家兔和猴子,拉坦前列素劑量達100mcg/眼/天時也未觀察到眼部毒性作用(臨床劑量為1.5mcg/眼/天)。但拉坦前列素引起猴子虹膜色素增加。
色素增加的機制似乎是刺激了虹膜黑素細胞內黑色素的產生,但未觀察到增殖性改變。虹膜色素改變可能是永久性的。
在長期眼毒性研究中,給予拉坦前列素6mcg/眼/天還引起瞼裂加大,該作用可逆並只在劑量高於臨床劑量時發生。這一作用在人類未觀察到。
拉坦前列素在細菌突變逆轉試驗,小鼠淋巴瘤的基因突變試驗和小鼠微核試驗中均呈陰性。體外人淋巴細胞試驗中觀察到染色體異常。前列腺素F2α,一種正常情況下存在的前列腺素,也觀察到類似作用,表明該作用為這一類物質所共有。
關於致突變試驗,進行了大鼠體內和體外的不定期DNA合成研究,結果呈陰性,表明拉坦前列素無致突變作用。小鼠和大鼠的致癌試驗也呈陰性。
動物試驗中未發現拉坦前列素對雄性和雌性生育力有任何影響。在大鼠胚胎毒性研究中,拉坦前列素靜脈給藥劑量5、50和250μg/kg/天未觀察到任何胚胎毒性。但在家兔,拉坦前列素劑量5μg/kg/天或以上時可引起胚胎死亡。
劑量5μg/kg/天(約為臨床劑量的100倍)可引起明顯的胚胎胎兒毒性,表現為晚期吸收和流產發生率增加以及胎兒重量降低。
未發現任何致畸作用。
藥代動力學
拉坦前列素(分子量432.58)為異丙酯化的前藥,無活性。當水解轉化為拉坦前列素酸以後具有生物活性。前藥可通過角膜很好地吸收,進入房水的藥物在透過角膜時已全部被水解。
人體研究顯示房水中藥物峰濃度在局部用藥後約2小時達到。猴子局部用藥後,拉坦前列素先分布於前房,結膜和眼瞼,只有很少量的藥物到達眼後房。
拉坦前列素酸在眼內幾乎沒有代謝。代謝主要發生在肝臟。人血漿中半衰期為17分鐘。主要代謝產物1,2-二去甲和1,2,3,4-四去甲代謝物在動物試驗中沒有或僅有微弱的生物活性,且主要從尿中排瀉。
人體研究顯示房水中藥物峰濃度在局部用藥後約2小時達到。猴子局部用藥後,拉坦前列素先分布於前房,結膜和眼瞼,只有很少量的藥物到達眼後房。
拉坦前列素酸在眼內幾乎沒有代謝。代謝主要發生在肝臟。人血漿中半衰期為17分鐘。主要代謝產物1,2-二去甲和1,2,3,4-四去甲代謝物在動物試驗中沒有或僅有微弱的生物活性,且主要從尿中排瀉。
貯藏
開封前 2-8℃ 冷藏,避光保存。
開封后可在低於 25℃ 室溫下保存,4周內用完。
開封后可在低於 25℃ 室溫下保存,4周內用完。
包裝
滴眼液裝於聚乙烯塑膠瓶中,外加紙盒包裝,2.5ml/瓶/盒。
有效期
36 個月
執行標準
進口藥品註冊標準 JX19990382
生產企業
Pfizer Manufacturing Belgium NV
核准日期
2006年11月30日
修訂日期
2008年02月14日 2010年01月27日 2010年08月12日 2010年11月12日 2011年02月01日 2011年06月22日 2011年12月12日 2012年09月17日
