含蛋白質的食品在高溫或鹼處理時,賴氨酸易和胱氨酸、絲氨酸、磷酸絲氨酸或脫氫丙氨酸發生交聯,會生成的一種新的胺基酸——賴丙氨酸。
賴丙氨酸(簡稱LAL),化學名為Nε-(D,L-2-氨基-2-羧乙基-D,L-賴氨酸)。由於具有兩個不對稱的碳原子,因而存在著4種光學異構體,分別為L-L,L-D,D-L,D-D(前面的字元表示賴氨酸部分,後面的字元表示丙氨酸部分的異構體)。LL-LAL和LD-LAL二的旋光度分別為100.7°和-14.8°。賴丙氨酸的穩定性性較差,受熱易發生分解,於熱醇溶液中會發生部分酯化,於熱水溶液中會發生部分分解。
基本介紹
- 中文名:賴丙氨酸
- 英文名:Lysinoalanine Dihydrochloride
- 化學式:C9H19N3O4
- 分子量:233.13767
- CAS登錄號:4418-81-9
- 沸點:490.2°C at 760 mmHg
- 密度:1.272g/cm3
- 閃點:250.3°C
- 三字簡稱:LAL
物理化學性質,1.1 解離常數,1.2 等電點PI,1.3 茚三酮反應,1.4 氧化反應,1.5 穩定性,
物理化學性質
賴丙氨酸[Nε-(D,L-2氨基-2-羧乙基-D,L-賴氨酸)]具有2個光學活性中心,因而存在著4種光學異構體,即L-L,L-D,D-L,D-D(前面的字元表示賴氨酸部分,後面的字元表示丙氨酸部分的異構體)
1.1 解離常數
PK1<1.5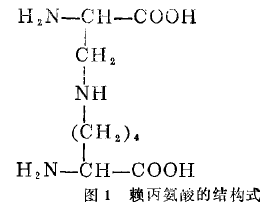 賴丙氨酸的結構式
賴丙氨酸的結構式
 賴丙氨酸的結構式
賴丙氨酸的結構式PK2=2.2
PK3=6.5
PK4=8.8
PK5=9.9
1.2 等電點PI
7.7 (L-D,L體) (Cf·賴氨酸的pI=9.5)
1.3 茚三酮反應
A570為亮氨酸的1.6倍,胺基酸分析儀的波峰面積為賴氨酸的1.42倍。
1.4 氧化反應
1.4.1過碘酸氧化
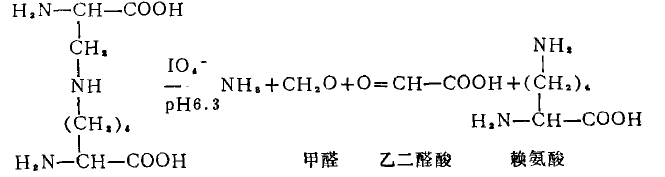 賴丙氨酸的過碘酸氧化反應
賴丙氨酸的過碘酸氧化反應1.4.2 酶氧化
(1)在用劇毒的L-胺基酸氧化酶作用時(0.2毫克酶,pH7.5,37℃,24小時),氧化分成L-L型的丙氨酸和賴氦酸兩部分。
(2)在用豬腎的結晶D-胺基酸氧化酶(比活性30u/毫克)作用時(pH8.3,30℃,24小時),僅氧化成L-D型的丙氮酸部分。
1.5 穩定性
(1)在乙醇中不穩定(60℃,10分鐘有20%被酯化).
(2)水溶液容易熱分解(即使在60℃也有相當的分解。因此,在用胺基酸分析儀測定時有結果偏低的危險。在115℃,16小時,有70%分解。生成賴氨酸65.5%、丙氨酸1.2%、甘氨酸2.9%、絲氨酸0.7%。若加鹽酸這種分解可稍有抑制)。
(3)在2N鹽酸中煮沸可迅速消旋.
(4)在強鹼中似有分解。
(5)在蛋白質的加水分解條件(6NH4CI,110℃,24小時)下,有10%分解。

