基本信息
拼音
zhēng fā
英文
①evaporate
②evaporation
例句
蕭紅《手》:“窗
前的
楊樹抽著芽,操場好像冒著
煙似的,被太陽蒸發著。”
老舍《
駱駝祥子》十八:“在這個白光里,每一個
顏色都刺目,每一個聲響都難聽,每一種氣味都混含著由地上蒸發出來的腥臭。”
概述
蒸發和沸騰都是汽化現象,是汽化的兩種不同方式。蒸發是在液體表面發生的汽化過程,沸騰是在液體內部和表面上同時發生的劇烈的汽化現象[2]。溶液的蒸發(evaporation)通常是指通過加熱使溶液中一部分溶劑汽化,以提高溶液中非揮發性組分的濃度(濃縮)或使溶質從溶液中析出結晶的過程。通常,溫度越高、液面暴露面積越大,蒸發速率越快;溶液表面的壓強越低,蒸發速率越快。
物理現象
原理
蒸發量是指在一定時段內水分經蒸發而散布到空中的量,通常用蒸發掉的水層厚度的毫米數表示,水面或
土壤的水分蒸發量,分別用不同的
蒸發器測定。一般
溫度越高、
濕度越小、風速越大、
氣壓越低、則蒸發量就越大;反之蒸發量就越小。從
微觀上看,蒸發就是液體
分子從液面離去的過程。由於液體中的分子都在不停地作無規則
運動,它們的平均動能的大小是跟液體本身的溫度相適應的。由於分子的無規則運動和相互碰撞,在任何時刻總有一些分子具有比平均動能還大的動能。這些具有足夠大動能的分子,如處於液面附近,其動能大于飛出時克服液體內分子間的
引力所需的功時,這些分子就能脫離液面而向外飛出,變成這種液體的汽,這就是
蒸發現象。飛出去的分子在和其他分子碰撞後,有可能再回到液面上或進入液體內部。如果飛出的分子多於飛回的,液體就在蒸發。
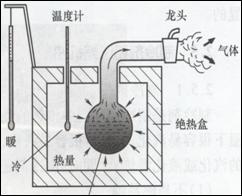 液體的蒸發
液體的蒸發 其他條件相同的不同液體,蒸發快慢亦不相同。這是由於液體分子之間
內聚力大小不同而造成的。例如,
水銀分子之間的內聚力很大,只有極少數動能足夠大的分子才能從液面逸出,這種液體蒸發就極慢。而另一些液體如
乙醚,分子之間的內聚力很小,能夠逸出液面的分子數量較多,所以蒸發得就快。
在
蒸發過程中,液體蒸發不僅吸熱還有使周圍物體冷卻的作用。當液體蒸發時,從液體裡跑出來的分子,要克服液體表面層的分子對它們的
引力而
做功。這些分子能做功,是因為它們具有足夠大的動能。比平均動能大的分子飛出液面,速度大的分子飛出去,而留存液體內部的分子所具有的平均動能變小了。所以在蒸發過程中,如外界不給液體補充
能量,液體的溫度就會下降。這時,它就要通過
熱傳遞方式從周圍物體中吸取
熱量,於是使周圍的物體冷卻。
影響因素
主要因素:(一)
溫度。
溫度越高,蒸發越快。因為在任何溫度下,分子都在不斷地運動,液體中總有一些速度較大的分子能夠飛出液面脫離束縛而成為汽分子,所以液體在任何溫度下都能蒸發。液體的溫度升高,分子的平均動能增大,速度增大,從液面飛出去的分子數量就會增多,所以液體的溫度越高,蒸發得就越快
 蒸發儀器蒸發皿
蒸發儀器蒸發皿 (二)液面表面積大小。如果液體表面面積增大,處於液體表面附近的分子數目增加,因而在相同的時間裡,從液面飛出的分子數量就增多,所以液面面積越大,蒸發速度越快
(三)液體表面上方空氣流動的速度。當飛入空氣里的汽分子和空氣分子或其他汽分子發生碰撞時,有可能被碰回到液體中來。如果液面上方空氣流動速度快,通風好,分子重新返回液體的機會越小,蒸發就越快。
分類
蒸發可分為常壓蒸發和減壓蒸發。
常壓蒸發
常壓蒸發裝置簡單,易於操作,一般在蒸發皿或燒杯中進行,待蒸發溶液的體積不應超過蒸發器皿容積的2/3。蒸發皿中的液面面積較大,有利於快速濃縮。若溶質對熱穩定,可將溶液放人蒸發皿或燒杯中,然後在水浴中加熱,也可用煤氣燈或電加熱器直接加熱。用煤氣燈直接加熱時,須先將蒸發皿置於石棉網上用小火均勻預熱,然後用大火加熱,至微沸時再改用小火維持沸騰狀態。在加熱過程中應不斷攪拌,以加快蒸發的速率,並防止溶液暴沸、濺出。若溶劑為有機溶劑,則不可用明火加熱,要選用水浴、油浴或電加熱器加熱,並且應在通風櫥(fume cupboard)中進行。
減壓蒸發
若被濃縮的物質對熱不穩定,常壓下易氧化、分解,或溶劑為高沸點的有機溶劑,或溶劑的量大、或有毒時,常採用減壓蒸餾的方式進行濃縮。
說明
(1) 蒸發可以在任何溫度下進行,而沸騰只能在一定溫度下發生。
(2) 蒸發時要從液體中吸收熱量,使液體溫度降低,所以蒸發有致冷作用;沸騰時要從周圍的物體吸收熱量,但溫度保持不變,這個不變的溫度叫沸點。
(3) 蒸發快慢與液體表面積的大小、溫度的高低、通風條件以及壓強大小等有關。在相同條件下,不同液體的蒸發快慢也不同,如酒精蒸發。
蒸發實驗
原理
利用加熱的方法,使溶液中
溶劑不斷
揮發而析出溶質(
晶體)的過程。
實驗儀器
蒸發皿 為一陶瓷淺底的圓碟狀容器。 當欲由溶液中得到
固體時,常需以加熱的方法趕走溶劑,此時就要用到蒸發皿。溶劑蒸發的
速率愈快,它的結晶
顆粒就愈小。視所需蒸發速率的快慢不同,可以選用直接將蒸發皿放在
火焰上加熱的快速蒸發、用水浴加熱的較和緩的蒸發或是令其在室溫的狀態下慢慢地蒸發三種方式。一般在
實驗室中要純化固體時,都要以再結晶的方法來使固體的純度增加。再結晶的方法通常為選取適當的溶劑,使不純物中的雜質在此溶劑中具有難溶或不溶的特性,而欲純化的成分則在此溶劑中有相當好的
溶解度。先將欲純化的固體以最少量的熱溶劑溶解,此時若有不溶的雜質,則應立即將溶液在此溫熱的狀況下過濾 ;如此即可將不溶的固體雜質藉過濾留在濾紙上;濾下的濾液中 主成分的純度即可增加,再將濾液倒入蒸發皿中令其結晶,得到的
晶體即為純度增高的
物質。
 蒸發儀器蒸發皿
蒸發儀器蒸發皿操作要領
1.蒸發皿中液體的量不得超過容積的2/3。
2.蒸發過程中必須用玻璃棒不斷攪拌,使液體受熱均勻,以防止局部溫度過高而使
液體飛濺。
3.當加熱至(大量)
固體出現時,應停止加熱利用餘熱蒸乾。
4.不能把熱的蒸發皿直接放在實驗台上,應墊上
石棉網。
5.坩堝鉗用於夾持蒸發皿。
操作口訣
皿中液體不宜多,防止飛濺要攪動。
較多固體析出時,移去酒燈自然蒸。
相關解釋
1、皿中液體不宜多,防止
飛濺要攪動:“皿”指蒸發皿。意思是說加入蒸發皿中的液體不宜過多(一般不應超過蒸發皿容積的2/3),在加熱過程中,要用
玻璃棒不斷攪動,防止由於局部溫度過高,造成液滴飛濺。
2、較多固體析出時,移去酒燈自然蒸:意思是說當蒸發皿中出現較多的固體時,應立即移去
酒精燈停止
加熱,利用蒸發皿的餘熱使液體自然蒸乾。
氣象過程
大氣中的水分經常處於沒有飽和的狀態,於是無論是海洋還是陸地都緩慢進行著水分從下墊面“蒸發”而進入大氣的物理過程。
自然界中蒸發現象頗為複雜,影響蒸發速度的主要因子有:水源;熱源;飽和差;風速與
湍流擴散強度。 ⑴
水源。 沒有水源就不可能有蒸發,因此開闊水域、雪面、冰面或潮濕土壤、
植物是產生蒸發的基本條件。在沙漠中,蒸發潛力很大,但實際蒸發量非常少,因幾乎無水可供蒸發。
⑵
熱源。 蒸發必須消耗熱量,在蒸發過程中如果沒有熱量供給,蒸發麵就會逐步冷卻,從而使蒸發麵上的
水汽壓減低,於是蒸發減緩或逐漸停止。因此蒸發速度在很大程度上決定於熱量的供給。
⑶
飽和差。 在其他因素相同的情況下,蒸發速度與飽和差成正比。嚴格說此處的
飽和水汽壓應由蒸發麵的溫度算出,但通常以一定的
氣溫下的飽和水汽壓代替。
⑷
風速與湍流擴散。 無風時,蒸發麵上的水汽單靠
分子擴散,水汽壓減小得慢,飽和差小,因而蒸發緩慢。有風時,湍流加強,蒸發麵上的水汽隨風和湍流迅速散布到廣大的空間,蒸發麵上水汽壓減小增快,飽和差增大,蒸發加快。
除上述基本因子外,大陸上的蒸發還應考慮到土壤的結構、濕度、植被的特徵等。海洋上的蒸發還應考慮水中的鹽分。 在影響蒸發的因子中,蒸發麵的溫度(熱量)通常是影響蒸發能力起決定作用的因子。由於蒸發麵(陸面及水面)的溫度有年、日變化,所以蒸發量也有年、日變化。全球的平均情況是每年大約從下墊面(海洋、陸地、冰原)蒸發的水層的深度為1m。
化工操作
化工生產中蒸發操作的目的通常有三。
①獲得濃縮的溶液直接作為化工產品或半成品;
②藉蒸發以脫除溶劑,將溶液增濃至飽和狀態,隨後加以冷卻,析出固體產物,即採用蒸發、結晶的聯合操作以獲得固體溶質;
③脫除溶質,製取純淨的溶劑。
圖為典型的蒸發裝置示意圖。蒸發器內備有足夠的加熱面,使溶液受熱
沸騰。溶液在蒸發器內因各處密度的差異而形成某種循環流動,被濃縮到規定
濃度後排出蒸發器外。
汽化的
蒸汽常夾帶有較多的霧末和液滴,因此蒸發器內需備有足夠的分離空間,往往還裝有適當形式的除沫器以除去液沫。排出的蒸氣如不再利用,應將其在冷凝器中加以冷凝。
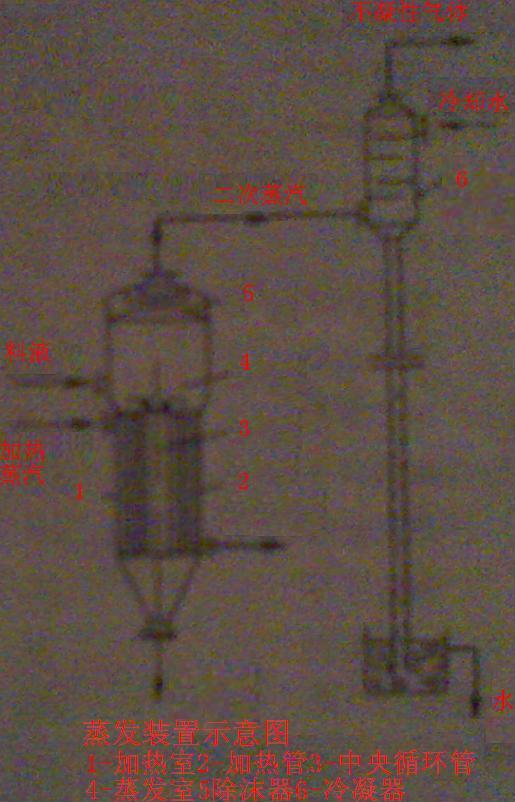 蒸發裝置示意圖
蒸發裝置示意圖蒸發操作可連續或間歇地進行,工業上大量物料的蒸發通常是連續的定態過程。
蒸發量測量
土壤蒸發量和和水面蒸發量的測定,在農業生產和
水文工作上非常重要。
雨量稀少、地下水源及流入
徑流水量不多的地區,如蒸發量很大,極易發生
乾旱。
 液體的蒸發
液體的蒸發 蒸發儀器蒸發皿
蒸發儀器蒸發皿 蒸發儀器蒸發皿
蒸發儀器蒸發皿
 液體的蒸發
液體的蒸發 蒸發儀器蒸發皿
蒸發儀器蒸發皿 蒸發儀器蒸發皿
蒸發儀器蒸發皿