絕熱過程是一個絕熱體系的變化過程,屬於封閉體系的一種。絕熱過程有絕熱壓縮和絕熱膨脹兩種。現實中,不存在真正意義上符合定義的絕熱過程,絕熱過程只是一種近似,所以有時也稱為絕熱近似。絕熱過程分為可逆過程和不可逆過程兩種。
基本介紹
- 中文名:絕熱過程
- 外文名:adiabatic process
- 類型:絕熱體系的變化過程
- 所屬領域:熱學
簡介
絕熱過程
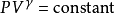
絕熱過程是一個絕熱體系的變化過程,屬於封閉體系的一種。絕熱過程有絕熱壓縮和絕熱膨脹兩種。現實中,不存在真正意義上符合定義的絕熱過程,絕熱過程只是一種近似,所以有時也稱為絕熱近似。絕熱過程分為可逆過程和不可逆過程兩種。
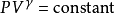
絕熱過程(熱學)編輯 鎖定 本詞條缺少概述圖,補充相關內容使詞條更完整,還能快速升級,趕緊來編輯吧!絕熱過程是一個絕熱體系的變化過程,屬於封閉體系的一種。絕熱...
絕熱過程是為了便於分析計算而進行的簡化和抽象,它又是實際過程的一種近似,當過程進行得很快,工質與外界來不及交換熱量時,例如,葉輪式壓氣機和氣流流經噴管的...
絕熱過程(adiabatic process)是指任一氣體與外界無熱量交換時的狀態變化過程,是...納米孔超級絕熱材料氣凝膠的製備與熱學特性. 《 過程工程學報 》 , 2002 倪...
以上三種過程方程的建立很直觀又極其容易,所以學生對它們沒有絲毫的疑慮.然而絕熱過程方程的建立就大不一樣了.現行的熱學教材上有二種不同的處理方法,一種是不作...
不可逆絕熱過程是指熱力學系統在狀態變化時經歷的一種理想過程。熱力學系統由某一狀態出發,經過某一過程到達另一狀態後,如果無論採用何種辦法都不能使系統和外界...
絕熱壓縮是與外界沒有熱量交換的壓縮過程。但外界對氣體做功,壓縮氣體,因此,並不同於孤立系統。根據能量守恆的原理,理想氣體在絕熱壓縮時溫度升高,在絕熱膨脹時溫度...
絕熱過程,系統與環境之間用絕熱壁隔開, 此時系統中所進行的過程稱為絕熱過程。循環過程,系統經一系列變化後又回到原來狀態的過程。熱力學過程分類 編輯 實際的熱力...
關於理想氣體,有可逆絕熱過程方程,在滿足理想氣體、絕熱、可逆這三個基本條件,才能使用該方程。從理想氣體的絕熱可逆方程可以看出:理想氣體在絕熱可逆過程中的任意某...
絕熱可逆過程:就是體系沒有熱量的散失,且該反映是可逆的過程。可逆的絕熱過程是等熵過程。等熵過程的對立面是等溫過程,在等溫過程中,最大限度的熱量被轉移到了...
絕熱體系的獲得,就是分別從傳導、對流和輻射三種方式上隔絕、阻止熱量的傳遞。熱力學系統始終不與外界交換熱量, 即dQ =0 的過程。根據熱力學第一定律,在絕熱過程...
《大學物理學(二)熱學》是1999年清華大學出版社出版的圖書,作者是張三慧。本書是清華大學教材《大學物理學》的第二冊,可作為高等院校的大學物理教材,也可以作為...
未飽和濕空氣團在上升過程中,先按乾絕熱上升,直至水汽達到飽和(即達到凝結高度),此後空氣團開始假絕熱上升,即空氣團中一旦有凝結水形成就全部從氣團中降落,並...
《熱學》是編者在多年講授熱學課程的基礎上,認真參考近年來出版的熱學教材,針對...5.7.3 等溫過程 5.7.4 絕熱過程 5.7.5 多方過程 5.8 熱力學循環 ...
由於體系熵的變化值等於可逆過程熱溫商δQ/T之和,所以只能通過可逆過程求的體系的熵變。孤立體系的可逆變化或絕熱可逆變化過程ΔS=0。...
絕熱壓縮性也稱“定熵壓縮係數”。簡單可壓縮系統在定熵過程中比容隨壓力的變化率與比容的比值。是表示物質系統在可逆絕熱條件下相對壓縮性的常用熱係數之一。 [1...
熱力學(thermodynamics)是從巨觀角度研究物質的熱運動性質及其規律的學科。屬於物理學的分支,它與統計物理學分別構成了熱學理論的巨觀和微觀兩個方面。熱力學主要是從...
不可逆絕熱過程Sf>Si,式中Sf和Si分別為系統的最終和最初的熵。也就是說,在...《新概念物理教程 熱學》第二版. 高等教育出版社. ISBN 9787040066777. 8. J...
循環/過程壓縮吸熱膨脹放熱 外燃機或熱泵經常使用的循環方式 埃里克森循環(第一類,1833年提出) 布雷頓循環 絕熱 等壓 絕熱 等壓 貝爾·科曼循環 (逆向布雷頓循環)...
熱力學定律是描述物理學中熱學規律的定律,包括熱力學第零定律、熱力學第一定律...物系的熵不變的過程本為孤立系統的可逆絕熱過程。所以, 在接近絕對零度時絕熱...
內能的巨觀定義式為:ΔU=Wa,其中ΔU為內能的變化量,Wa為絕熱過程外界對系統的做功量。在巨觀定義中,內能是一個相對量。內能是系統的一種狀態函式(簡稱態函式)...
卡諾循環是由法國工程師尼古拉·萊昂納爾·薩迪·卡諾於1824年提出的,以分析熱機的工作過程,卡諾循環包括四個步驟: 等溫吸熱, 絕熱膨脹,等溫放熱,絕熱壓縮。即理想氣...
4-1 熱力過程分析概述4-2 定容過程4-3 定壓過程4-4 定溫過程4-5 絕熱過程4-6 多變過程思考題習題第五章 熱力學第二定律...
較高壓力下的流體(氣或液)經多孔塞(或節流閥)向較低壓力方向絕熱膨脹過程稱為節流膨脹。1852年,焦耳和湯姆遜設計了一個節流膨脹實驗,使溫度為T1的氣體在一個...
1.7 絕熱過程與多方過程 1.8 卡諾循環 1.9 熱力學第二定律 1.10 卡諾定理和熱力學溫標 1.11 熵 熵增加原理 第2章 均勻介質熱力學 2.1 熱力學函式 2.2 ...
若體系在恆溫條件下發生了狀態變化,則體系的變化為“恆溫過程”。若體系變化時和環境之間無熱量交換,則稱為“絕熱過程”。途徑:完成一個熱力學過程,可以採取不同...
