硫酸鉍(Bismuth Sulfate),也稱為鹼式硫酸鉍。分子式為Bi2(SO4)3,分子量為706.15。
為白色針狀結晶或粉未,呈酸性反應。在水或醇中分解成鹼式鹽。加熱至465℃分解放出三氧化硫,能溶於稀鹽酸或稀硝酸,不溶於水和醇。
基本介紹
- 中文名:硫酸鉍
- 英文名:Bismuth Sulfate
- 別稱:鹼式硫酸鉍
- 化學式:Bi2(SO4)3
- 分子量:706.15
- CAS登錄號:7787-68-0
- EINECS登錄號:232-129-5
- 熔點:710℃
- 水溶性:不溶於水
- 密度:5.08
- 外觀:白色針狀結晶或粉未
物化性質,合成方法,用途,貯存方法,計算化學數據,
物化性質
其結晶為白色固體Bi2(SO4)3·nH2O(n=2或7), 它與釔、鑭、鐠的硫酸鹽同晶型。硫酸鉍在400℃以下穩定,在400℃以上分解為鹼式鹽和氧化鉍,加熱至465℃分解放出三氧化硫。硫酸鉍遇水水解產生不溶的鹼式鹽Bi(OH)3·Bi(OH)SO4。
合成方法
將10g金屬鉍慢慢加入到20mL濃硝酸中,使其全部溶解。這一步也可用硝酸來溶解三氧化二鉍Bi2O3。往溶液中加入15mL濃硫酸,加熱濃縮即可生成無色沉澱。在250~300℃的溫度下進一步加熱並蒸發至乾,加熱至最後重量不再減少為止。此時即獲得硫酸鉍的結晶。此外,在濃硫酸中的硫酸鉍不存在單獨的Bi3+,而是一系列的配位離子。
2、直接將三氧化二鉍Bi2O3或氫氧化鉍溶於熱的濃硫酸也可製得硫酸鉍。
用途
1、測定其他金屬硫酸鹽;
2、用作藥物,用於製藥工業,也用作分析試劑。
貯存方法
密封保存。
計算化學數據
1、疏水參數計算參考值(XlogP):無
2、氫鍵供體數量:0
3、氫鍵受體數量:12
4、可旋轉化學鍵數量:0
5、互變異構體數量:無
6、拓撲分子極性表面積:266
7、重原子數量:17
8、表面電荷:0
9、複雜度:62.2
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量:5
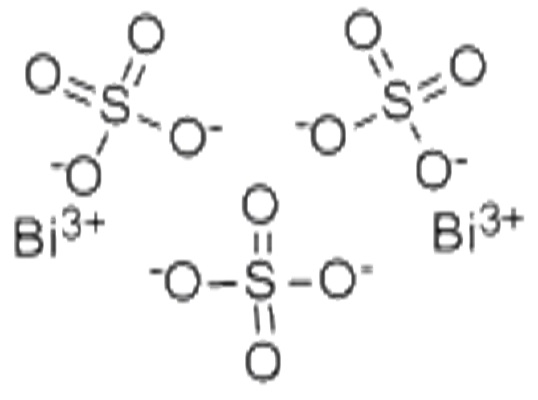
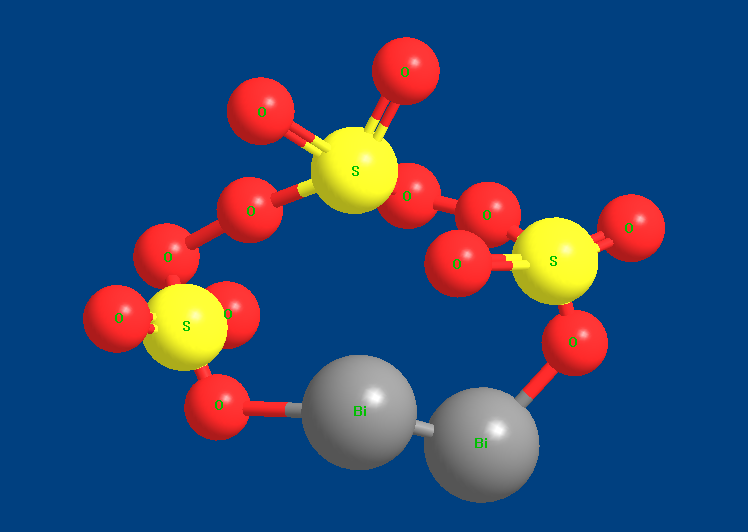 Bi2(SO4)3 3D結構
Bi2(SO4)3 3D結構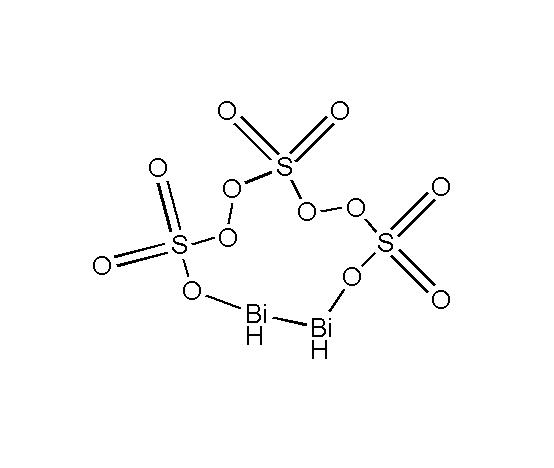 Bi2(SO4)3
Bi2(SO4)3