基本介紹
- 中文名:硫代硫酸
- 英文名:thiosulfuric acid
- 化學式:H2S2O3
- 分子量:114.14
- 穩定性:很不穩定
- Ka1:0.25
- Ka2:1.9×10^-2
基本信息
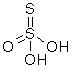


硫代硫酸是指硫酸(H2SO4)中的一個氧原子被硫原子取代的產物(H2S2O3或H2SO3S),兩個硫原子的平均氧化數為+2。其中一個硫原子氧化數為+6(或+4),另一個...
硫代硫酸鈉,又名次大蘇打、海波(來源於其別名 sodium hyposulfite)。它是常見的硫代硫酸鹽,無色透明的單斜晶體。 硫代硫酸鈉易溶於水,遇強酸反應產生硫和二氧化硫...
硫代硫酸銨是一種化學物質,分子式(NH4)2S2O3,常溫下為白色晶體,極易溶於水。...... 硫代硫酸銨是一種化學物質,分子式(NH4)2S2O3,常溫下為白色晶體,極易...
注射用硫代硫酸鈉,適應症為主要用於氰化物中毒,也可用於砷、汞、鉛、鉍、碘等中毒。...
硫代硫酸鈉注射液,適應症為主要用於氰化物中毒,也可用於砷、汞、鉛、鉍、碘中毒。...... 化學名稱:硫代硫酸鈉 分子式:Na2S2O3·5H2O 分子量:248.19 輔料為:...
粗硫代硫酸鈉(crude sodium thiosulfate)為無色單斜晶體,分子式為Na2S2O3,密度為1.667g/cm3。它的五水鹽(Na2S2O3·5H2O)俗稱大蘇打,熔點為48.5℃,密度為1...
硫代硫酸鈉溶液(Sodium thiosulfate)具有還原特性,與亞硝酸鹽配合套用於氰化物中毒,使解毒效果顯著提高,和砷、鉍、汞、碘、鉛燈光生成毒性低的硫化物隨尿排出。硫代...
硫代酸鹽是由金屬陽離子或銨根和硫代酸根組成的鹽類。...... 硫代酸鹽種類繁多,酸式硫代酸鹽較少,硫在其中多顯負價(硫代硫酸中取代氧的硫亦如此),具有還原性。...
硫代硫酸鈉五水合物,無色單斜晶繫結晶,無臭,有清涼帶苦的味道。線性分子式為 Na2S2O3·5H2O。...
硫代硫酸鈉,PT是一種化學物質,分子式是Na2S2O3·5H2O。...... 硫代硫酸鈉,PT是一種化學物質,分子式是Na2S2O3·5H2O。中文名 硫代硫酸鈉,PT 外文名 Sodium ...
