形態結構
病毒外形呈彈狀(60~400nm×60~85nm),一端純圓,一端平凹,有囊膜,內含衣殼呈螺旋對稱。核酸是單股不分節負鏈
RNA。
基因組長約12kb,從3′到5′端依次為編碼N、M1、M2、G、L蛋白的5個
基因,各個基因間還含非編碼的間隔序列。五種蛋白都具有
抗原性。M1、M2蛋白分別構成衣殼和囊膜的基質。L蛋白為聚合酶。
G蛋白在囊膜上構成病毒刺突,與病毒致病性有關,N蛋白為核蛋白有保護RNA功能。G蛋白和N蛋白是狂犬病病毒的主要抗原,刺激機體可誘生相應抗體和
細胞免疫。過去一直認為G蛋白是唯一誘生中和抗體,並能提供狂犬病保護性免疫的抗原。而近年研究表明,除G蛋白外,該病毒的核糖核蛋白(
RNP)在誘生保護性免疫應答上也起重要作用。
 狂犬病病毒
狂犬病病毒狂犬病病毒
宿主範圍廣,可感染鼠,家兔、
豚鼠、
馬、
牛、
羊、犬、貓等,侵犯中樞神經細胞(主要是大腦
海馬回錐體細胞)中增殖,於細胞漿中可形成嗜酸性包涵體(
內基氏小體Negri body)。在人
二倍體細胞、
地鼠腎細胞、雞胚、鴨胚細胞中增養增殖,藉此可用於製備
組織培養疫苗。
抗原型與變異
狂犬病病毒僅一種血清型,但其毒力可發生變異。從自然感染動物體內分離的病毒株稱野毒株(Wild strain)或街上毒株 (Street strain),致病力強,自腦外接種易侵入腦組織及
唾液腺。將野毒株在家兔腦內連續傳50代後,家兔致病潛伏期逐漸縮短,2~4周縮短至4~6日,如再繼續傳代不再縮短,稱固定毒株 (Fixed Strain) ,固定毒株對人及動物致病力弱,腦外接種不侵入腦內增殖,不引起狂犬病,
巴斯德首先創用固定制成減毒活疫苗,預防狂犬病。
抵抗力
狂犬病病毒對熱、紫外線、日光、乾燥的抵抗力弱,加溫50℃1小時、60℃5分鐘100℃2分鐘、高壓鍋110℃1分鐘即死,也易被
強酸、
強鹼、甲醛、碘、乙酸、
乙醚、肥皂水及離子型和非離子型
去污劑滅活。於4℃可保存一周,如置50%甘油中於室溫下可保持活性1周。
狂犬病的分型
用血清學方法可將狂犬病毒屬分為4 個血清型,Ⅰ型病毒有CVS 原型株、古典RV、街毒和疫苗株,血清Ⅱ、Ⅲ及Ⅳ型病毒為狂犬病相關病毒, 其原型株分別為Lagos bat、Mokola 和Duvenhage 病毒。
1993 年,Bourhy 等人根據核蛋白基因N 端的500 個鹼基的同源性將狂犬病毒屬(Lyssavirus)分為6 個基因型:基因1~4 型分別對應於血清Ⅰ~Ⅳ型,從德國和芬蘭蝙蝠中分離到的2 株歐洲狂犬病毒EBLV-1、EBLV-2 為基因型5 和6。1996 年7 月, 澳大利亞首次報導了發現
於果蝠體內的Lyssavirus,被定為基因7 型,即ABLV。在中亞吉爾吉斯斯坦的小鼠耳蝠(Myotis blythi)中分離到Aravan 病毒,對其N基因及推導的胺基酸序列進行分析,發現它與已知的7 個基因型的病毒均有明顯區別,MAbs 檢測其抗原特性與其他類型的病毒也有區別,因此有人認為這是一種新的基因型
致病免疫
致病性
狂犬病是人獸共患性疾病,主要在野生動物及家畜中傳播。人狂犬病主要被患病動物咬傷所致,或與畜密切接觸有關。也可能通過不顯性皮膚或黏膜而傳播,如狗舔肛門,宰狗、切狗肉等引起感染。並有
角膜移植引起感染的報告。在大量感染蝙蝠的密集區,其
分泌液造成氣霧,可引起
呼吸道感染。
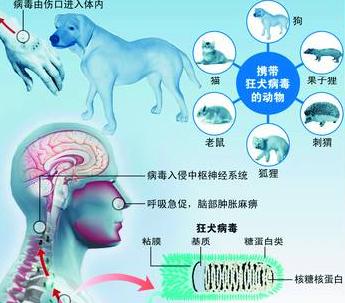 狂犬病病毒
狂犬病病毒人被咬傷後,病毒進入傷口 ,先在該部
周圍神經背根神經節內,沿著傳入感覺神經纖維上行至
脊髓后角,然後散布到脊髓和腦的各部位內增殖損害。在發病前數日,病毒從腦內和脊髓沿傳出神經進入唾液腺內增殖,不斷隨唾液排出。潛伏期1~2個月,短者5~10天,長者1年至數年。潛伏期的長短取決於咬傷部位與頭部距離遠近、傷口的大小、深淺、有無衣服阻擋,以及侵入病毒的數量。有人認為病毒在犬群多次傳播後毒力增強,可縮短潛伏期。
人發病時,先感不安,頭痛,發熱,侵入部位有刺痛或出現爬蟻走的異常感染。繼而出現
神經興奮性增強,脈速、出汗、
流涎、多淚、
瞳孔放大,吞咽時咽喉肌肉發生
痙攣,見水或其他輕微刺激可引起發作,故又名“恐水病”。最後轉入麻痹、昏迷、呼吸及循環
衰竭而死亡,病程大約5~7日。
免疫性
機體感染病毒後產生的抗體除中和,補體介導溶解和抗體依賴細胞毒作用外,特異性lgG抗體還能提高和調節T細胞對狂犬病病毒抗原反應,是接觸狂犬病病毒後同時注射特異性抗體和疫苗的重要依據。細胞免疫也是抗狂犬病病毒主要免疫之一,如殺傷性T淋巴細胞針對靶抗原G,N蛋白可溶解病毒,單核細胞產生IFN和IL2對抑制病毒複製和抵抗病毒攻擊起重要作用。
微生物學
將咬人的狗捕獲,觀察10~14天,不發病,則可認為未患狂犬病。若觀察期間發病,將它殺死,取腦作
病理切片檢查
包涵體,或用螢光標記抗
狂犬病毒血清染色,檢查抗原,如為陰性,則用10%腦懸液注射小白鼠腦內,發病後取腦組織同上檢測包涵體和抗原,可提高陽率,但需時較長約28天。如於發病前用同位素標記的
合成寡核苷酸探針檢測狂犬病毒RNA,於1-2天就出結果。
患者可採取唾液沉渣塗片,螢光抗體染色檢查細胞內病毒抗原。或發病後2-3天作瞼、頰皮膚活檢,用螢光抗體染色,於
毛囊周圍神經纖維中可找見病毒抗原。亦可將狂犬病毒固定毒株感染細胞製成抗原片,加入不同稀釋病人血清阻止螢光抗體染色以測定抗體,一般24小時可出結果。
防治原則
公共衛生措施
捕殺野犬,加強
家犬管理或口服獸用減毒活疫苗(與食物混合餵食)。預防家畜及野生動物的狂犬病是防止人狂犬病的重要根本措施,其任務涉及面廣,需要全社會的配合支持與理解。
咬傷處理
人被疑似狂犬咬傷時,立即用15%肥皂水沖洗和浸泡傷口 ,再塗75%的酒精或
碘酒(只用於濃度咬傷),然後用
碳酸氫鈉沖洗。
特異預防
用人
狂犬病免疫球蛋白(20IU/kg)或抗狂犬病馬血清(40IU/kg),以1/2時在傷口周圍浸潤注射,其餘作
肌肉注射。同時立即肌內注射人二倍體纖維母細胞
狂犬病疫苗1次,於第一次注射後3,7,14,28天再行注射,共5次,可防止發病。中國套用自製的地鼠腎細胞狂犬病苗,已取得良好效果。目前研製成功狂犬病病毒糖蛋白重組痘苗病毒
疫苗,狂犬病病毒G、N亞平位疫苗等,正在試用中。
特殊情況
狂犬病病毒SRV~9|株是經克隆獲得的中等蝕斑口服
弱毒疫苗候選株,具有安全和
免疫原性較好等優點。本試驗根據狂犬病病毒糖蛋白核苷酸5'末端和3'末端序列設計了一對引物,通過反轉錄-聚合酶鏈式反應(
RT-PCR)分別擴增了SRV~9|及其母源株SAD B19糖蛋白的全長cDNA。測序結果表明,SRV~9|和SAD B19糖蛋白cDNA讀框長1575bp,編碼524胺基酸殘基的多肽。通過和其母源株SAD B19核苷酸序列比較發現,SRV~9|的158、575、931位鹼基分別出現了G→A、A→G和A→G的轉換,相應地導致第53位、192位、311位胺基酸出現了Gly→Gl u、His→Arg、Thr→Ala突變;和中國現行的犬用
疫苗株ERA的核苷酸和胺基酸比較,有10個鹼基不同,7個胺基酸發生改變。經Jameson-Wolf
抗原表位優勢圖分析發現,SRV~9|在192位胺基酸的改變,導致該部位產生了一個新的潛在抗原位點。由於狂犬病病毒糖蛋白是誘導機體產生中和抗體唯一抗原,因此,上述胺基酸的改變可能與其特殊的蝕斑特性和其安全性提高有關。保持對毒株的胺基酸序列分析也是監測其特性的重要手段之一。
傳播渠道
狂犬病病毒最主要的傳播途徑就是感染了狂犬病的動物在咬傷人時,通過唾液使狂犬病毒進入人體,狂犬病毒還可以通過無損傷的正常黏膜進入人體,或帶有狂犬病毒的液體濺入眼睛,通過眼結膜進入人體,但以這種方式進入人體的例子要少得多,另外,通過吸入空氣中帶有狂犬病毒飛沫而感染的例子也很少見,只有空氣中狂犬病毒的濃度達到極高程度時,才可能發生。
 狂犬病疫情呈上升趨勢
狂犬病疫情呈上升趨勢人與人的一般接觸不會傳染狂犬病,理論上只有發了病的狂犬病人咬了健康人,才有使被他咬傷的人得狂犬病的可能,發了病的狂犬病人或發病前幾天的人也有可能通過性途徑把狂犬病毒傳染給對方,狂犬病人污染了用具,他人再通過被污染的用具受到感染的可能性很小,狂犬病人的器官、組織、如
角膜移植給健康人則有極高的危險性。
存活時間
狂犬病毒的體外生存能力很差,離體後很快就會失去活性,一般在體外數分鐘就失去活性,所以狂犬病一般不會通過間接的途徑傳播, 狂犬病毒對酸,鹼,新潔爾滅,福馬林等消毒藥物敏感;70%酒精,0.01%碘液和1%-2%的肥皂水亦能使病毒滅活.通過黏膜感染一般也不發病.
 狂犬病病毒
狂犬病病毒 狂犬病病毒
狂犬病病毒 狂犬病疫情呈上升趨勢
狂犬病疫情呈上升趨勢
