基本信息,藥物說明,藥品名稱,成分,性狀,適應症,製劑,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,有效期,執行標準,藥物分析,來源(名稱)、含量(效價),性狀,鑑別,檢查,含量測定,方法名稱,套用範圍,方法原理,
基本信息
中文名稱:烏苯美司
中文別名:[S-(R*,S*)]-N-(3-氨基-2-羥基-1-氧代-4-苯丁基)-L-亮氨酸;貝他定;N-[(2S,3R)-3-氨基-2-羥基-4-苯丁醯]-L-亮氨酸;N-[(2S,3R)-3-氨基-2-羥基-4-苯基丁醯基]-L-亮氨酸;([2S,3R]-3-氨基-2-羥基-4-苯基丁醯基)-L-亮氨酸;
英文名稱:Ubenimex
英文別名:nk421;BENIMEX;BESTATIN;Bestatin,UbeniMex;
CAS號:58970-76-6
分子式:C16H24N2O4
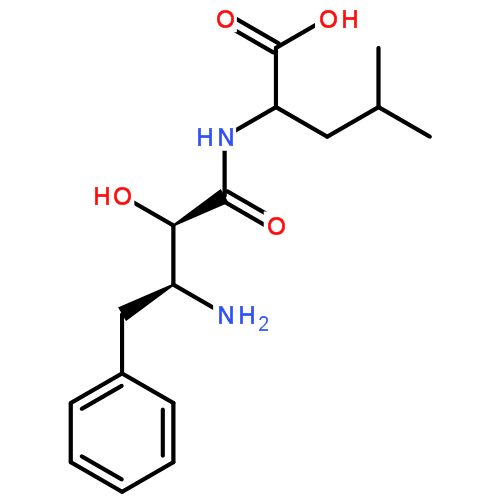
結構式:
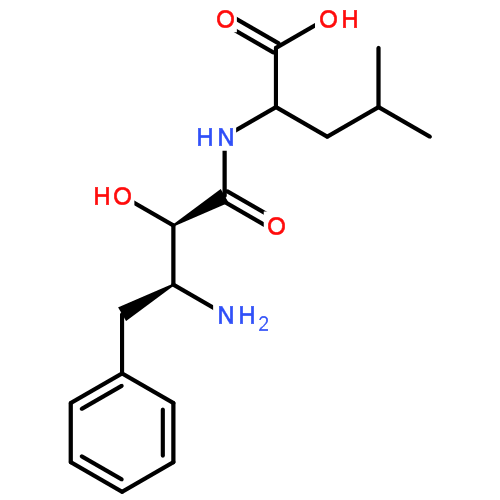 烏苯美司結構式
烏苯美司結構式分子量:308.37300
精確質量:308.17400
PSA:112.65000
LogP:1.62400
物化性質
外觀與性狀:白色結晶粉末
密度:1.197 g/cm
熔點:245°C (dec.)(lit.)
沸點:604.7ºC at 760 mmHg
閃點:319.5ºC
折射率:1.557
穩定性:常溫常壓下穩定
儲存條件:通風低溫乾燥,與庫房食品原料分開存放
藥物說明
藥品名稱
通用名:烏苯美司
英文名:Ubenimex
漢語拼音:
膠囊:Wubenmeisi Jiaonang
片劑:Wubenmeisi Pian
成分
化學結構式:
分子式C16H24N2O4
分子量:308.38
性狀
本品內容物為白色粉末。
適應症
本品可增強免疫功能,用於抗癌化療、放療的輔助治療,老年性免疫功能缺陷等。可配合化療、放療及聯合套用於白血病、多發性骨髓瘤、骨髓增生異常綜合症及造血幹細胞移植後,以及其它實體瘤患者。
製劑
口服片劑或膠囊
規格
10mg
用法用量
成人,一日30mg(3粒),1次(早晨空腹口服)或分3次口服;兒童酌減。症狀減輕或長期服用,也可每周服用2~3次,10個月為一療程。
不良反應
劑量超過200mg/日,可使T細胞減少。偶有皮疹、瘙癢、頭痛、面部浮腫和一些消化道反應,如噁心、嘔吐、腹瀉、軟便。個別可出現一過性輕度AST升高。一般在口服過程中或停藥後消失。
禁忌
未進行該項實驗且無可靠參考文獻。
注意事項
未進行該項實驗且無可靠參考文獻。
孕婦及哺乳期婦女用藥
安全性尚未確定,宜慎用。
兒童用藥
嬰幼兒用藥的安全性尚未確定,宜慎用。
老年用藥
未進行該項實驗且無可靠參考文獻。
藥物相互作用
尚未明確。
藥物過量
未進行該項實驗且無可靠參考文獻。
藥理毒理
本品從鏈黴菌屬(Streptomyces ofivorecticuli)的培養液中分離所得的二肽化合物,可競爭性地抑制氨肽酶N(aminopeptidase N/CD13)及亮氨酸肽酶(Leucineamino-Peptidase)。增強T細胞的功能,使NK細胞的殺傷活力增強,且可使集落刺激因子合成增加而刺激骨髓細胞的再生及分化。本品能幹擾腫瘤細胞的代謝,抑制腫瘤細胞增生,使腫瘤細胞凋亡,並激活人體細胞免疫功能,刺激細胞因子的生成和分泌,促進抗腫瘤效應細胞的產生和增殖。
藥代動力學
本品口服吸收良好、迅速,1小時後血藥濃度達峰值。約有15%在肝中被代謝為羥基烏苯美司。80%~85%呈原形自尿排出。
貯藏
密閉保存。
有效期
36個月
執行標準
《中國藥典》2010版二部
藥物分析
來源(名稱)、含量(效價)
本品為N-[(2S,3R)-3-氨基-2-羥基-4-苯基丁醯]-L-亮氨酸。按乾燥品計算,含C16H24N2O4不得少於98.5%。
性狀
本品為白色結晶性粉末;無臭,味苦。
本品在水或甲醇中微溶;在冰醋酸中易溶,在0.1mol/L鹽酸溶液或0.1mol/L氫氧化鈉溶液中溶解。
比旋度
取本品,精密稱定,加0.1mol/L鹽酸溶液溶解並定量稀釋製成每1ml中約含10mg的溶液,依法測定(2010年版藥典二部附錄Ⅵ E),比旋度為-15.0°至-18.0°
鑑別
(1)取本品約5mg,加1mol/L氫氧化鈉溶液0.5ml與硫酸銅試液1滴,顯深藍色。
(2)取本品約10mg,加20%醋酸溶液2ml、茚三酮約5mg與1mol/L氫氧化鈉溶液2滴,加熱,溶液漸顯藍紫色。
(3)取本品與烏苯美司對照品適量,用30%醋酸溶液分別溶解製成每1ml中含1mg的供試品溶液與對照品溶液,照有關物質項下的色譜條件試驗,供試品溶液主峰的保留時間應與對照品溶液主峰的保留時間一致。
(4)本品的紅外光吸收圖譜應與對照的圖譜(《藥品紅外光譜集》911圖)一致。
檢查
1酸度
取本品0.25g,加水25ml振搖,濾過,取濾液,依法測定(2010年版藥典二部附錄Ⅵ H),pH值應為4.5~7.0。
2有關物質
取本品,加30%醋酸溶液溶解並稀釋製成每1ml中約含10mg的溶液,作為供試品溶液;精密量取適量,用30%醋酸溶液定量稀釋製成每1ml中含0.1mg的溶液,作為對照溶液。照高效液相色譜法(2010年版藥典二部附錄ⅤD)試驗。用十八烷基矽烷鍵合矽膠為填充劑;以甲醇-0.6%磷酸二氫鈉溶液(45:55)為流動相,柱溫40℃;檢測波長為254nm。理論板數按烏苯美司峰計算不低於2500。取對照溶液20μl注入液相色譜儀,調節檢測靈敏度,使主成分色譜峰的峰高約為滿量程的10%。再精密量取供試品溶液與對照溶液各20μl,分別注入液相色譜儀,記錄色譜圖至主成分峰保留時間的2倍。供試品溶液的色譜圖中如有雜質峰,各雜質峰面積的和不得大於對照溶液主峰面積(1.0%)。
3乾燥失重
取本品,在105℃乾燥至恆重,減失重量不得過0.5%(2010年版藥典二部附錄ⅧL)。
4熾灼殘渣
取本品1.0g,依法檢查(2010年版藥典二部附錄Ⅷ N),遺留殘渣不得過0.1%
5重金屬
取熾灼殘渣項下遺留的殘渣,依法檢查(2010年版藥典二部附錄Ⅷ H第二法),含重金屬不得過百萬分之二十。
含量測定
取本品約0.25g,精密稱定,加冰醋酸30ml使溶解,照電位滴定法(2010年版藥典二部附錄Ⅶ A),用高氯酸滴定液(0.1mol/L)滴定,並將滴定的結果用空白試驗校正。每1ml的高氯酸滴定液(0.1mol/L)相當於30.84mg的C16H24N2O4。
方法名稱
烏苯美司原料藥—烏苯美司的測定—電位滴定法
套用範圍
本方法採用滴定法測定烏苯美司原料藥中烏苯美司的含量。本方法適用於烏苯美司原料藥。
方法原理
供試品加冰醋酸溶解後,用高氯酸滴定液進行電位滴定,並將滴定的結果用空白試驗校正,根據滴定液使用量,計算烏苯美司的含量。
試劑:
1. 冰醋酸
2. 高氯酸滴定液(0.1mol/L)
3.結晶紫指示液
4 .基準鄰苯二甲酸氫鉀
儀器設備: 電位滴定儀
試樣製備: 1.高氯酸滴定液(0.1mol/L)
配製:取無水冰醋酸(按含水量計算,每1g水加醋酐5.22mL)750mL,加入高氯酸(70~72%)8.5mL,搖勻,放冷,加無水冰醋酸適量使成1000mL,搖勻,放置24小時。若所測供試品易乙醯化,則須用水分測定法測定本液的含水量,再用水和醋酐調節至本液的含水量為0.01%~0.2%。
標定:取在105℃乾燥至恆重的基準鄰苯二甲酸氫鉀約0.16g,精密稱定,加無水冰醋酸20mL使溶解,加結晶紫指示液1滴,用本液緩緩滴定至藍色,並將滴定結果用空白試驗校正。每1mL高氯酸滴定液(0.1mol/L)相當於20.42mg的鄰苯二甲酸氫鉀。根據本液的消耗量與鄰苯二甲酸氫鉀的取用量,算出本液的濃度。
2. 結晶紫指示液
取結晶紫0.5g,加冰醋酸100mL使溶解
操作步驟: 精密稱取供試品約0.25g,加冰醋酸30mL使溶解,照電位滴定法,用高氯酸滴定液(0.1mol/L)滴定,並將滴定的結果用空白試驗校正。每1mL高氯酸滴定液(0.1mol/L)相當於30.84mg的C16H24N2O4。
註:“精密稱取”系指稱取重量應準確至所稱取重量的千分之一。“精密量取”系指量取體積的準確度應符合國家標準中對該體積移液管的精度要求。
 烏苯美司結構式
烏苯美司結構式