溶液百分比濃度(濃度可以用一定的溶液中溶質的克數、克分子數或克當量數計算。)是指溶液(一般用單位溶液)所含溶質的重量的百分比。
一種可溶物質溶於一種溶劑後,在該溶劑的分布密度以百分比的方式表示,稱為溶液百分比濃度(溶液質量分數),常用C%來表示(也可表示為w)。
基本介紹
- 中文名:溶液百分比濃度
- 分 類:質量濃度
- 意 義:是溶液濃稀程度的標準
- 公 式:溶質質量/溶液質量×100%
意義

溶液百分比濃度(濃度可以用一定的溶液中溶質的克數、克分子數或克當量數計算。)是指溶液(一般用單位溶液)所含溶質的重量的百分比。
一種可溶物質溶於一種溶劑後,在該溶劑的分布密度以百分比的方式表示,稱為溶液百分比濃度(溶液質量分數),常用C%來表示(也可表示為w)。

溶液百分比濃度(濃度可以用一定的溶液中溶質的克數、克分子數或克當量數計算。)是指溶液(一般用單位溶液)所含溶質的重量的百分比。一種可溶物質溶於一種溶劑後,...
是分析化學中的一個名詞。含義是以1升溶液中所含溶質的摩爾數表示的濃度。以單位體積里所含溶質的物質的量(摩爾數)來表示溶液組成的物理量,叫作該溶質的摩爾...
質量百分比濃度即質量分數,是物理學術語,用來表述單位質量的溶液中含有某物質的百分比。...
體積百分比濃度在相同的溫度和壓力下,物質B的體積VB與溶液的體積V之比,稱為物質B的體積分數,又稱體積百分比,符號為φB,表達式為φB=×100%...
一種可溶物質溶於一種溶劑後,在該溶劑的分布密度以百分比的方式表示,稱為溶液百分比濃度(溶液質量分數)常用C%來表示(也可表示為w)...
溶液濃度可分為質量濃度(如質量百分濃度)和體積濃度(如摩爾濃度、當量濃度)兩類質量百分濃度溶液的濃度用溶質的質量占全部溶液質量的百分率表示的叫質量百分濃度, 用...
福爾摩斯由於長期注射百分之七濃度的古柯鹼溶液而神經失常,在住院接受弗洛伊德治療時發現一樁大案,兩人合作偵破,推遲了戰爭。[1] 百分之七溶液作者簡介 編輯 ...
溶液中各組分含量的比值,用來表示溶液的濃度。...... 也叫重量百分濃度,是溶質重量與溶液總重量之比。例如,5.0克氯化鈉和95克水組成的溶液中,氯化鈉的重量百分數...
一定比例,所有二價離子的活度以該比例的平方改變,所有三價離子的活度以該比例的三次方改變,則溶液濃度的改變將不破壞原來溶液的平衡,土壤吸附的各種陽離子的比例也...
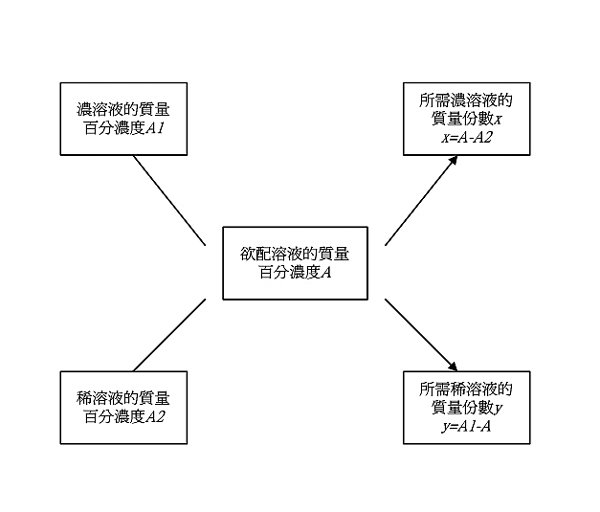
同一物質的甲、乙兩溶液的百分比濃度分別為a%、b%(a%>b%),現用這兩種溶液配製百分比濃度為c%的溶液。問取這兩種溶液的質量比應是多少?...
波美度(°Bé)是表示溶液濃度的一種方法。把波美比重計浸入所測溶液中,得到的度數就叫波美度。
配製百分比濃度溶液百分比濃度溶液的稀釋方法摩爾和分子量的概念摩爾濃度摩爾濃度溶液的稀釋方法摩爾濃度轉換為百分比濃度百分比濃度轉換為摩爾濃度...
