溶出伏安法又稱反向溶出極譜法,這種方法是使被測的物質,在待測離子極譜分析產生極限電流的電位下電解一定的時間,然後改變電極的電位,使富集在該電極上的物質重新溶出,根據溶出過程中所得到的伏安曲線來進行定量分析。
基本介紹
- 中文名:溶出伏安法
- 又稱:反向溶出極譜法
- 原理:由溶出過程中所得到的伏安曲線
- 套用:金屬離子的檢測
介紹
基本原理
溶出伏法(stripping voltammetry)包含電解富集和電解溶出兩個過程。
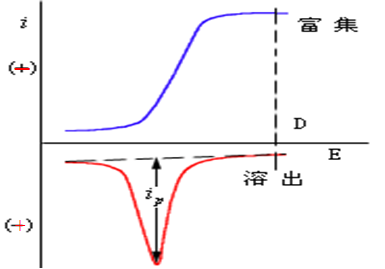 陽極溶出伏安法極化曲線
陽極溶出伏安法極化曲線溶出伏安法又稱反向溶出極譜法,這種方法是使被測的物質,在待測離子極譜分析產生極限電流的電位下電解一定的時間,然後改變電極的電位,使富集在該電極上的物質重新溶出,根據溶出過程中所得到的伏安曲線來進行定量分析。
 陽極溶出伏安法極化曲線
陽極溶出伏安法極化曲線溶出伏安法又稱反向溶出極譜法,這種方法是使被測的物質,在待測離子極譜分析產生極限電流的電位下電解一定的時間,然後改變電極的電位,使富集在該電極上的物質重新...
陽極溶出伏安法是指在一定的電位下,使待測金屬離子部分地還原成金屬並溶入微電極或析出於電極的表面,然後向電極施加反向電壓,使微電極上的金屬氧化而產生氧化電流,...
《化學試劑:陽極溶出伏安法通則(GB/T 3914-2008)》代替GB/T 3914—1983《化學試劑——陽極溶出伏安法通則》,與GB/T 3914—1983相比主要變化如下:修改了範圍(...
採用電化學分析法進行痕量元素測定,除用懸汞電極溶出伏安法測定Cu、Pb、Cd、Zn、S等元素外,近年來發展了玻璃碳電極鍍金膜溶出伏安法測定某些重金屬元素。另外用金...
根據電解過程中的電流電壓曲線(伏安曲線)來進行分析的方法。電化學分析法溶出伏安法 將恆電位電解富集法與伏安法結合的一種極譜分析方法。它首先將欲測物質在適當...
例如“三辛基氧化膦修飾電極三元絡合物體系測定銪(Ⅲ)的研究”;“痕量鉛在草酸修飾電極上陽極溶出伏安法的研究”;“硫辛酸修飾碳纖維微電極在抗壞血酸存在下選擇性...
控制電位極譜法包括直流極譜法、交流極譜法、單掃描極譜法、方波極譜法、脈衝極譜法等。控制電流極譜法有示波極譜法。此外還有極譜催化波、溶出伏安法。...
3.5.5 研磨溶出伏安法3.5.6 套用3.6 流動分析3.6.1 原理3.6.2 電解池設計3.6.3 傳質與電流回響3.6.4 檢測模式例題思考題與習題參考文獻...
發表了多篇化學方面的論文《SH-84型精密擠壓式懸汞電極的研製》(與金文睿等人合作,發表於《分析化學》1986年第二期;《陽極溶出伏安法測定水中痕量鉛》、《極譜法...
吸收光譜——又可分為火焰原子化法與無火焰電熱原子化法、等離子發射光譜法、原子螢光光度法等)和電化學分析法(包括極譜催化波法、陽極溶出伏安法及離子選擇電極法...
中國法醫學報,1988;3(4):214-216 94. 喬文建,丁虹. 痕量銅在8-羥基喹啉修飾電極上催化溶出伏安法的研究. 高等學校化學學報1991,12(9):175-177丁虹會議論文 ...
如國標中鉛的測定方法中的第五法和鉻的測定方法的第二法均為示波極譜法。陽極溶出伏安法是將恆電位電解富集與伏安法測定相結合的一種電化學分析方法。這種方法...
其檢測限可達ng/ml水平運用檢測MT的電化學檢測方法有:示差脈衝極譜法(DPP)、微分脈衝極譜法、示差脈衝陽極溶出伏安法(DPASV)和循環伏安法(CV)等。[1] ...
實驗6 陽極溶出伏安法測定水樣中的痕量錒和鉻儀器分析實驗第二章 分子光譜分析實驗 2.1 紫外一可見分光光度法2.2 紅外吸收光譜法...
12.4 溶出伏安法的電極體系12.5 溶出伏安法在醫藥衛生領域中的套用第三篇 色譜法第13章 色譜法基礎13.1 概述13.2 色譜流出曲線和常用色譜參數...
7、湖南省科技廳項目,納米顆粒編碼結合陽極溶出伏安法的DNA單鹼基突變檢測技術研究(項目主持人)8、湖南省教育廳重點項目,生物活性物質的雙光子螢光探針的設計合成及其...
(1) 無火焰原子吸收分光光度法 (2) 陽極溶出伏安法 (3) 雙硫腙分光光度法 0.19×10-3 4.0×10-3 2.6×10-3 HY 003.4-91 HY 003.4-91 HY ...
第六節 電化學分析法94一、電化學分析法的種類和特點94二、電位分析法96三、極譜分析法110四、溶出伏安法117第三章 分析套用技術120...
而且還能與測定方法(如脈衝伏安、溶出伏安法等)的靈敏性和修飾劑化學反應的選擇性相結合,因此可以認為化學修飾電極是把分離、富集和選擇性測定三者合而為一的一種...
對於比較簡單的化學形態分析,某些方法可直接完成,如用分光光度法分析某些同一元素的不同價態,陽極溶出伏安法分離分析穩定態與不穩定態金屬等。而對於複雜的化學形態...
實驗8陽極溶出伏安法測定海水中的鉛含量22012 2設計性實驗22112 2 1實驗目的22112 2 2基本內容和要求22112 2 3實驗方案設計備選題目22112 3設計性實驗示例222...
