基本介紹
- 中文名:洗氣
- 對象:洗氣的對象為水蒸氣
- 濃硫酸:適用範圍:中性及酸性氣體
- 不適用範圍::有機不飽和化合物
常見乾燥劑,酸性乾燥劑,鹼性乾燥劑,中性乾燥劑,鹽類乾燥劑,洗氣的舉例,洗氣方式,物理方式,化學方式,注意事項,
常見乾燥劑
:
酸性乾燥劑
1、濃硫酸:
適用範圍:中性及酸性氣體。
2、五氧化二磷:
適用範圍:主要用於乾燥有機物,由於生成的磷酸會覆蓋表面,所以常與載體連用。
不適用範圍:醇 有機酸 HCl(鹽酸) HF(氫氟酸)等。
3、十氧化四磷:主要用於乾燥濃硫酸。
鹼性乾燥劑
2、金屬鈉:用於乾燥非極性有機物,不能幹燥含水量過多的物質,否則有危險。
中性乾燥劑
鹽類乾燥劑
洗氣的舉例
2、 通過盛氫氧化鈉溶液的洗氣瓶
3、 通過盛有灼熱氧化銅的試管
這裡面是除去三種氣體,很明顯,濃硫酸是除去水蒸氣的;氫氧化鈉是除去二氧化碳的(但是注意,氣體從氫氧化鈉溶液裡面出來會帶出水蒸氣,所以,這步必須放在濃硫酸的前面,);灼熱氧化銅,是用來除去氫氣的,這個跟2差不多,氫氣被還原以後,也會生成水,所以正確的操作順序應該是231 。
最後總結,除去氣體,有水,水通常放最後除去。
檢驗氣體,檢驗水,水通常放第一步除去。
認為是231
不用3做為第一個的理由是。CO2+H2=CO+H2O (合成水煤氣的反應、要加熱)
引入CO後無法在後二個步驟中除去。
所以先通過2,除去CO2。
再通過3,除去H2,這裡會有水生成了。
最後通過1,完全將水除去。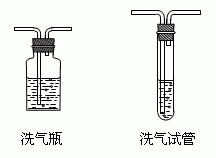 洗氣裝置
洗氣裝置
 洗氣裝置
洗氣裝置洗氣方式
物理方式
氣體中需要被去除的雜質在洗液中溶解度較大,並且雜質氣體僅僅是單純的溶解於洗液。
化學方式
注意事項
直型玻璃管(盛固),接短進短出。
裝置:廣口瓶或試管(盛液),長進短出。
溶液不會與所要提純的氣體發生化學或物理反應。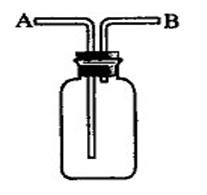 洗氣瓶
洗氣瓶
 洗氣瓶
洗氣瓶溶液在除去混合氣中非目的氣時不會產生新的雜質氣體。

