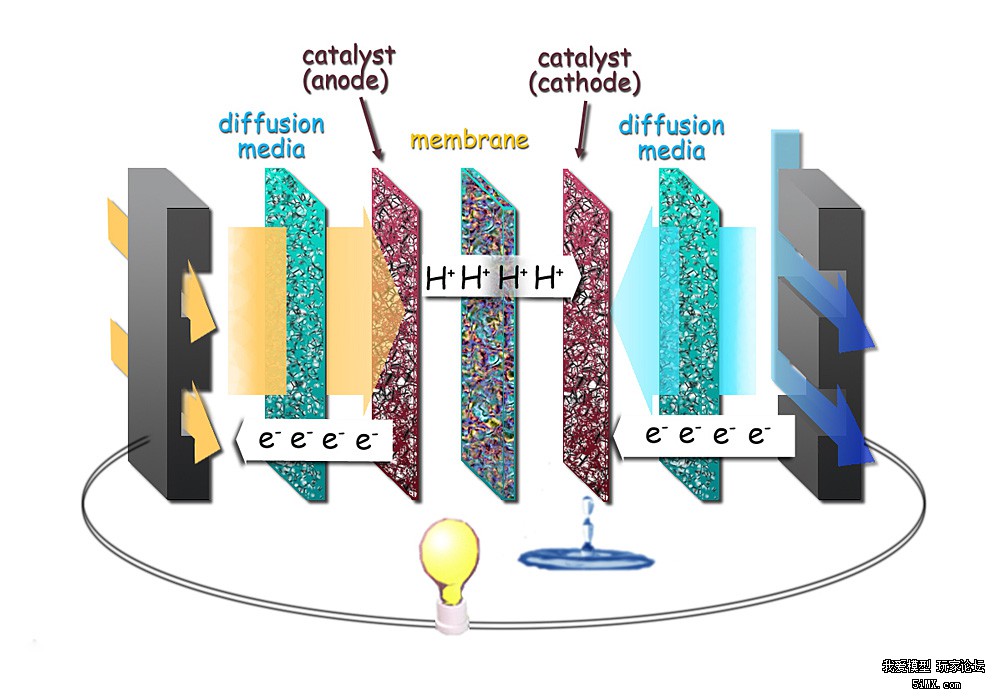
概述
燃料電池是很有發展前途的新的動力電源,一般以氫氣、碳、甲醇、硼氫化物、煤氣或天然氣為燃料,作為負極,用空氣中的氧作為正極.和一般電池的主要區別在於一般電池的活性物質是預先放在電池內部的,因而電池容量取決於貯存的活性物質的量;而燃料電池的活性物質(燃料和氧化劑)是在反應的同時源源不斷地輸入的,因此,這類電池實際上只是一個能量轉換裝置。這類電池具有轉換效率高、容量大、比能量高、功率範圍廣、不用充電等優點,但由於成本高,系統比較複雜,僅限於一些特殊用途,如飛船、潛艇、軍事、電視中轉站、燈塔和浮標等方面。
原理
氫-空氣-水系統工作時,向氫電極供應氫氣,同時向氧電極供應氧氣。氫、氧氣在電極上的催化劑作用下,通過電解質生成水。這時在氫電極上有多餘的電子而帶負電,在氧電極上由於缺少電子而帶正電。接通電路後,這一類似於燃燒的反應過程就能連續進行。
工作時向負極供給燃料(氫),向正極供給氧化劑(氧氣)。氫在負極上的催化劑的作用下分解成正離子H+和電子e-。氫離子進入電解液中,而電子則沿外部電路移向正極。用電的負載就接在外部電路中。在正極上,氧氣同電解液中的氫離子吸收抵達正極上的電子形成水。這正是水的電解反應的逆過程。
氫-空氣-水系統不需要將還原劑和氧化劑全部儲藏在電池內的裝置。氫-空氣-水系統的反應物都在電池外部它只是提供一個反應的容器。氫氣和氧氣都可以由電池外提供。
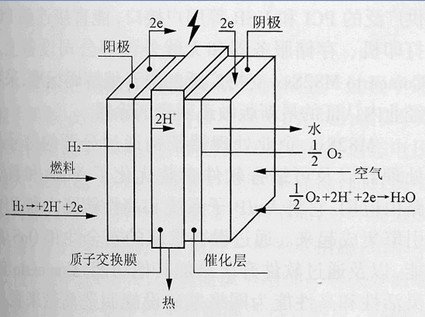 燃料電池系統
燃料電池系統反應過程
利用這個原理,燃料電池便可在工作時源源不斷地向外部輸電,所以也可稱它為一種"發電機"。一般來講,書寫燃料電池的化學反應方程式,需要高度注意電解質的酸鹼性。 在正、負極上發生的電極反應不是孤立的,它往往與電解質溶液緊密聯繫。如氫-空氣-水系統有酸式和鹼式兩種:
若電解質溶液是鹼、鹽溶液則
若電解質溶液是酸溶液則
在鹼溶液中,OHˉ含量極高,故負極處生成的H+會直接與OHˉ結合生成水,而正極處生成的OHˉ由於缺少H+結合而以離子的形態存在。酸性溶液則正好相反。
系統分類
氫-空氣-水系統按電池結構和工作方式分為離子膜、培根型和石棉膜三類。
(1)離子膜氫-空氣-水系統:用
陽離子交換膜作電解質的酸性燃料電池,現代採用全氟磺酸膜。電池放電時,在氧電極處生成水,通過燈芯將水吸出。這種電池在常溫下工作、結構緊湊、重量輕,但離子交換膜內阻較大,放電電流密度小。
(2)培根型燃料電池系統:屬鹼性電池。氫、氧電極都是雙層多孔鎳電極(內外層孔徑不同),加鉑作催化劑。電解質為80%~85%的苛性鉀溶液,室溫下是固體,在電池工作溫度(204~260°C)下為液體。這種電池能量利用率較高,但自耗電大,起動和停機需較長的時間(起動需24小時,停機17小時)。
(3)石棉膜燃料電池系統:也屬鹼性電池。氫電極由多孔鎳片加鉑、鈀催化劑製成,氧電極是多孔銀極片,兩電極夾有含35%苛性鉀溶液的石棉膜,再以有槽鎳片緊壓在兩極板上作為集流器,構成氣室,封裝成單體電池。放電時在氫電極一邊生成水,可以用循環氫的辦法排出,亦可用靜態排水法。這種電池的起動時間僅15分鐘,並可瞬時停機。
 原理示意圖
原理示意圖主要特點
(1)產物是水,清潔環保;
(2)容易持續通氫氣和氧氣,產生持續電流;
(3)能量轉換率較高,超過80%(普通燃燒能量轉換率30%多);
(4)可以組合為燃料電池發電站,排放廢棄物少,噪音低,綠色發電站。
 燃料電池系統
燃料電池系統

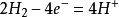


 原理示意圖
原理示意圖