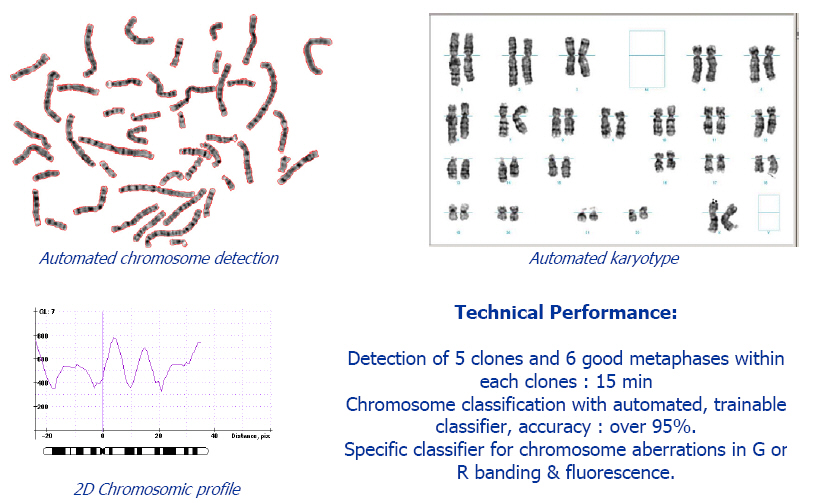
染色體畸變分析實驗是細胞在有絲分裂中期,染色質逐漸變粗變短,而形成染色體,染色體的長短、大小、著絲點等特徵較為顯著,易觀察。觀察到的一切畸變均為來源於不能被修正或不能正常修復時的損傷,裂隙不應記為有意義的畸變,而由多個裂隙引起的易位、放射體環、多著色點等,為遺傳性損傷指標。
基本介紹
- 中文名:染色體畸變分析實驗
- 外文名:Chromosome aberration analysis experiment
- 屬於:毒理學研究方法
- 指標:染色體的易位、放射體環等
- 套用:評價新藥安全性
- 細胞:人外周血淋巴細胞等
染色體畸變實驗,染色體畸變實驗在新藥評價中的套用,套用研究背景,推薦使用的細胞,受試物處理與取樣時間,
染色體畸變實驗
細胞在有絲分裂中期,染色質逐漸變粗變短,而形成染色體,染色體的長短、大小、著絲點等特徵較為顯著,易觀察。觀察到的一切畸變均為來源於不能被修正或不能正常修復時的損傷,裂隙不應記為有意義的畸變,而由多個裂隙引起的易位、放射體環、多著色點等,為遺傳性損傷指標。一般染色體斷裂和再接合時,細胞在第一次分裂後不能再分裂而致死,而對稱性的染色體單體互換、易位、缺失、遺傳上可以存活的易位,這種細胞遺傳的危害可能很大;當每個細胞發生多個染色體畸變比只有單個染色體畸變的損傷更加嚴重;最終遺傳物質是否誘變力陽性時,應全面考慮畸變類型、頻率和剖量關係。實驗組與對照組相比,染色體畸變率有明顯的劑量反應關係,差異有統計學意義,可確認為陽性結果。
染色體畸變實驗在新藥評價中的套用
套用研究背景
日本將體外染色體畸變實驗作為Ames實驗的補充,這兩項體外實驗和一項體內實驗(即小鼠骨髓細胞微核實驗)作為新藥短期致突變實驗的基本組合,對新的工業化合物和農藥的安全性評價也採用類似的方案。據文獻報導,使用原代細胞或已建株的細胞系,用或不用代謝活化系統檢測已知的致癌物約有39%為陽性,在Ames實驗中為陽性的化合物,約79%在染色體畸變實驗中也是陽性,而那些在Ames實驗中為陰性的化合物,在染色體畸變實驗中約有09%仍為陽性。上述結果說明在藥物和化合物的短期致突變實驗評價中,如果只做Ames實驗,許多遺傳毒性化合物將會被認為是無毒的。因此,體外染色體畸變實驗對藥物和各種化合物的潛在性遺傳毒性的安全評價,是一個很有用的補充實驗。但是在上述實驗中,若有一種實驗為陽性,在小鼠體內微核實驗或致癌實驗中,不一定是陽性。如果染色體實驗和Ames實驗均為陽性,特別是體內微核實驗為肯定陽性時,常常在致癌試驗中是陽性結果,土述三種致突變實驗為判斷腫瘤的發生預先提供了信息。
推薦使用的細胞
有文獻報導,採用已建立的細胞系或原代細胞,例如人外周血淋巴細胞或中國倉鼠肺成纖維細胞系(CHL)或中國倉鼠卵巢細胞系(CHO)為常用的實驗材料。套用這些材料的優點是:(1)染色體的數目少,有利於計數分析,細胞的增殖周期短,在簡單的培養基中能生長;(2)同一個細胞系可用於不同的實驗;(3)細胞對S9活化相對穩定;(4)細胞對各種化合物是敏感的。美國國家毒理學計畫(NTP)推薦使用CHO細胞系,日本工作者多使用CHL細胞系。
新藥評價中染色體實驗要求如下:(1)使用原代細胞或已建立的細胞系;(2)至少設計三個劑量組,首先選擇抑制50%細胞生長濃度,當化合物無細胞毒性時,最高濃度應限定在10mmol/L;(3)設溶劑對照和已知斷裂劑作陽性對照,加S9代謝活化和不加S9活化對照;(4)選用合適的代謝活化方法,如選用S9的濃度及合適的代謝活化時間等;(5)細胞經受試物處理後,選擇合適的收穫細胞時間。經受試物作用後細胞周期可能延遲,所以需要兩個不同的取樣時間。每個劑量組至少兩個樣本,每個樣本觀察100箇中期細胞,分析染色體的數目異常和結構畸變;(6)列表統計出染色體畸變率及畸變類型,染色體畸變的分類應遵照國際公認的標準。染色體型畸變和染色單體裂隙應分別統計,對染色體和染色單體裂隙很難確定統一的標準,因此建議各研究者在報告中應註明自己的標準。
受試物處理與取樣時間
通過初試細胞毒性,選擇合適的藥物濃度,.藥物對細胞的毒性及誘發染色體畸變常常是在很窄的劑量水平,經處理24-84h後,根據細胞生長狀況判斷細胞毒性。如果受試物對細胞無毒性,最大劑量可用2=3mg/mol然而對可溶性受試物(例如鹽溶液),最大濃度應限制在10mmol/L,因為通常在此濃度以上時,培養基中的滲透壓開始增加,培養基的pH或滲透壓的改變也許不會直接損傷染色體,但能間接地引起染色體畸變。對不易溶解的藥物,建議用狡甲基纖維素鈉(CMC)懸液作溶劑,因為這種粒子十分微小,能被吞噬細胞所利用。按照OECD對新藥的評價標準,不易溶解的藥物實驗時應做到最大的溶解度,不能用乙醇作為實驗溶劑,因為在培養基中乙醇被轉化為乙醛,可能出現假陽性結果。
化合物與細胞的接觸時間在實驗中是一個關鍵問題,必要時可以連續處理,直到收穫細胞,使細胞在整個實驗中接觸受試物。如果細胞生長不良或沒有觀察到中期分裂相,可更換新鮮的培養液培養。實驗中使用S9混合物時,由於S9本身的細胞毒性作用,細胞不能長時間接觸S9,根據1988年Ishidate介紹的懸孵培養法,細胞懸液與S9隻能接觸l-3h。而用另一種平皿培養法只是單層細胞接觸S9,用這種方法細胞與S9接觸可長達3-6h,這樣可使某些化合物在低劑量水平即能誘發出較多的畸變。
收穫細胞的最佳時間主要取決於使用的細胞種類,、原則上是要使所觀察到的染色體畸變是在受試物處理後的第一個分裂中期。經受試物處理後細胞分裂周期可能延長,所以較長時間的培養可觀察到更多的畸變。許多化合物處理48h比24h會引起更多的畸變。這一結果說明,選擇不同的實驗條件對所得結果可以產生很大的影響。染色體不穩定性畸變與穩定性畸變的關係大部分不穩定性畸變是致死性的,可能產生不了遺傳效應。