基本介紹
性質,製取,毒性,安全極限,
性質
的化學式是S2F10,為五氟化硫的二聚物,在常溫常壓下為易揮發性液體,無色、無臭、無味,化學上極穩定。在水和濃鹼液中分解極慢且不溶於其中,在200至300℃時即完全分解生成SF4和SF6。S2F10是一種劇毒物質,其毒性超過光氣,主要破壞呼吸系統,空氣中含1ppm(百萬分比濃度)時白鼠八小時致死,美國和西德規定在空氣中允許濃度為0.025ppm.英文名稱為disulfur decafluoride。
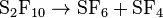 反應
反應- 能與N2F4反應,生成 SF5NF2:
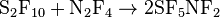 反應
反應- 能與過量的氯氣反應,生成 SF5Cl:
 反應
反應製取
 製取方法
製取方法毒性
十氟化二硫是帶有類似二氧化硫氣味的無色液體或氣體,毒性大約是光氣的四倍。其毒性被認為是由於它在肺中發生歧化反應,生成 SF6 和 SF4;SF6 較不活潑,而 SF4 能與肺中的水反應,生成亞硫酸和氫氟酸,傷害人體:反應如下 反應
反應
 反應
反應安全極限
氟化物等的安全極限
名稱 | 安全極限 | 致死原因 | 說明 |
SF6 | 1000 | >80%(體積) | 美、德規定致死含量為1000 |
SF4 | 0.1 | 德國標準 | |
S2F10 | 0.01 | 1μl/l/18h | 德國標準 |
HF | 3 | 德國標準 | |
SF2 | 5 | 美國標準 | |
SO2 | 5 | 德國標準 | |
COCl2(光氣) | 1 | 25-40μl/l/h | 列出此毒氣作為比較 |

