《利奈唑胺晶型B及其製備方法和用途》是江蘇豪森藥業集團有限公司於2016年1月12日申請的專利,該專利的申請號為2016100178056,公布號為CN105503764A,授權公布日為2016年4月20日,發明人是楊勇、盛志輝、周炳城、喬智濤、陳安豐。
《利奈唑胺晶型B及其製備方法和用途》提供一種利奈唑胺晶型B,該晶型的粉末X-射線衍射圖中,衍射角度2θ(±0.2°)在9.43,11.29,13.27,14.13,15.55,16.69,19.04,21.92和22.35處有特徵吸收峰,且該晶型具有粒徑小、溶出度好等優點,該發明還提供了該晶型的製備方法以及含有治療有效量的該晶型藥物組合物及其在治療各種細菌造成的皮膚感染中的套用。
2018年12月20日,《利奈唑胺晶型B及其製備方法和用途》獲得第二十屆中國專利優秀獎。
(概述圖為《利奈唑胺晶型B及其製備方法和用途》摘要附圖)
基本介紹
- 中文名:利奈唑胺晶型B及其製備方法和用途
- 公告號:CN105503764A
- 授權日:2016年4月20日
- 申請號:2016100178056
- 申請日:2016年1月12日
- 申請人:江蘇豪森藥業集團有限公司
- 地址:江蘇省連雲港市經濟技術開發區
- 發明人:楊勇、盛志輝、周炳城、喬智濤、陳安豐
- Int.Cl.:C07D263/20(2006.01)I; A61K31/5377(2006.01)I; A61P31/04(2006.01)I
- 代理機構:南京眾聯專利代理有限公司
- 代理人:顧進
- 類別:發明專利
專利背景,發明內容,專利目的,技術方案,改善效果,附圖說明,技術領域,權利要求,實施方式,榮譽表彰,
專利背景
利奈唑胺(Linezolid),化學名:(S)-N-[[3-[3-氟-4-(4-嗎啉基)苯基]-2-氧代-5-噁唑烷基]甲基]乙醯胺,是第一個人工合成的用於臨床的新型噁唑烷酮類抗菌藥,用於治療革蘭陽性(G+)球菌引起的感染,包括由MRSA引起的疑似或確診院內獲得性肺炎(HAP)、社區獲得性肺炎(CAP)複雜性皮膚或皮膚軟組織感染(SSTI)以及耐萬古黴素腸球菌(VER)感染,其分子式為C16H20FN3O4,具有下式(I)的結構: 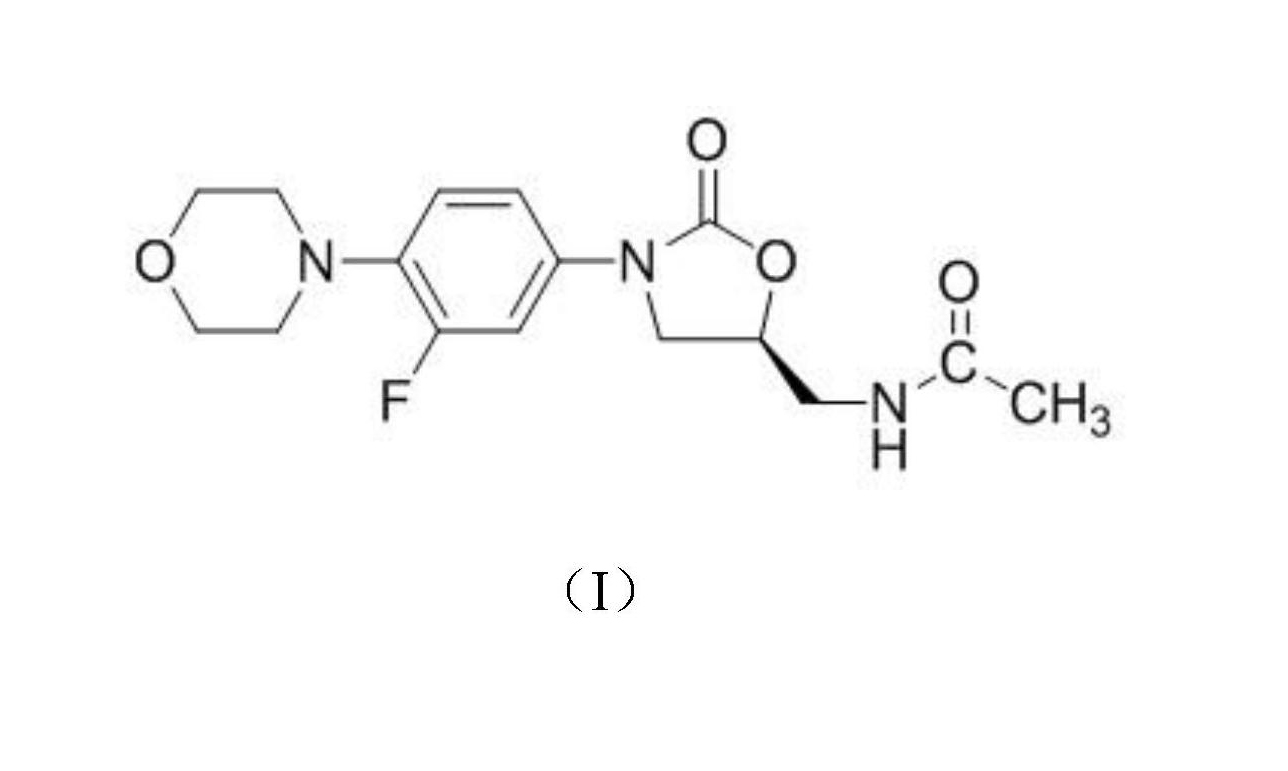

美國專利NO.5688792、歐洲專利NO.717738、以色列專利NO.110802、加拿大專利NO.2168560、國際專利WO95/07171和中國專利CN101128442、CN101220001、CN101774978、文獻J.Med.Chem.39(3)673-679,1996;TetrahedronLett.,40(26)4855,1999;中國醫藥工業雜誌,2010(41)1,6,1-62,公開了利奈唑胺及其製備方法。
利奈唑胺有多種晶型,通常認為有五種晶型。文獻(J.Med.Chem.39(3)673-679,1996)公開了利奈唑胺晶型I,其熔點為181.5-182.5攝氏度,紅外光譜吸收在3284、3092、1753、1728、1649、1565、1519、1447、1435cm-1。其製備過程如下:利奈唑胺粗品用矽膠柱(5.5cm*34cm)純化,然後用3-10%的甲醇-乙酸乙酯溶液洗脫,得到比較純的產品,然後用乙酸乙酯和正己烷重結晶,收率68.8%。
此工藝使用柱層析純化,工藝過程複雜,收率低,溶劑使用量大,混合溶劑不易回收且無法直接重複使用。
專利US6444813和US6559305所描述的是利奈唑胺晶型II,紅外光譜吸收在3364、1748、1675、1537、1517、1445、1410、1401、1358、1329、1287、1274、1253、1237、1221、1145、1130、1123、1116、1078、1066、1049、907、852和758cm-1。粉末X-射線2θ值在7.10,9.54,13.88,14.23,16.18,16.79,17.69,19.41,19.69,19.93,21.61,22.39,22.84,23.52,24.16,25.28,26.66,27.01和27.77處有特徵峰。
此工藝使用大量有機溶劑加熱溶解利奈唑胺粗品,通過敞口蒸發部分溶劑誘導析晶,獲得利奈唑胺晶型II。該工藝操作複雜,對設備要求較高,且在實際生產中,這種敞蒸發溶劑的方法能耗大,危險性高,容易造成環境污染,對人員危害性較大。
WO2005/035530所描述的是利奈唑胺晶型III,粉末X-射線2θ值在7.6,9.6,13.6,14.9,18.2,18.9,21.2,22.3,25.6,26.9,27.9和29.9處有特徵峰。紅外光譜吸收在3338、1741、1662、1544、1517、1471、1452、1425、1400、1381、1334、1273、1255、1228、1213、1197、1176、1116、1082、1051、937、923、904、869、825和756cm-1。
此工藝使用高沸點溶劑高溫溶解利奈唑胺粗品,冷卻析晶獲得利奈唑胺晶型III。該工藝使用了各種高沸點溶劑,容易導致成品殘留溶劑超標,影響藥品使用的安全性。
CN102260222B所描述的是利奈唑胺晶型V,粉末X-射線2θ值在7.36,9.28,13.44,14.62,16.76,17.94,18.43,18.67,19.77,20.68,20.92,22.14,25.40,26.80,27.67,28.34,29.68,33.63和34.10度處有特徵峰。
此工藝使用甲苯/二甲苯高溫溶解利奈唑胺粗品,冷卻析晶獲得利奈唑胺晶型V,因為甲苯/二甲苯沸點較高,無法解決成品中殘留溶劑超標的問題,且甲苯/二甲苯本身毒性較高,容易對環境造成污染。
CN102850289B所描述的是利奈唑胺晶型VI,粉末X-射線2θ值在11.25,16.27,16.70,18.95,19.69,22.73,25.09,25.31,26.22,26.55,27.54和29.60處有特徵峰。
此工藝通過加入鹽酸使利奈唑胺溶清,低溫下加入鹼使利奈唑胺析晶得到晶型VI,該工藝使用了大量鹽酸,容易污染水體,不利於車間操作。
上述文獻報導的利奈唑胺晶型不僅製備工藝複雜、安全性低,而且獲得的晶型粒徑大且分布不均勻。眾所周知,利奈唑胺在水中的溶解度較小,僅為微溶,為了提高利奈唑胺的溶解度,常常需要採用粉碎過篩的方法,以獲得粒徑更小的顆粒,但是在粉碎過程中易產生大量的粉塵,不僅嚴重影響操作人員的人身安全,而且會造成物料的浪費。且在製劑生產過程中,若活性物質的粒徑大且分布不均勻,則容易出現活性物質與輔料難混勻的現象。
因此,開發一種穩定性好且粒徑小、分布均勻、溶出效果好的利奈唑胺晶型是十分必要的。
發明內容
專利目的
《利奈唑胺晶型B及其製備方法和用途》的目的在於解決上述現有技術存在的缺陷,提供一種利奈唑胺的新晶型,將其命名為晶型B,該晶型B具有穩定性好、粒徑小、溶出效果好等優點,可保證藥物生物利用度。
技術方案
《利奈唑胺晶型B及其製備方法和用途》的目的通過以下技術方案得以實現:
利奈唑胺晶型B,使用Cu-Ka輻射,其粉末X-射線衍射光譜的2θ角(±0.2°)在9.43,11.29,13.27,15.55,16.69,19.04,21.92和22.35處有特徵峰。
優選地,所述利奈唑胺晶型B,使用Cu-Ka輻射,其粉末X-射線衍射光譜的2θ角(±0.2°)在9.43,11.29,13.27,14.13,15.55,16.69,17.26,19.04,19.86,20.32,21.92,22.35,23.97和25.16處有特徵峰。
優選地,所述利奈唑胺晶型B,其粉末X-射線衍射光譜圖以2θ角(°)、晶面間距D以及相對強度I(%)的晶型表達,如表1所示: 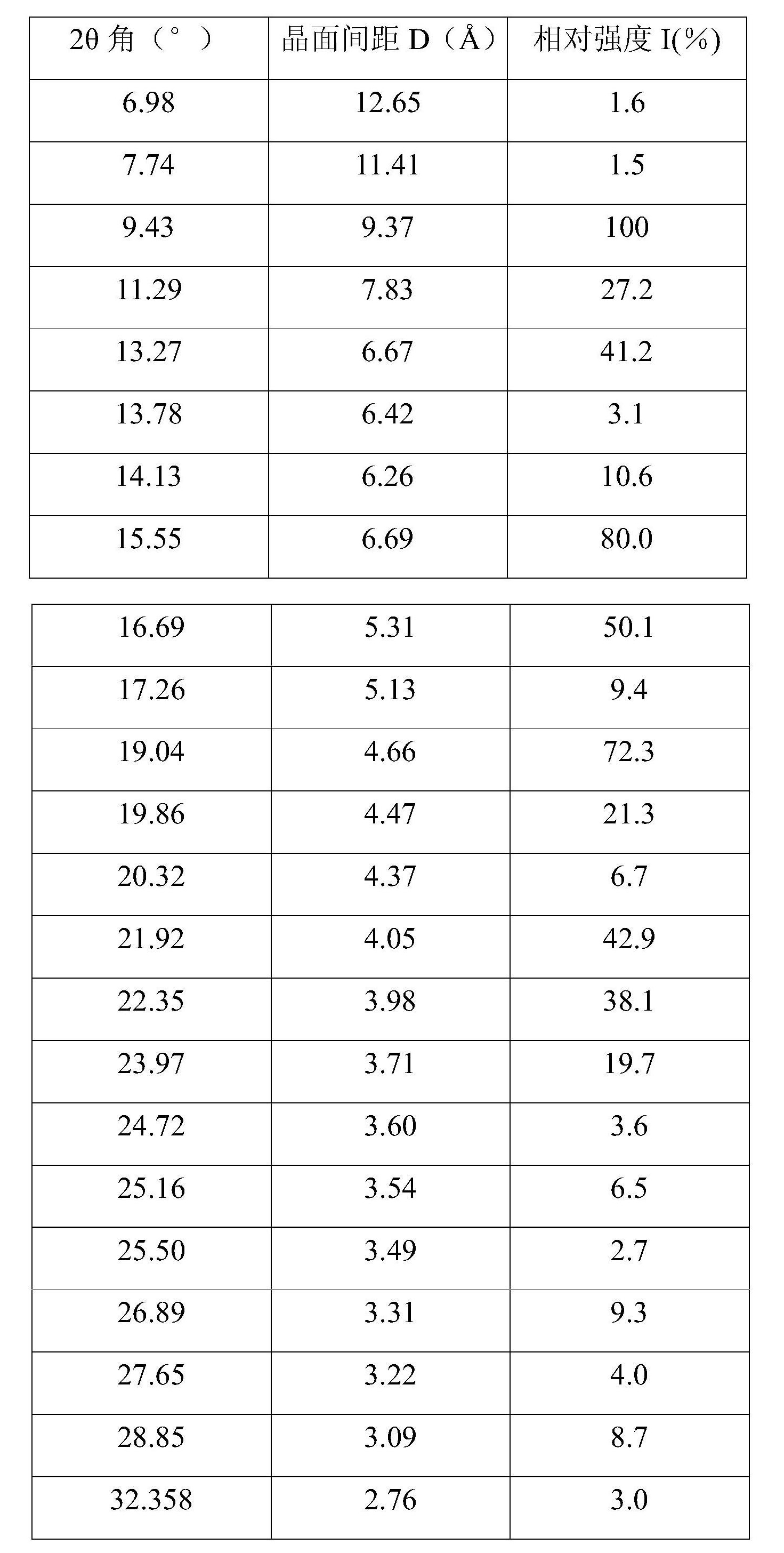

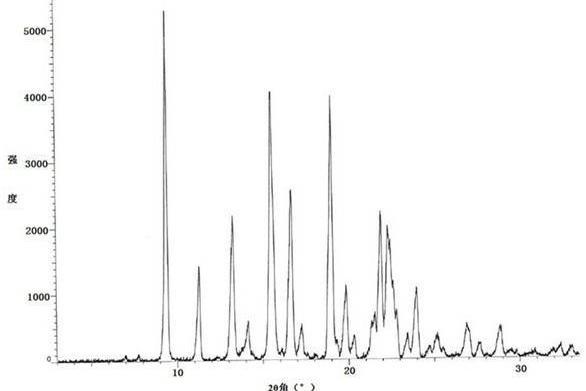
優選地,所述利奈唑胺晶型B,其粉末X-射線衍射光譜圖基本如圖1。
《利奈唑胺晶型B及其製備方法和用途》人驚奇地發現利奈唑胺晶型B,在形態和粒徑上均有很大的改善,不僅顆粒細小且分布均勻,大大提高了藥物溶解度和溶出速率。在片劑開發過程中,《利奈唑胺晶型B及其製備方法和用途》的利奈唑胺晶型B可壓縮性強,幾乎無裂片、碎片等問題,符合藥典要求的片劑。
優選地,所述利奈唑胺晶型B,其粒徑為D(0.9)≤20微米,D(0.5)≤10微米和D(0.1)≤4微米;更優選地,其粒徑為D(0.9)≤16微米,D(0.5)≤5微米和D(0.1)≤2微米。
優選地,所述利奈唑胺晶型B,其比表面積≤3平方米/克,更優選地,比表面積≤2平方米/克。
優選地,所述利奈唑胺晶型B,其比表面積介於0.2平方米/克和2平方米/克之間,介於0.5平方米/克和1.5平方米/克之間,或介於0.5平方米/克和1平方米/克之間。
優選地,所述利奈唑胺晶型B具有良好的藥物溶出度,在0.1摩爾/升鹽酸環境中,5分鐘內,藥物溶出即可達到85%以上;10分鐘內,藥物溶出即可達到95%以上。
優選地,所述利奈唑胺晶型B,在0.1摩爾/升鹽酸環境中,5分鐘內,藥物溶出即可達到88%以上;10分鐘內,藥物溶出即可達到96%以上。
《利奈唑胺晶型B及其製備方法和用途》還提供了上述利奈唑胺晶型B的製備方法,其包括如下步驟:將利奈唑胺鹽酸鹽置於水中,加熱至固體溶解,用鹼調節溶液pH>7,攪拌析晶,過濾得到利奈唑胺晶型B。
優選地,利奈唑胺鹽酸鹽和水的質量體積比(克/毫升)為1:30~70,更優選1:40~60,最優選1:45~50。
優選地,加熱溫度為30攝氏度-70攝氏度,更優選40攝氏度-60攝氏度,最優選40攝氏度-50攝氏度。
優選地,所述鹼選自碳酸鈉、碳酸氫鈉、碳酸鉀、碳酸氫鉀、氫氧化鈉、氫氧化鉀、醋酸鈉、醋酸鉀、磷酸鉀、氨水、三乙胺中的一種或兩種以上以任意比例混合所得的混合物,更優選碳酸鈉、碳酸鉀。
優選地,所述溶液的pH=8~10,更優選pH=9~10。
優選地,析晶結束後,一般還進行自然冷卻過程,更優選自然冷卻至室溫。
優選地,過濾獲得利奈唑胺晶型B後,可按該領域常規方法進行乾燥處理,如真空乾燥,更優選40攝氏度-50攝氏度真空乾燥。
在符合該領域常識的基礎上,上述各優選條件,可任意組合,即得《利奈唑胺晶型B及其製備方法和用途》各較佳實例。
《利奈唑胺晶型B及其製備方法和用途》還提供一種上述利奈唑胺晶型B的藥物組合物,其包含有效治療量的利奈唑胺晶型B和藥學上可接受的載體。一般是將治療有效量的利奈唑胺晶型B與一種或多種藥學上可接受的載體混合或藥物組合物或製劑,該藥物組合物或製劑是以製藥領域中熟知的方式進行製備的。
《利奈唑胺晶型B及其製備方法和用途》的目的還在於提供所述利奈唑胺晶型B及包含該晶型的藥物組合物在製備治療革蘭陽性(G+)球菌引起的感染的藥物中的用途,包括由MRSA引起的疑似或確診院內獲得性肺炎(HAP)、社區獲得性肺炎(CAP)複雜性皮膚或皮膚軟組織感染(SSTI)以及耐萬古黴素腸球菌(VER)感染。
改善效果
《利奈唑胺晶型B及其製備方法和用途》的有益效果包括:《利奈唑胺晶型B及其製備方法和用途》提供的利奈唑胺晶型B穩定性好、粒徑小、可壓縮性和藥物溶出效果好,有利於提高藥物的生物利用度,對於藥物療效及安全性的提高具有重要意義。《利奈唑胺晶型B及其製備方法和用途》提供的利奈唑胺晶型B的製備方法,操作簡單,且不使用有機溶劑,有效解決了成品中殘留溶劑超標的問題,是一種環保、節能的製備方法,且重現性好,適用於工業化大生產。
附圖說明
圖1:利奈唑胺晶型B的XRD圖譜。
圖2:利奈唑胺晶型B的粒度分布圖譜。
技術領域
《利奈唑胺晶型B及其製備方法和用途》屬於醫藥技術領域,具體涉及一種利奈唑胺晶型B及其製備方法,以及含有治療有效量的該晶型藥物組合物及其在治療各種細菌造成的皮膚感染中的套用。
權利要求
1.利奈唑胺晶型B,其特徵在於,其比表面積≤3平方米/克,其粉末X-射線衍射光譜的2θ角(±0.2°)在9.43,11.29,13.27,15.55,16.69,19.04,21.92和22.35處有特徵峰。
2.根據權利要求1所述的利奈唑胺晶型B,其特徵在於,其粉末X-射線衍射圖譜2θ角(±0.2°)在9.43,11.29,13.27,14.13,15.55,16.69,17.26,19.04,19.86,20.32,21.92,22.35,23.97和25.16處具有特徵峰。
3.根據權利要求1所述的利奈唑胺晶型B,其特徵在於,其粒徑為D(0.9)≤20微米,D(0.5)≤10微米和D(0.1)≤4微米。
4.根據權利要求1所述的利奈唑胺晶型B,其特徵在於,其粒徑為D(0.9)≤16微米,D(0.5)≤5微米和D(0.1)≤2微米。
5.權利要求1-4任意一項所述利奈唑胺晶型B的製備方法,其特徵在於,包括如下步驟:將利奈唑胺鹽酸鹽置於水中,加熱至固體溶解,用鹼調節溶液pH>7,攪拌析晶,過濾得到利奈唑胺晶型B,其中利奈唑胺鹽酸鹽和水的質量體積比(克/毫升)為1:45~50,加熱溫度為40攝氏度-60攝氏度。
6.根據權利要求5所述的製備方法,其特徵在於,所述加熱溫度為40攝氏度-50攝氏度。
7.根據權利要求5所述的製備方法,其特徵在於,所述鹼選自碳酸鈉、碳酸氫鈉、碳酸鉀、碳酸氫鉀、氫氧化鈉、氫氧化鉀、醋酸鈉、醋酸鉀、磷酸鉀、氨水、三乙胺中的一種或兩種以上以任意比例混合所得的混合物。
8.根據權利要求5所述的製備方法,其特徵在於,所述鹼選自碳酸鈉或碳酸鉀。
9.根據權利要求5所述的製備方法,其特徵在於,所述溶液的pH=8~10。
10.根據權利要求5所述的製備方法,其特徵在於,所述溶液的pH=9~10。
11.一種藥物組合物,包含有效量的權利要求1-4任意一項所述的利奈唑胺晶型B及藥學上可接受的賦形劑。
12.權利要求1-4任意一項所述的利奈唑胺晶型B及權利要求11所述的藥物組合物在製備治療革蘭陽性(G+)球菌引起的感染藥物中的用途。
實施方式
- 實施例1 利奈唑胺晶型B的製備
取2.5克利奈唑胺鹽酸鹽置於反應瓶中,加入100毫升水,在攪拌的條件下加熱至50攝氏度,固體溶解,滴加10%碳酸鉀溶液,調節反應液pH=9~10。反應液攪拌析晶,自然冷卻至室溫,過濾。所得濾餅在40~50攝氏度,真空乾燥4~6小時得到利奈唑胺晶型B,其XRD圖譜基本如圖1所示。
- 實施例2 利奈唑胺晶型B的製備
取2.2克利奈唑胺鹽酸鹽置於反應瓶中,加入100毫升水,在攪拌的條件下反應液加熱至40攝氏度,固體溶解。滴加10%碳酸鉀溶液,調節反應液pH=8~9。反應液攪拌析晶,自然冷卻至室溫,過濾。所得濾餅在40~50攝氏度,真空乾燥4~6小時得到利奈唑胺晶型B,其XRD圖譜基本如圖1所示。
- 實施例3 晶型穩定性考察
將《利奈唑胺晶型B及其製備方法和用途》的利奈唑胺晶型B樣品置於溫度為25攝氏度,相對濕度為60%的環境中,並定期觀察晶體的外觀變化和檢測利奈唑胺的含量,其實驗結果如表2所示:
表2 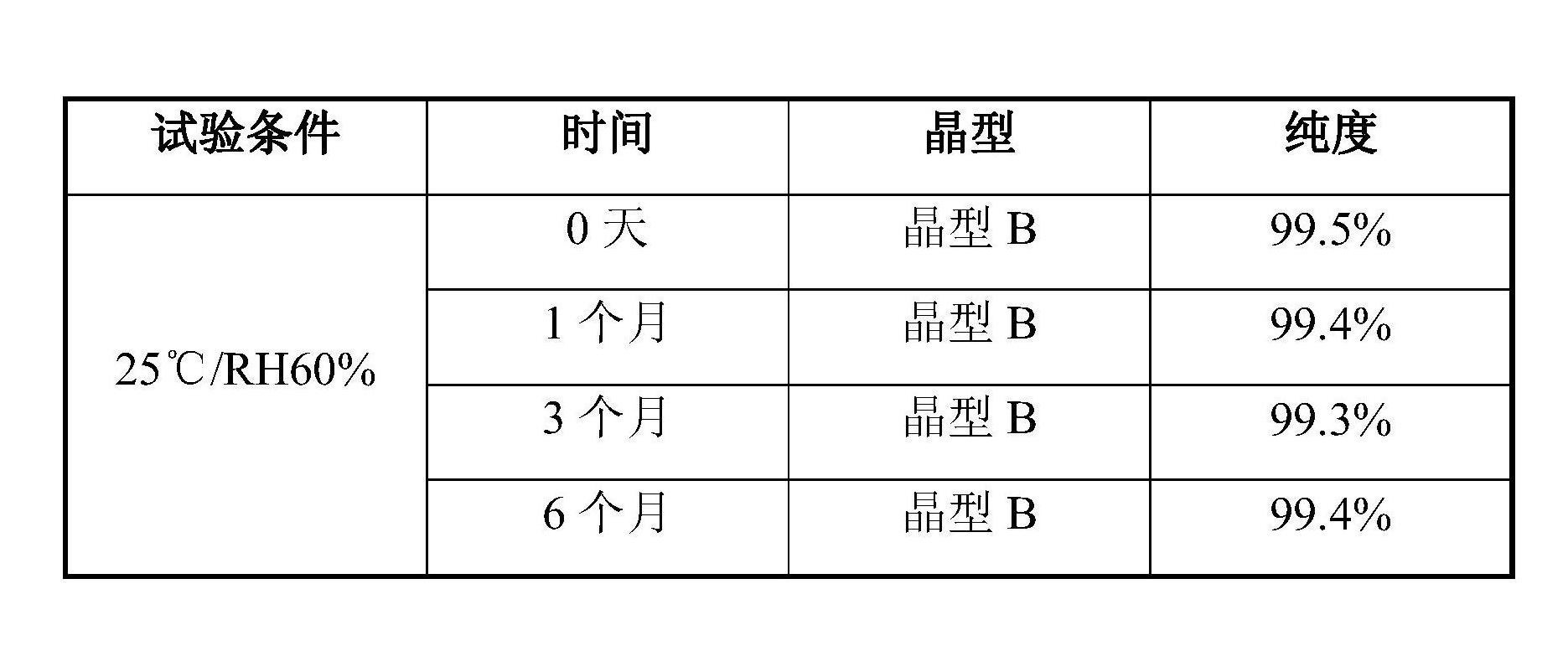

實驗結果表明,《利奈唑胺晶型B及其製備方法和用途》利奈唑胺晶型B穩定可控,方便存儲與運輸,符合藥用要求。
- 實施例4 晶型粒徑考察
將《利奈唑胺晶型B及其製備方法和用途》利奈唑胺晶型B與現有技術中公開的利奈唑胺晶型進行粒徑分布測試,實驗結果如表2和圖2所示。
表2:利奈唑胺晶型B與其他晶型樣品粒徑檢測比較 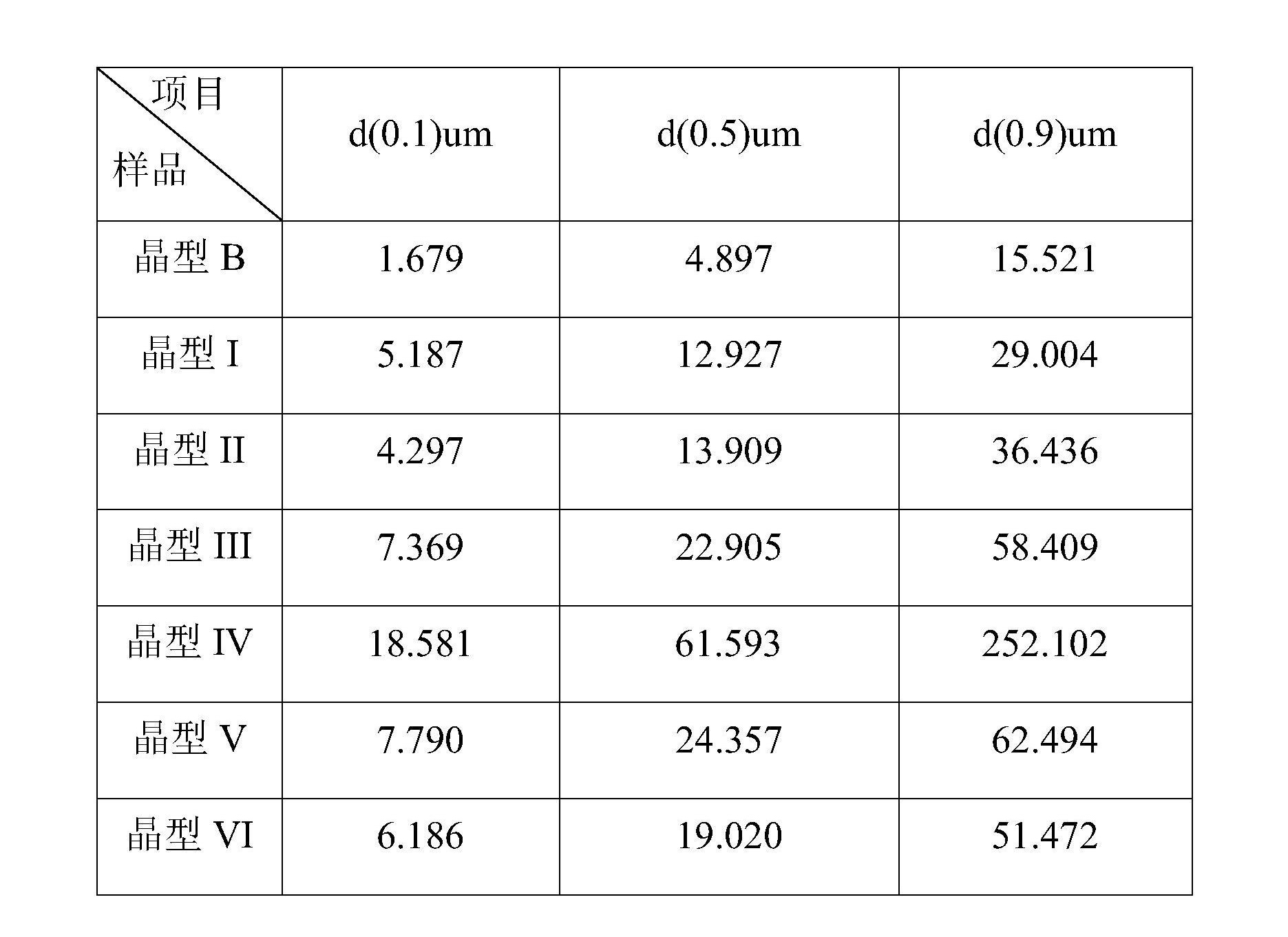

結果顯示,《利奈唑胺晶型B及其製備方法和用途》獲得的利奈唑胺晶型B粒徑小且分布均勻,晶型B樣品中90%的顆粒粒徑≤15.52微米,50%的顆粒粒徑≤4.90微米,10%的顆粒粒徑≤1.68微米。與現有技術公開的晶型相比,粒徑更小,並且具有更窄的粒徑分布。
- 實施例5 溶出度考察
《利奈唑胺晶型B及其製備方法和用途》對利奈唑胺晶型B樣品進行了製劑工藝穩定性和製劑體外溶出度測試。將樣品按照製劑工藝分別製備成6批片劑,製劑處方如表2所示。
表2製劑處方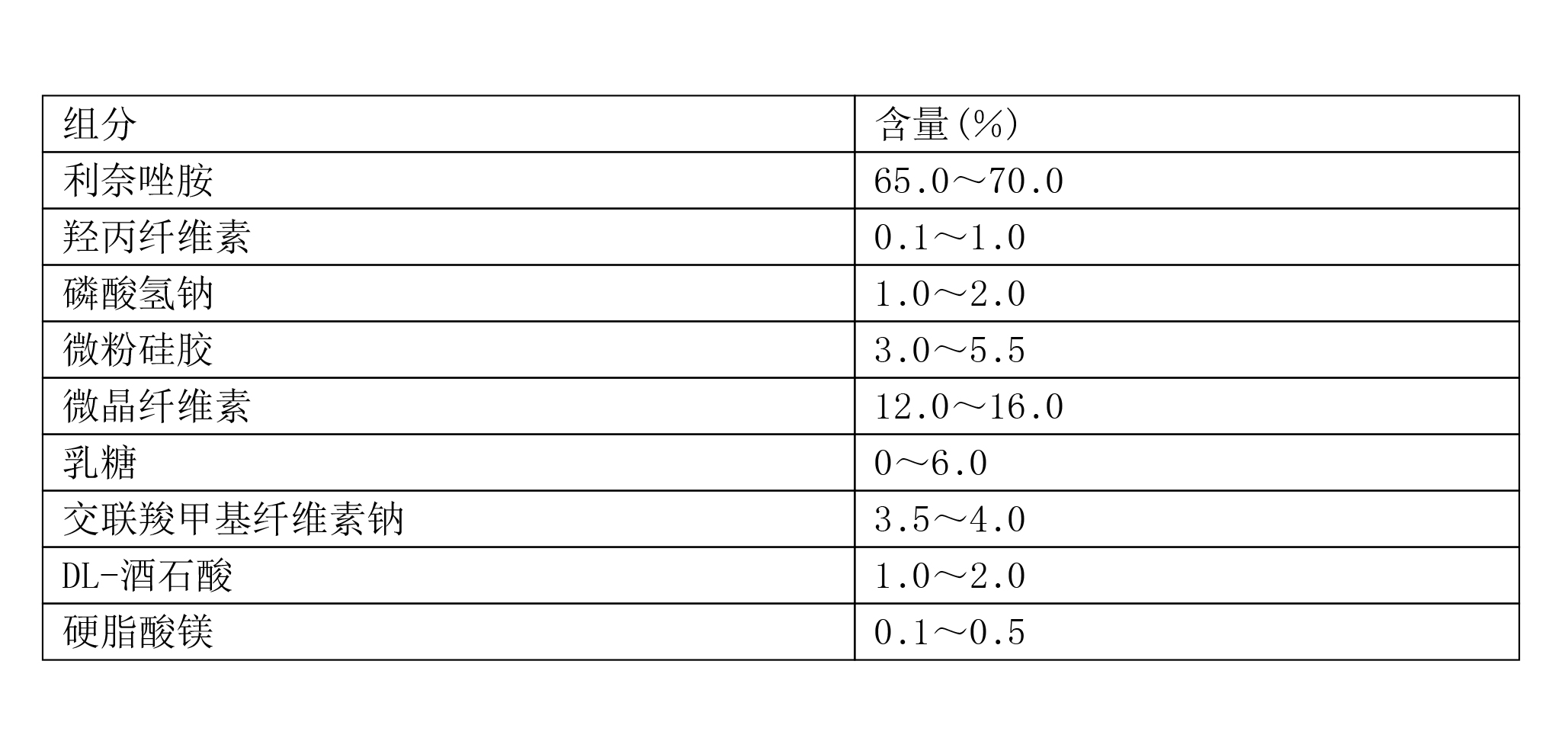

片劑體外溶出度的測試:從每批製劑樣品中隨機抽取6片樣品,在模擬胃液環境中測定45分鐘內利奈唑胺溶出數據,結果如表3。
表3:利奈唑胺晶型B片劑在0.1摩爾/升鹽酸環境中累積溶出度 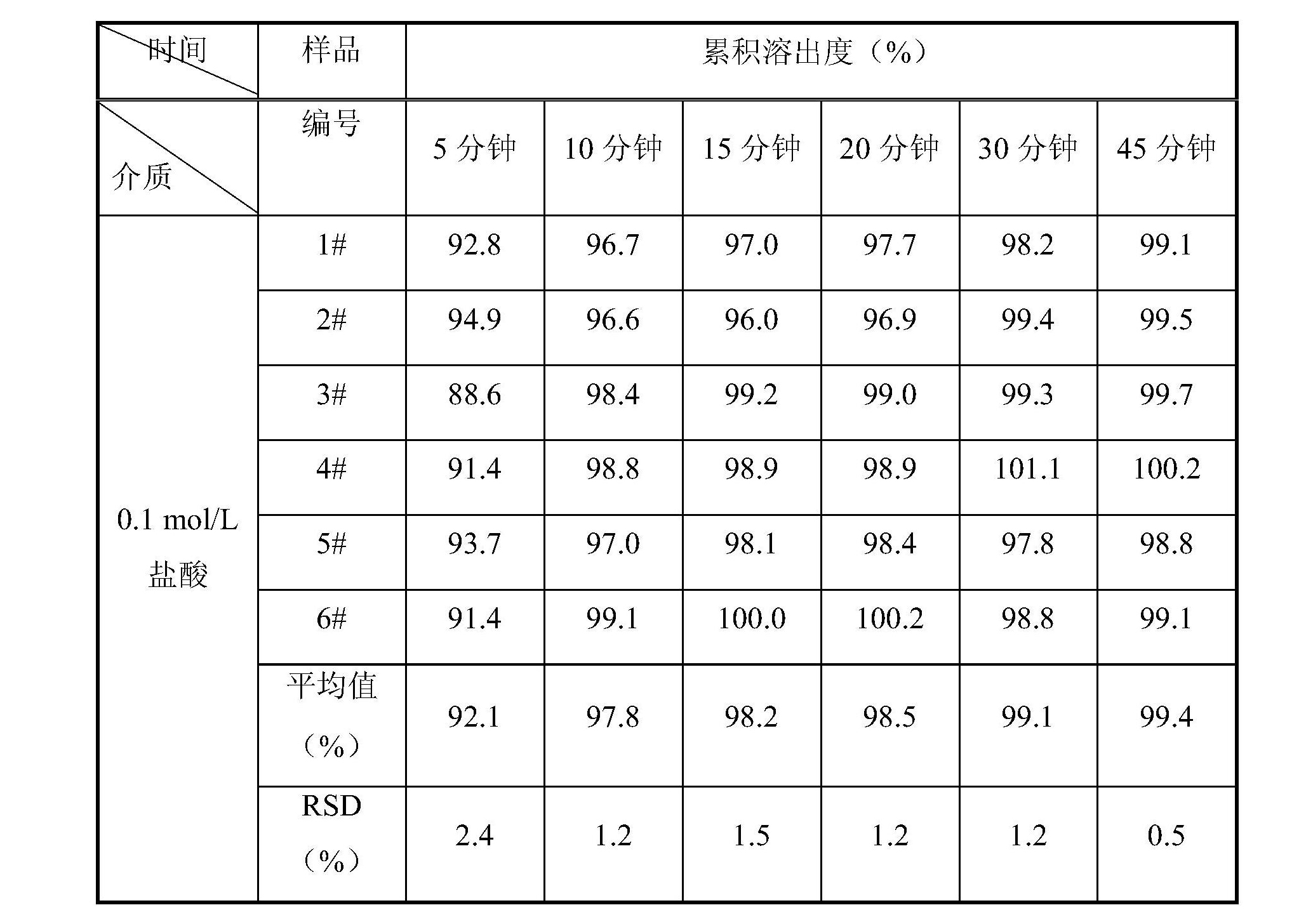

結果表明,利奈唑胺晶型B樣品壓縮性好,所得片劑不易龜裂(完整率達100%),而且製劑溶出數據非常好,達到了藥用的要求,提升了藥物的生物利用度。
榮譽表彰
2018年12月20日,《利奈唑胺晶型B及其製備方法和用途》獲得第二十屆中國專利優秀獎。