倍清星(奧拉西坦注射液),適應症為用於腦損傷及其引起的神經功能缺失、記憶與智慧型障礙的治療。
基本介紹
- 藥品名稱:倍清星
- 藥品類型:處方藥
- 用途分類:主要興奮大腦皮層的藥物
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,批准文號,生產企業,核准日期,修訂日期,
成份
本品主要成份為奧拉西坦,輔料為磷酸二氫鈉和乙二胺四乙酸二鈉鹽。
其藥物成份奧拉西坦的化學名稱: 4-羥基-2-氧代-1-吡咯烷乙醯胺
化學結構式:
分 子 式:C6H10N2O3
分 子 量:158.16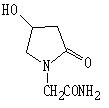
其藥物成份奧拉西坦的化學名稱: 4-羥基-2-氧代-1-吡咯烷乙醯胺
化學結構式:
分 子 式:C6H10N2O3
分 子 量:158.16

性狀
本品為幾乎無色或微黃色澄明液體。
適應症
用於腦損傷及其引起的神經功能缺失、記憶與智慧型障礙的治療。
規格
5ml:1.0g
用法用量
靜脈滴注,每次4.0g,每日一次,可酌情增減用量,用前加入到100~250ml 5%葡萄糖注射液或0.9%氯化鈉注射液中,搖勻。對神經功能缺失的治療通常療程為2周,對記憶與智慧型障礙的治療通常療程為3周。
不良反應
據國外文獻報導,奧拉西坦的不良反應少見,偶見皮膚瘙癢、噁心、精神興奮、頭暈、頭痛、睡眠紊亂,但症狀較輕,停藥後可自行恢復。
禁忌
對本品過敏者、嚴重腎功能損害者禁用。
注意事項
1、 輕、中度腎功能不全者應慎用,必需使用本品時,須減量。
2、 患者出現精神興奮和睡眠紊亂時,應減量。
2、 患者出現精神興奮和睡眠紊亂時,應減量。
孕婦及哺乳期婦女用藥
本品在孕婦及哺乳期婦女使用的安全性尚不明確,因此,不應使用。
兒童用藥
尚不明確。
老年用藥
若出現不良反應時,須減量。
藥物相互作用
尚不明確。
藥物過量
目前尚無本品藥物過量反應的相關報導。
藥理毒理
藥理作用 本品為吡拉西坦的類似物,可改善老年性痴呆和記憶障礙症患者的記憶和學習功能。機理研究結果提示,本品可促進磷醯膽鹼和磷醯乙醇胺合成,提高大腦中ATP/ADP的比值,使大腦中蛋白質和核酸的合成增加。
毒理研究 動物研究提示:本品急性毒性低,小鼠灌胃給藥10g/kg,靜脈給藥2g/kg和大鼠灌胃給藥10g/kg均未見動物死亡;未表現出致突變、致癌作用及生殖毒性。
毒理研究 動物研究提示:本品急性毒性低,小鼠灌胃給藥10g/kg,靜脈給藥2g/kg和大鼠灌胃給藥10g/kg均未見動物死亡;未表現出致突變、致癌作用及生殖毒性。
藥代動力學
奧拉西坦注射液經靜脈給予健康受試者後,在體內的藥代動力學符合二室模型,消除半衰期為3小時左右。奧拉西坦在體內廣泛分布,主要以腎臟、肝臟和肺內濃度最高。小鼠口服奧拉西坦後,腦內於4小時可達藥物的峰濃度。藥物與血漿白蛋白的結合率低,很少透過胎盤屏障,主要以原形從腎臟排出。靜脈給予2g與4g劑量的Cmax分別為110.87±29.22μg/mL和214.60±47.98μg/mL, 統計距參數AUC0-t 200.93±36.63mg· h /L和451.65±106.87mg ·h /L,t1/2β 3.03±0.62h和3.85±0.44h, CL/F 10.24±1.97mL ·kg/h和3.87±1.05mL· kg /h,V/F 59.26±48.77mL/kg和31.64±18.28mL/kg。24h尿藥累積排泄率分別為82.14%±2.57%和82.99%±5.28%。
貯藏
遮光,密封,在陰涼(不超過20℃)處保存。
包裝
(1)安瓿,每盒6支或每盒4支。
(2)安瓿,每盒1支+5ml預灌封注射器、每盒2支+10ml預灌封注射器、每盒4支+20ml預灌封注射器、每盒4支+2支10ml預灌封注射器。
(2)安瓿,每盒1支+5ml預灌封注射器、每盒2支+10ml預灌封注射器、每盒4支+20ml預灌封注射器、每盒4支+2支10ml預灌封注射器。
有效期
暫定18個月。
執行標準
國家食品藥品監督管理局標準(試行)YBH11802005
批准文號
國藥準字H20050860
生產企業
廣東世信藥業有限公司
核准日期
2007年04月18日
修訂日期
2009年06月22日 2010年02月28日
