基本介紹
- 中文名:亨德森-哈塞爾巴爾赫方程
- 外文名:Henderson-Hasselbalch equation
簡介,歷史,推論,參看,
簡介
亨德森-哈塞爾巴爾赫方程(Henderson-Hasselbalch equation)是化學中關於酸鹼平衡的一個方程。該方程使用pKa(即酸解離常數)描述pH值的變化。它可以用來估算緩衝體系的pH。方程的創始人是美國化學家勞倫斯·約瑟夫·亨德森和丹麥科學家卡爾·阿爾伯特·哈塞爾巴爾赫。
若有弱酸HA水解如下:
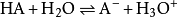


若有鹼水解如下:
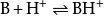
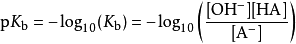

類比可得:

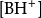
採用攝氏25度下的性質,可以推導出以下表示pH的公式:
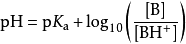
歷史
亨德森方程的形式為:

推論
在H-H方程成立的前提下,可以得出如下推論:
- 體系中,只要弱酸及其共軛鹼的濃度相等,pH即確定為pKa,而與濃度無關。
- 緩衝體系,pH比pKa大1時,鹼濃度是酸濃度的10倍。反之亦然。
