基本介紹
- 中文名:二氧化三碳
- 外文名:Carbon suboxide; 1,2-Propadiene-1,3-dione
- 別名:次氧化碳
- 化學式:C3O2
- 分子量:68.03
- CAS登錄號:504-64-3
- 熔點:-111.3 ℃
- 沸點:6.8 ℃
- 水溶性:與水反應
- 外觀:無色氣體
研究簡史,理化性質,製備方法,計算化學數據,
研究簡史
1873年,Brodie通過對一氧化碳放電,首次製得了二氧化三碳,Marcellin Berthelot創造了低氧化碳(carbon suboxide)這個名稱,而後來Otto Diels表示,更貼近有機化學的名稱,如二羰基甲烷(dicarbonyl methane)與二氧代丙二烯(dioxallene)也是正確的名稱。
理化性質
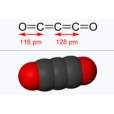
分子形狀為直線形,具有D∞h點群的對稱性,結構式可寫成O=C=C=C=O,C-C鍵長128pm,C-O鍵長116pm。
C3O2是一種非常活潑的化合物,除能跟水發生加成反應外,還能跟NH3、HCl、ROH(R為鏈烴基)等發生加成反應。例如C3O2跟NH3加成:
C3O2 + 2NH3→H2N-CO-CH2-CO-NH2
此外C3O2能與O2反應,生成CO2。C3O2還可以光解:
C3O2 -hv→ C2O + CO
製備方法
二氧化三碳可以通過加熱乾燥的五氧化二磷(分子式為P2O5)和丙二酸或丙二酸酯衍生物的混合物來製備。所以二氧化三碳也可視為丙二酸的酸酐,即丙二酸酐,也就是丙二酸脫水兩次的產物。此外,丙二酸分子間脫一分子水生成的酸酐也是存在的。
以丙二酸為原料製取二氧化三碳的裝置如圖所示: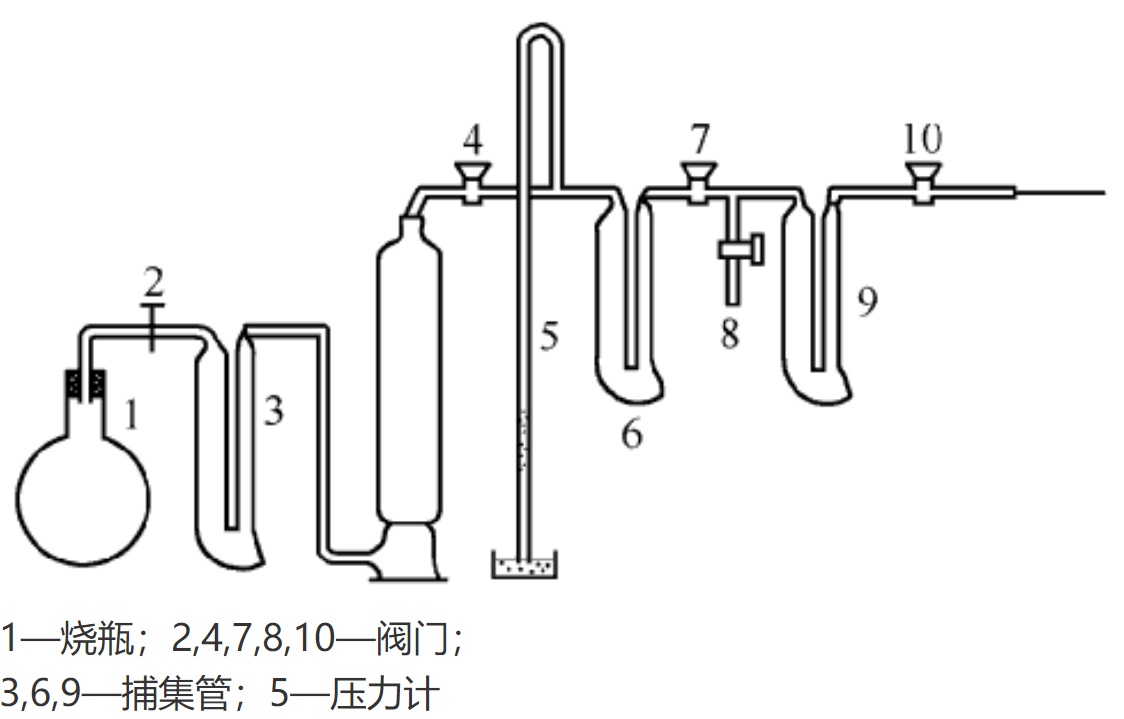

製備反應裝置
稱取20g丙二酸、40g乾燥的砂子和200g新鮮的五氧化二磷,將三者充分混勻後裝入燒瓶1中,然後對整個系統抽真空,當抽至13.3322Pa壓力時,關閉旋塞10,放置使原料乾燥。過幾個小時後,打開旋塞10,再抽真空,用液氮冷卻捕集管3。用油浴加熱燒瓶1,至140℃後保溫1h進行反應。此時,捕集管3中的C3O2粗品被冷凝。然後,撤去油浴,將系統關閉,停泵,由導管8導入乾燥空氣,關閉旋塞2,再抽真空,管3中的粗產物被抽入管6中,關閉系統旋塞10,粗品在管6中得到緩慢蒸餾。一定時間後,將管6置於乙醇浴(-115℃到-110℃),產品則可轉移到液氮冷卻的管9中。
注意管6中的產物不可太滿。捕集管6中經緩慢蒸餾的產物,在高真空下分餾,可得純淨的二氧化三碳。
計算化學數據
1、疏水參數計算參考值(XlogP):0.1
2、氫鍵供體數量:0
3、氫鍵受體數量:2
4、可旋轉化學鍵數量:0
5、互變異構體數量:無
6、拓撲分子極性表面積:34.1
7、重原子數量:5
8、表面電荷:0
9、複雜度:91.3
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量:1