專利背景
鋰是國民經濟和人民生活息息相關的重要稀有金屬之一,在
玻璃陶瓷、石油化工、冶金、
紡織、合成橡膠、潤滑材料、醫療等傳統領域得到了廣泛套用。而
碳酸鋰是鋰化學工業的基礎性化合物,有多種用途,可廣泛用於醫藥、電池等領域。
世界上鋰資源比較豐富,主要分布在南、北美洲、亞洲、澳洲和非洲。現今世界上開採套用最多的鋰礦物是鋰輝石、透鋰長石、鋰雲母和鋰磷鋁石等鹽湖、含鋰滷水和井水也是重要的鋰資源,西方國家利用鹽滷水生產鋰化合物(如碳酸鋰)已占鋰產品生產能力的30%左右。我國是鋰資源大國,已探明的鋰資源儲量居世界第二位,其中滷水鋰含量占總儲量的79%,主要分布於西藏、青海兩地的鹽湖中。青海
柴達木盆地亞輝滷水中鋰的儲量占到了全國總量的58%左右。
滷水提鋰的主要方法有沉澱法、溶劑萃取法、離子交換吸附法以及煅燒浸取法等。2014年10月前已有技術中,專利CN102432044A採用了吸附法對滷水中的氯化鋰進行濃縮,之後採用沉澱法來製得碳酸鋰產品。專利CN102275956A採用萃取和反萃取來得到NaCl和LiCl反萃取液以及NH
4Cl和LiCl反萃取液,之後採用沉澱法來製得納米級和微米級的碳酸鋰產品。專利CN102963914A採用蒸發濃縮、加鹼沉澱雜質離子、過濾以及加沉澱劑製得碳酸鋰,並經洗滌和灼燒之後得到高純碳酸鋰。這些方法存在滷水中氯化鋰濃縮倍數不高、沉澱反應耗時長以及碳酸鋰中雜質含量較高等問題。
發明內容
專利目的
《一種由滷水提取電池級鋰的工藝及裝置》所要解決的技術問題是:提高從滷水中提取鋰的工藝中耗時長、氯化鋰濃縮倍數不高、收率低、試劑使用量大、碳酸鋰產品中雜質含量高的問題,提出了一種由滷水提取電池級鋰的工藝及裝置。
技術方案
根據《一種由滷水提取電池級鋰的工藝及裝置》的一個方面:一種由滷水提取電池級鋰的工藝,包括如下步驟:
第1步、用鋰吸附劑對滷水進行吸附,再對鋰吸附劑進行解吸,得到解吸液;
第2步、將解吸液除鎂,得到除鎂的解吸液;
第3步,對除鎂的解吸液進行濃縮,得到含鋰濃縮滷水。
根據該發明的一個實施方式:所述的滷水中Mg和Li的重量比優選為1:1~400:1,更優選為2:1~200:1,最優選為2:1~150:1。Li的質量百分比濃度優選為0.1~15.0克/升,更優選為0.3~10.0克/升,最優選為0.5~8.0克/升。
根據該發明的一個實施方式:鋰吸附劑是指鋁鹽鋰吸附劑、氫氧化物吸附劑、銻酸型吸附劑、離子篩型吸附劑中的一種或幾種的混合物。
根據該發明的一個實施方式:第1步中,是將鋰吸附劑分散在滷水中,得到混合液,再對混合液進行固液分離,對分離後的鋰吸附劑進行解吸。鋰吸附劑的在滷水中的加入量優選0.05~5克/升,更優0.2克/升。鋰吸附劑加入滷水後,攪拌30~60分鐘,滷水溫度為30~60℃。固液分離的步驟中包括使用分離膜進行濃縮的步驟;所述的分離膜的材質優選採用陶瓷膜;所述的分離膜優選採用微濾膜。固液分離的步驟優選是採用分離膜進行濃縮,得到吸附劑濃縮液,再用板框過濾器對吸附劑濃縮液進行脫水。分離膜的平均孔徑範圍是50~200納米;過濾溫度為30~80℃,操作壓力0.2~0.5兆帕,膜面流速1~4米/秒。分離膜進行濃縮過程中需要進行定期反衝洗,反衝間隔30~60分鐘,反衝時間為10~30秒。
根據該發明的一個實施方式:第1步中是將鋰吸附劑裝入吸附柱體(也稱填料柱體)中,注入滷水進行吸附,再注入洗脫液進行解吸,得到解吸液。
第1步中得到解吸液之後,通過過濾器進行過濾之後,再將透過液送入第2步中的除鎂步驟。洗脫劑是水或者磷酸溶液,磷酸溶液的pH為1~2,解吸溫度50~100℃。
根據該發明的一個實施方式:第2步中除鎂的操作步驟是採用納濾膜過濾或者離子交換樹脂吸附的方式去除鎂離子。納濾膜截留分子量為100~300,納濾操作壓力為1.0~3.0兆帕,操作溫度為20~45℃。採用納濾膜進行除鎂時,是通過至少兩級納濾膜進行過濾。一級納濾的濃縮倍數優選是3~6倍,二級納濾的濃縮倍數優選是8~12倍。
根據該發明的一個實施方式:採用納濾膜過濾去除鎂離子之後,再用陽離子交換樹脂進行除鎂。
根據該發明的一個實施方式:第3步中的濃縮步驟採用反滲透膜濃縮、DTRO膜濃縮、電滲析膜濃縮、蒸發濃縮中的至少一種,得到含鋰濃縮滷水。更優選的,濃縮步驟是先用反滲透膜濃縮,再對反滲透膜濃縮液採用DTRO膜濃縮或者蒸發濃縮中的至少一種再進行濃縮,得到含鋰濃縮滷水。反滲透濃縮過程的運行壓力為3.0~4.0兆帕,溫度為30~40℃。
根據該發明的一個實施方式:第3步中得到含鋰濃縮滷水後,向其中加入BaCl2、Na2CO3以及NaOH溶液使使得滷水中的SO4、Ca以及Mg形成沉澱,並去除沉澱。加入順序是依次加入BaCl2、Na2CO3以及NaOH溶液。加入的BaCl2的摩爾濃度比含鋰濃縮滷水中的SO4摩爾濃度大1%~5%,加入的Na2CO3的摩爾濃度比含鋰濃縮滷水中的Ca的摩爾濃度大1~10%,加入的NaOH的摩爾濃度比含鋰濃縮滷水中的Mg的摩爾濃度的2倍再大1~5%。
根據該發明的一個實施方式:向去除了沉澱的含鋰濃縮滷水中,加入Na2CO3溶液使Li2CO3沉澱,將沉澱分離、烘乾後,得到碳酸鋰。
根據該發明的一個實施方式:分離沉澱的步驟是採用陶瓷膜分離,陶瓷膜孔徑範圍是為20~200納米,優選膜孔徑為50納米,運行過程中壓力為0.1~0.5兆帕,溫度為10~50℃。
根據該發明的另一個方面:一種由滷水提取電池級鋰的裝置,包括有吸附解吸裝置、除鎂裝置、濃縮裝置,吸附解吸裝置的解吸液出口與除鎂裝置的入口連線,除鎂裝置的出口與濃縮裝置的入口連線,濃縮裝置的濃縮液出口與第一沉澱槽連線,在第一沉澱槽上還設定有第一碳酸鈉罐,第一沉澱槽的出口還連線於第二固液分離器。
所述的吸附解吸裝置是吸附劑填充柱。在吸附劑填充柱的出口上還連線有過濾器,過濾器的出口與除鎂裝置連線。所述的吸附解吸裝置包括有依次連線的吸附槽、第一固液分離器、解吸槽,解吸槽的出口與除鎂裝置連線。所述的第一固液分離器包括有陶瓷膜裝置和板框過濾器,陶瓷膜裝置的截留側的出口與板框過濾器的入口連線,陶瓷膜裝置的入口連線在吸附槽,板框過濾器的截留側與解吸槽連線。所述的除鎂裝置是指納濾膜裝置或者離子交換樹脂裝置。所述的除鎂裝置是指依次連線的納濾膜和離子交換樹脂柱,納濾膜的入口連線於吸附解吸裝置,納濾膜的滲透側連線於離子交換樹脂柱,離子交換樹脂柱的出口連線於濃縮裝置。所述的濃縮裝置選自反滲透膜裝置、DTRO膜裝置、電滲析膜裝置、蒸發濃縮裝置中的至少一種。所述的濃縮裝置是指依次連線的反滲透膜和DTRO膜,反滲透膜的入口連線於除鎂裝置,反滲透膜的截留側連線於DTRO膜的入口,DTRO膜的出口連線於第一沉澱槽。所述的濃縮裝置的出口依次通過第二沉澱槽和第三固液分離器再連線於第一沉澱槽;濃縮裝置的出口連線於第二沉澱槽的入口,第二沉澱槽的出口連線於第三固液分離器的入口,第三固液分離器的截留側的出口連線於第一沉澱槽;在第二沉澱槽上分別設定有氯化鋇罐、第二碳酸鈉罐、氫氧化鈉罐。所述的第二固液分離器是陶瓷膜過濾裝置。所述的第三固液分離器是陶瓷膜過濾裝置。所述的陶瓷膜過濾裝置中,陶瓷膜孔徑範圍是為20~200納米,優選膜孔徑為50納米。所述的陶瓷膜裝置中,陶瓷膜孔徑範圍是為20~200納米。
有益效果
《一種由滷水提取電池級鋰的工藝及裝置》採用吸附劑對滷水中的鋰離子進行吸附和解吸,並採用陶瓷膜過濾器對吸附劑進行截留,採用反滲透膜和DTRO膜對滷水進行深度濃縮,可以有效地提高LiCl的濃縮倍數,不受天氣和曬鹽場地的限制,顯著提高碳酸鋰沉澱法獲得的產品得率和產品質量。
附圖說明
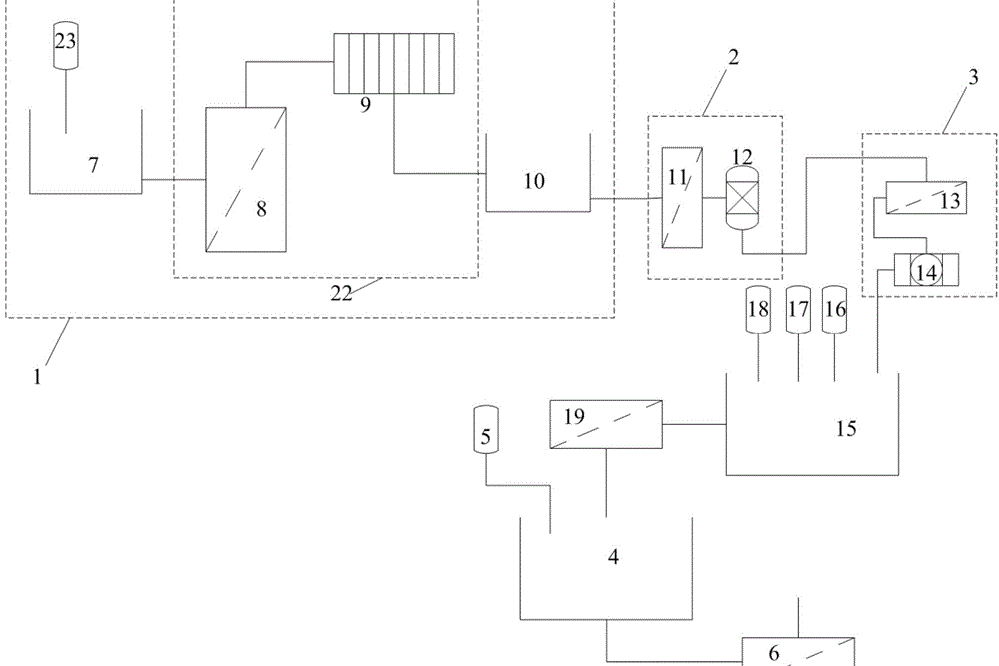
圖1是《一種由滷水提取電池級鋰的工藝及裝置》提供的一種由滷水提取電池級鋰的裝置的結構示意圖。
圖2是該發明提供的另一種由滷水提取電池級鋰的裝置的結構示意圖。
其中,1、吸附解吸裝置;2、除鎂裝置;3、濃縮裝置;4、第一沉澱槽;5、第一碳酸鈉罐;6、第二固液分離器;7、吸附槽;8、陶瓷膜裝置;9、板框過濾器;10、解吸槽;11、納濾膜;12、離子交換樹脂柱;13、反滲透膜;14、DTRO膜;15、第二沉澱槽;16、氯化鋇罐;17、第二碳酸鈉罐;18、氫氧化鈉罐;19、第三固液分離器;20、吸附劑填充柱;21、過濾器;22、第一固液分離器;23、吸附劑罐。
權利要求
1.一種由滷水提取電池級鋰的工藝,其特徵在於,包括如下步驟:第1步、用鋰吸附劑對滷水進行吸附,再用洗脫劑對鋰吸附劑進行解吸,得到解吸液;第2步、將解吸液除鎂,得到除鎂的解吸液;第3步,對除鎂的解吸液進行濃縮,得到含鋰濃縮滷水;第1步中,是將鋰吸附劑分散在滷水中,得到混合液,再對混合液進行固液分離,對分離後的鋰吸附劑進行解吸。
2.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:所述的滷水中Mg和Li的重量比為1:1~400:1。
3.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:所述的滷水中Mg和Li的重量比為2:1~200:1。
4.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:所述的滷水中Mg和Li的重量比為2:1~150:1。
5.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:所述的滷水中Li的質量百分比濃度為0.1~15.0克/升。
6.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:所述的滷水中Li的質量百分比濃度為0.3~10.0克/升。
7.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:所述的滷水中Li的質量百分比濃度為0.5~8.0克/升。
8.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:鋰吸附劑是指鋁鹽鋰吸附劑、氫氧化物吸附劑、銻酸型吸附劑、離子篩型吸附劑中的一種或幾種的混合物。
9.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:鋰吸附劑的在滷水中的加入量0.05~5克/升。
10.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:鋰吸附劑的在滷水中的加入量0.2克/升。
11.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:鋰吸附劑加入滷水後,攪拌30~60分鐘,滷水溫度為30~60℃。
12.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:所述的固液分離的步驟中包括使用分離膜進行濃縮的步驟。
13.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:固液分離的步驟是採用分離膜進行濃縮,得到吸附劑濃縮液,再用板框過濾器對吸附劑濃縮液進行脫水。
14.根據權利要求12或13所述的由滷水提取電池級鋰的工藝,其特徵在於:所述的分離膜的材質採用陶瓷膜。
15.根據權利要求12或13所述的由滷水提取電池級鋰的工藝,其特徵在於:所述的分離膜採用微濾膜;分離膜的平均孔徑範圍是50~200納米;過濾溫度為30~80℃,操作壓力0.2~0.5兆帕,膜面流速1~4米/秒。
16.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:第1步中的洗脫劑是水或者磷酸溶液,磷酸溶液的pH為1~2,解吸溫度50~100℃。
17.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:第2步中除鎂的操作步驟是採用納濾膜過濾或者離子交換樹脂吸附的方式去除鎂離子。
18.根據權利要求17所述的由滷水提取電池級鋰的工藝,其特徵在於:納濾膜截留分子量為100~300,納濾操作壓力為1.0~3.0兆帕,操作溫度為20~45℃。
19.根據權利要求17所述的由滷水提取電池級鋰的工藝,其特徵在於:採用納濾膜進行除鎂時,是通過至少兩級納濾膜進行過濾,一級納濾的濃縮倍數是3~6倍,二級納濾的濃縮倍數是8~12倍。
20.根據權利要求19所述的由滷水提取電池級鋰的工藝,其特徵在於:採用納濾膜過濾去除鎂離子之後,再用陽離子交換樹脂進行除鎂。
21.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:第3步中的濃縮步驟採用反滲透膜濃縮、DTRO膜濃縮、電滲析膜濃縮、蒸發濃縮中的至少一種,得到含鋰濃縮滷水。
22.根據權利要求21所述的由滷水提取電池級鋰的工藝,其特徵在於:濃縮步驟是先用反滲透膜濃縮,再對反滲透膜濃縮液採用DTRO膜濃縮或者蒸發濃縮中的至少一種再進行濃縮,得到含鋰濃縮滷水。
23.根據權利要求21所述的由滷水提取電池級鋰的工藝,其特徵在於:反滲透濃縮過程的運行壓力為3.0~4.0兆帕,溫度為30~40℃。
24.根據權利要求1所述的由滷水提取電池級鋰的工藝,其特徵在於:第3步中得到含鋰濃縮滷水後,向其中加入BaCl2、Na2CO3以及NaOH溶液使使得滷水中的SO4、Ca以及Mg形成沉澱,並去除沉澱。
25.根據權利要求24所述的由滷水提取電池級鋰的工藝,其特徵在於:加入順序是依次加入BaCl2、Na2CO3以及NaOH溶液。
26.根據權利要求24所述的由滷水提取電池級鋰的工藝,其特徵在於:加入的BaCl2的摩爾濃度比含鋰濃縮滷水中的SO4摩爾濃度大1%~5%,加入的Na2CO3的摩爾濃度比含鋰濃縮滷水中的Ca的摩爾濃度大1~10%,加入的NaOH的摩爾濃度比含鋰濃縮滷水中的Mg的摩爾濃度的2倍再大1~5%。
27.根據權利要求24所述的由滷水提取電池級鋰的工藝,其特徵在於:向去除了沉澱的含鋰濃縮滷水中,加入Na2CO3溶液使Li2CO3沉澱,將沉澱分離、烘乾後,得到碳酸鋰。
28.根據權利要求24或27所述的由滷水提取電池級鋰的工藝,其特徵在於:分離沉澱的步驟是採用陶瓷膜分離,陶瓷膜孔徑範圍是為20~200納米,膜孔徑為50納米,運行過程中壓力為0.1~0.5兆帕,溫度為10~50℃。
29.一種由滷水提取電池級鋰的裝置,包括有吸附解吸裝置(1)、除鎂裝置(2)、濃縮裝置(3),其特徵在於:吸附解吸裝置(1)的解吸液出口與除鎂裝置(2)的入口連線,除鎂裝置(2)的出口與濃縮裝置(3)的入口連線,濃縮裝置(3)的濃縮液出口與第一沉澱槽(4)連線,在第一沉澱槽(4)上還設定有第一碳酸鈉罐(5),第一沉澱槽(4)的出口還連線於第二固液分離器(6);所述的吸附解吸裝置(1)包括有依次連線的吸附槽(7)、第一固液分離器(22)、解吸槽(10),解吸槽(10)的出口與除鎂裝置(2)連線。
30.根據權利要求29所述的由滷水提取電池級鋰的裝置,其特徵在於:所述的第一固液分離器(22)包括有陶瓷膜裝置(8)和板框過濾器(9),陶瓷膜裝置(8)的截留側的出口與板框過濾器(9)的入口連線,陶瓷膜裝置(8)的入口連線在吸附槽(7),板框過濾器(9)的截留側與解吸槽(10)連線。
31.根據權利要求29所述的由滷水提取電池級鋰的裝置,其特徵在於:所述的除鎂裝置(2)是指納濾膜裝置或者離子交換樹脂裝置。
32.根據權利要求29所述的由滷水提取電池級鋰的裝置,其特徵在於:所述的除鎂裝置(2)是指依次連線的納濾膜(11)和離子交換樹脂柱(12),納濾膜(11)的入口連線於吸附解吸裝置(1),納濾膜(11)的滲透側連線於離子交換樹脂柱(12),離子交換樹脂柱(12)的出口連線於濃縮裝置(3)。
33.根據權利要求29所述的由滷水提取電池級鋰的裝置,其特徵在於:所述的濃縮裝置(3)選自反滲透膜裝置、DTRO膜裝置、電滲析膜裝置、蒸發濃縮裝置中的至少一種。
34.根據權利要求33所述的由滷水提取電池級鋰的裝置,其特徵在於:所述的濃縮裝置(3)是指依次連線的反滲透膜(13)和DTRO膜(14),反滲透膜(13)的入口連線於除鎂裝置(2),反滲透膜(13)的截留側連線於DTRO膜(14)的入口,DTRO膜(14)的出口連線於第一沉澱槽(4)。
35.根據權利要求29所述的由滷水提取電池級鋰的裝置,其特徵在於:所述的濃縮裝置(3)的出口依次通過第二沉澱槽(15)和第三固液分離器(19)再連線於第一沉澱槽(4);濃縮裝置(3)的出口連線於第二沉澱槽(15)的入口,第二沉澱槽(15)的出口連線於第三固液分離器(19)的入口,第三固液分離器(19)的截留側的出口連線於第一沉澱槽(4)。
36.根據權利要求35所述的由滷水提取電池級鋰的裝置,其特徵在於:在第二沉澱槽(15)上分別設定有氯化鋇罐(16)、第二碳酸鈉罐(17)、氫氧化鈉罐(18)。
37.根據權利要求35所述的由滷水提取電池級鋰的裝置,其特徵在於:所述的第二固液分離器(6)是陶瓷膜過濾裝置。
38.根據權利要求35所述的由滷水提取電池級鋰的裝置,其特徵在於:所述的第三固液分離器(19)是陶瓷膜過濾裝置。
實施方式
操作內容
鋰的主要資源包括鋰礦石和含鋰滷水。《一種由滷水提取電池級鋰的工藝及裝置》中,術語“滷水”可以是指天然滷水(如:鹽湖滷水、地下滷水、地熱滷水或者製鹽滷水)或者人工配置的滷水。尤其是,在許多情況下,與其它類型的滷水相比,鹽湖滷水具有高的鋰濃度,適合用作該發明中的原料。在該發明中,可以從含有高濃度的鎂和硫酸(它們為由普通方法製備碳酸鋰時的干擾成分)有效地製備碳酸鋰,並且M克/升i比值和SO4/Li比值超過10的、難以從其中回收鋰的含鋰滷水可以用作該發明中的原料。對於滷水型資源,鹽湖滷水是最重要的來源。在造山帶(例如安第斯山脈)中,包含氯化鈉在內的水溶性成分(它們從周圍的海成岩石溶出)隨流水流入通過快速隆起而形成的山頂湖中,並且經過長期濃縮,從而析出鹽並且堆積形成鹽湖。在飽和滷水內部鹽湖堆積,該飽和滷水被稱為鹽湖滷水。鹽湖滷水包含源自海水的氯化鈉作為主要成分,並且還包含陽離子成分(例如,鉀、鋰、鎂和鈣)和陰離子成分(例如氯、溴、硫酸和硼酸)。除了海水成分的影響之外,其組成根據鹽湖周圍的礦物種類和火山活動而變化。在鹽湖滷水中,鋰濃度高的鹽湖滷水成為鋰資源的開發目標。滷水中回收鋰的方法主要包括通過日曬蒸發的濃縮步驟、通過添加化學品的雜質去除步驟、以及通過添加碳酸鈉的碳酸化步驟。主要包含氯化物的滷水對於氯化鋰具有高溶解度,並且鋰濃度可以增加到約60克/升的高濃度。然而,在滷水包含大量硫酸根離子的情況下,在蒸發濃縮的過程中會析出硫酸鋰(Li2SO4·H2O)。因此,鋰濃度僅能增加到約6克/升,並且鋰以硫酸鋰的形式被損失掉。另外,當鹽湖滷水包含上述各種離子成分時,鎂通過碳酸化步驟而以碳酸鎂的形式析出,並且可能混合在作為最終產品的碳酸鋰中,從而使最終產品的純度降低,因此需要在碳酸化步驟之前去除鎂。具體而言,烏尤尼鹽湖(玻利維亞)、青海鹽湖(中國)等中的滷水的鎂含量高,並且M克/升i的濃度比為19至62。因此,不僅需要大量化學品(如氫氧化鈣和碳酸鈉)以去除鎂,而且還會形成大量的氫氧化鎂和碳酸鎂泥漿,並且濃縮的滷水被包裹在泥漿中,這將妨礙含有鋰的濃縮滷水的回收。另外,鹽湖滷水的硫酸根離子濃度經常較高,例如,在烏尤尼鹽湖(玻利維亞)中,SO4/Li的濃度比為24,在青海鹽湖(中國)中,SO4/Li的濃度比為138(在阿塔卡馬鹽湖(智利)中,SO4/Li的濃度比為11),在這些鹽湖中,2014年10月前的情況是,在蒸發濃縮步驟中鋰濃度僅能升高到6克/升,因此,不能獲得適合於碳酸化步驟的濃縮滷水,其中所述碳酸化步驟通常套用於濃度為約60克/升以上的高濃度區域。一旦例如鎂離子、硫酸根離子、鋇離子等雜質離子的水平被儘可能地降低,例如降低至ppm級,如低於20ppm,優選低於0.0005wt%,或更低如0.00001wt%,含鋰滷水即可適於進行回收工藝以回收非常純的鋰鹽,如氯化鋰和/或碳酸鋰,或者鋰金屬。
《一種由滷水提取電池級鋰的工藝及裝置》中可以處理的滷水中,Mg和Li的重量比優選為1:1~400:1,更優選為2:1~200:1,最優選為2:1~150:1。Li的質量百分比濃度優選為0.1~15.0克/升,更優選為0.3~10.0克/升,最優選為0.5~8.0克/升。
《一種由滷水提取電池級鋰的工藝及裝置》中首先採用鋰吸附劑對滷水中的鋰進行吸附,然後再通過解吸的方式將鋰洗脫而得到解吸液。該發明中所述的鋰吸附劑可以採用公知的對鋰離子具有選擇性吸附的固體吸附劑,通常這類的吸附劑都呈顆粒狀、具有較大的比表面積,其材質一般包括有有機吸附劑和無機吸附劑。對於有機系的吸附劑,一般是指高分子離子交換樹脂,基本上是強酸性吸附樹脂,例如IR-120B型陽離子交換樹脂。對於無機吸附劑,可以採用2014年10月前已有的鋁鹽吸附劑(如通式為LiX·2Al(OH)3·nH2O,其中X代表陰離子,通常是Cl,n代表結晶水的個數)、無定型氫氧化物吸附劑(主要是鋁氧化物吸附劑)、層狀吸附劑(一般為砷酸鹽或者磷酸鹽類鋰吸附劑,也可以是鈦酸鹽類鋰吸附劑)、複合銻酸型吸附劑和離子篩型吸附劑等。對於離子篩型氧化物吸附劑,可以例舉的,包括有單斜晶銻酸鹽系(如Li1-xHxSbO3,0<x<1)、鈦酸鹽系(如Li2TiO3)、錳氧化物系等(如尖晶石型錳氧化物,它是由諸如MnO2、MnCO3或MnOOH等錳化合物和諸如LiOH、Li2CO3的鋰化合物或鎂化合物Mg(OH)2反應生成前驅體後,再經酸洗而製得),也可以是摻雜有其它金屬元素,尤其是過渡金屬元素製備摻雜型錳氧化物鋰離子篩,例如LiMg0.5Mn1.5O4、LiZn0.5Mn1.5O4、LiTi0.5Mn1.5O4、LiFe0.5Mn1.5O4、Li1.33-x/3CoxMn1.67-2x/3O4、LiFeMnO4、LiAlMnO4、LiCu0.5Mn1.5O4等。也可以是複合型吸附劑,例如在弱鹼性陰離子交換樹脂的空隙中附著有大量的LiX·2Al(OH)3·nH2O的複合型吸附劑,其中X為鹵素。在該發明的一些實施例中採用了含鋁鹽型吸附劑,在另外一些實施例中採用的是磷酸鐵離子篩,它為FeSO4、MexFeyPO4中的一種或幾種的混合物。Me為Mg、Al、Ti、Ni、Co、Mn、Mo、Nb中的一種或幾種的混合。0<x<1,0<y<1。其製備方法可以參閱專利文獻CN102049237。
對於上述的吸附操作,可以採用的是將吸附劑裝填於吸附柱中,使滷水流過吸附柱中的吸附劑床層,從而完成鋰離子在吸附劑上的吸附,然後再通過加入洗脫液從而使鋰離子被洗脫,在得到解吸液之後,再優選通過過濾器進行過濾之後,再將透過液送入到後續的除鎂處理步驟中,過濾器可以採用粗過濾器,作用是去除其中的吸附劑顆粒及泥沙,例如採用常規的砂濾、濾布等過濾部件。
由於在進行吸附、解吸操作時,仍然會有一些鎂離子和其它的二價鹼金屬離子存在於解吸液中,對洗脫得到的解吸液進行除鎂離子時,可以降低解吸液中的鎂/鋰比,這裡的去除鎂離子的操作可以採用沉澱法、納濾或者離子交換樹脂除鎂等方法,但是在該發明的一個優選實施方式中,採用納濾或者離子交換樹脂除鎂的方法。
當採用向裝填有吸附劑的吸附柱中供入洗脫液對鋰吸附劑進行洗脫的過程中,隨著洗脫過程的進行,解吸液中的Mg含量會發生下降,經過試驗發現,降低解吸液中的Mg含量,有利於降低納濾的工藝負荷、提高納濾濃縮倍數、降低納濾透過液的Mg含量,但是從另一方面來說,發現Mg離子存在時,納濾膜對鋰離子具有負截留效應,即納濾透過液中Li濃度增大的現象,因此Mg的含量不能過低,否則在納濾過程中,在納濾的過程中鋰離子的負截留現象減弱,會出現一部分鋰離子被截留的情況發生,影響到產品收率。當解吸液中Mg含量為2~3克/升時停止解吸。在該優選條件下,納濾膜透過液中Li濃度相比原料液能夠提高10~20%。但是,這種操作方式仍然存在有操作時間長、效率低的問題。
對於鋰吸附劑進行吸附操作的過程,在該發明的一個改進實施方式中,是通過將鋰吸附劑混合於滷水中,攪拌後使其分散於滷水中,這種操作方式可以有較高的工作效率,達到吸附飽和的時間短於採用吸附劑填充的方式。將吸附劑混合於滷水中的操作,可以採用將其置於攪拌槽,再在攪拌槽中加入吸附劑並連續攪拌,鋰離子吸附到吸附劑上,得到吸附劑和滷水混合液;攪拌30~60分鐘,滷水溫度為30~60℃。鋰吸附劑的在滷水中的加入量優選0.05~5克/升,更優0.2克/升。
當上述的吸附過程完成後,再將鋰吸附劑和滷水的混合液進行固液分離處理,以使吸附劑被分離開,這樣可以更好地對其進行解吸操作,這裡所述的固液分離,沒有特別限定。作為具體的固液分離處理的方法,可舉出離心分離方式、壓榨分離方式、過濾方式、上浮分離方式、沉降分離方式。在其中一種優選實施方式中,是需要將混合液送入分離膜中進行濃縮,鹽湖中的其他離子例如Mg、Ca等作為透過液排出。這裡所述的分離膜優選採用微濾膜,在得到濃縮液之後,再通過常規的脫水的方法使濃縮液進一步地脫水,例如:蒸發、離心等,較優是採用板框過濾的方式進行脫水,得到吸附劑濾餅。用於該步驟的微濾膜為平均孔徑是0.01微米~5毫米的膜。作為這些微濾膜的材質,只要能夠實現將吸附劑濃縮這樣的該發明目的即可,沒有特別限定,可以舉出:纖維素、纖維素酯、聚碸、聚醚碸、聚氯乙烯、氯丙烯、聚烯烴、
聚乙烯醇、
聚甲基丙烯酸甲酯、
聚偏二氟乙烯、聚四氟乙烯等有機材料,或者不鏽鋼等金屬、或者陶瓷等無機材料。微濾膜的材質可以考慮混合液的性狀或者運行成本來適當選擇,從操作容易性考慮,優選陶瓷等無機材料。陶瓷膜過濾溫度為30~80℃,操作壓力0.2~0.5兆帕,膜面流速1~4米/秒。在另一個實施方式中,通過將微濾膜的平均孔徑控制在50~200納米之間時,可以進一步地提高最終得到的鋰的收率。
在一個改進實施方式中,最好是要對陶瓷膜過濾進行反衝處理,反衝裝置自動採用陶瓷膜滲透清液對陶瓷膜過濾設備進行反衝,將附著在膜通道表面的吸附劑濾餅反衝脫落,有效減輕膜污染,提高膜通量,有助於系統長期穩定運行。反衝間隔過短,延長了過濾的時間,增加了成本;反衝間隔過長,膜表面的濾餅過厚,陶瓷膜會在較長時間內在低通量下運行,也延長了過濾時間。反衝時間過短,不能將膜表面的吸附劑完全反衝脫落,過濾通量不能有效恢復;反衝時間過長,反衝需要更多的滲透水量,還需繼續陶瓷膜處理,增加過濾負額,所以選擇反衝間隔30~60分鐘,反衝時間為10~30秒。
在對分離膜濃縮液進行進一步地脫水而得到吸附劑濾餅之後,為了進一步地提高產品純度,還最好對其進行洗滌,用以去除濾餅中夾帶的雜質離子,然後再用解吸液進行解吸操作。洗滌劑優選水或LiCl的水溶液,其中水的電導率優選為2~10微秒/厘米,LiCl的水溶液的LiCl的濃度優選為0.02~5克/升;鋰離子解吸液為水(優選去離子水)或者磷酸溶液,磷酸溶液的pH優選控制在1~2,解吸溫度優選50~100℃。
在得到解吸液之後,其中存在有Li離子,也會帶有一定量的諸如Mg、Ca等雜質離子,接下來,需要進一步地去除Mg、Ca等雜質離子。正如上述所述,可以採用納濾或者離子交換樹脂的方法進行去除雜質離子,上一步中的鋰吸附劑起到初步脫鎂的作用,該步驟可以降低鎂鋰比,更重要的是給後續納濾分離減輕負荷,使納濾工藝中的鎂的透過率也減小,更重要地是這一步可以降低過濾體系中的鎂離子的強度,使納濾工藝中的濃縮倍數提高,使得納濾過程中濃縮倍數提高,提高鋰的提取收率,設備自動化容易實現。
該文中納濾膜是定義為“阻止小於2納米的粒子和溶解的大分子的壓力驅動膜”的膜。適用於《一種由滷水提取電池級鋰的工藝及裝置》的有效納濾膜優選是這樣的膜:在該膜表面上有電荷,因而通過細孔分離(粒度分離)和得益於該膜表面上的電荷的靜電分離的結合而表現出提高的分離效率。因此,必需採用這樣的納濾膜,該納濾膜能夠在將作為回收目標的鹼金屬離子與具有不同電荷特性的其他離子藉助電荷進行分離的同時、通過粒度分離來去除高分子類物質。作為該發明中使用的納濾膜的材料,可以使用乙酸纖維素系聚合物、聚醯胺、磺化聚碸、聚丙烯腈、聚酯、聚醯亞胺和乙烯基聚合物等高分子材料。所述不限於僅由一種材料構成的膜,可以是包含多種所述材料的膜。關於膜結構,所述膜可以是非對稱膜,其在膜的至少一面上具有緻密層,並且具有從緻密層向膜內部或者另一面孔徑逐漸變大的微孔;或者是複合膜,其在非對稱膜的緻密層上具有由其它材料所形成的非常薄的功能層。
有利地,所述的納濾膜可以為一級納濾或者兩級納濾,優選兩級納濾,採用兩級納濾除鎂可以進一步地提高鎂的去除率,同時也可以進一步地去除其它的二價離子,使產品的純度更高。這主要是由於多級納濾可以提高二價鹽的截留率,但是納濾的過濾級數也不能過多,否則會導致在經過多級過濾後,體系中有一部分鋰離子也被截留,影響到收率。納濾膜截留分子量為100~300,納濾操作壓力為1.0~3.0兆帕,優選地,納濾操作壓力可以為2.5兆帕,操作溫度為20~45℃,進一步地,操作溫度可以為25~40℃。溫度過低,會導致納濾膜的通量低,直接影響整個工藝的處理量以及處理效率,溫度過高,對有機納濾膜元件會造成一定的負擔,長時間的高溫運行,會導致納濾膜壽命減短,最終不可再生。壓力過低,同樣會導致納濾膜的通量低,再者還會導致納濾膜元件對Mg的截留率降低,壓力過高,會直接導致運行能耗增加,經濟成本加大,其次還會導致運行過程中體系溫度升高過快,影響膜元件的壽命。一級納濾的濃縮倍數優選是3~6倍,如果濃縮倍數過高,會導致通量較小,系統能耗過大,如果濃縮倍數小時,則不能將滲透液提濃,使後續工藝負擔較高,二級納濾的濃縮倍數優選是8~12倍。在一個優選的實施例中,採用了兩級納濾,一級納濾的操作溫度30℃、壓力3.0兆帕,二級納濾的操作溫度為40℃,壓力為3.0兆帕;反滲透運行壓力3.5兆帕,溫度是35℃。在一個優選的實施例中,納濾膜對於硫酸鎂的截留率≥98%。
離子交換樹脂透過液或者納濾膜透過液即可以通過碳酸鹽沉澱法對其中的鋰進行沉澱提純,但是最好是要對其進行濃縮處理,將鋰離子的濃度進一步的提高之後,可以提高其收率、減小藥劑的消耗。根據《一種由滷水提取電池級鋰的工藝及裝置》的一個實施方式,在得到離子交換樹脂透過液之後,需要將透過液進行濃縮,以提高其濃度。濃縮的方式可以採用反滲透膜濃縮、蒸發濃縮等。較優採用的是先採用反滲透膜對離子交換樹脂透過液進行濃縮,最好再通過DTRO膜(碟管式反滲透膜)或者是電滲析膜進行濃度濃縮,使LiCl的濃度可以提升20~30倍,再將濃縮液用蒸發的方式進一步地濃縮。蒸發器可以為多效蒸發器。
作為反滲透膜的材料,一般使用醋酸纖維素類聚合物、聚醯胺、聚酯、聚醯亞胺、乙烯基聚合物等高分子材料。另外,作為其構造,有在膜的至少一側具有緻密層,從該緻密層向膜內部或者另一側的表面具有緩緩變大的孔徑的微細孔的非對稱膜以及在該非對稱膜的緻密層上具有由其他材料形成的非常薄的活性層的複合膜等。其中,作為反滲透膜的形式,有中空絲、平膜等.通常,優選中空絲和平膜的膜厚為10微米~1毫米,中空絲的外徑為50微米~4毫米。另外,作為平膜,優選非對稱膜,作為複合膜優選被織物、編織物、無紡布等基材支撐的膜.但是,《一種由滷水提取電池級鋰的工藝及裝置》的方法可以不依賴於反滲透膜的材料、膜構造或形式地加以利用,對於任意一種情況都有效。反滲透膜裝置的濃縮液一般具有壓力能量,為了降低運轉成本,優選回收該能量。作為回收能量的方法,可以用安裝到任意部分的高壓泵上的能量回收裝置回收,優選用安裝在高壓泵的前後或組件之間的專用渦輪型能量回收泵回收。
反滲透濃縮過程的運行壓力為3.0~4.0兆帕,溫度為30~40℃。溫度過低,會導致反滲透膜的通量低,直接影響整個工藝的處理量以及處理效率,溫度過高,對有機納濾膜元件會造成一定的負擔,長時間的高溫運行,會導致納濾膜壽命減短,最終不可再生。壓力過低,同樣會導致納濾膜的通量低,再者還會導致納濾膜元件對Mg的截留率降低,壓力過高,會直接導致運行能耗增加,經濟成本加大,相比於傳統的鎂離子交換樹脂除鎂,再用反滲透進行濃縮的工藝,《一種由滷水提取電池級鋰的工藝及裝置》的方法中,可以將反滲透的濃縮倍數提高至5~8倍,而傳統方法的反滲透的濃縮倍數只有2~3倍,甚至更低。
在《一種由滷水提取電池級鋰的工藝及裝置》的一個實施方式中,當上述的濃縮的方式可以採用反滲透膜濃縮時,除鎂步驟的操作是採用納濾膜進行濃縮,這是因為如果採用離子交換樹脂進行除鎂操作時,在體系中引入了鈉離子,這使得體系中的鈉離子的含量大幅提高,導致了反滲透過程的過程中濃縮倍數不高,表現在反滲透運行時的通量過低,無法達到工程所需,而且也會導致對反滲透的濃縮液進一步濃縮時耗時、能耗大的問題。而當採用了吸附和納濾分離工藝時,就高效地脫除鎂離子,不引入鈉離子,可以使反滲透過程保持較高的濃縮倍數,這就對後續的曬鹽、濃縮或者蒸發更為有利,當需要對鋰離子進行沉澱提取時,所耗費的藥劑也很少。通常情況下,當採用納濾去除鎂離子時,可以相對於採用採用離子交換樹脂除鎂來說,使反滲透膜的濃縮倍數由3倍提高至6倍以上。
術語“濃縮倍數”在該發明中是指待過濾的料液的體積與濃縮過濾結束之後的濃縮液的體系的比值。
《一種由滷水提取電池級鋰的工藝及裝置》的一個改進的實施方式中,還可以對除鎂過程中的納濾膜透過液送入離子交換樹脂吸附塔進行深度除鈣鎂離子,優選採用弱酸型陽離子交換樹脂,陽離子交換樹脂為本領域技術人員所知曉的對鹼土金屬陽離子具有選擇性的陽離子交換樹脂都可以用於該發明。可以例舉地,如:德國LanxessEuropeGmbH的市售商品Lewatit MonoPlus TP208等。解吸液的流動速度優選是3~10BV/小時。深度除鎂鈣後的滷水再送入後續的濃縮步驟中。
根據該發明的一個實施方式,濃縮後的滷水則進入蒸發器進行蒸發後,向其中加入BaCl2、Na2CO3以及NaOH溶液,使得滷水中的SO4、Ca以及Mg等形成沉澱,生成的BaSO4、CaCO3、Mg(OH)2,並通過陶瓷膜過濾器進行固液分離,去除其中的雜質離子。作為改進,加入的BaCl2的摩爾濃度比含鋰濃縮滷水中的SO4摩爾濃度大1%~5%,加入的Na2CO3的摩爾濃度比含鋰濃縮滷水中的Ca的摩爾濃度大1~10%,加入的NaOH的摩爾濃度比含鋰濃縮滷水中的Mg的摩爾濃度的2倍再大1~5%。作為上述方法的改進,加入BaCl2、Na2CO3以及NaOH沉澱劑的過程中均需攪拌,攪拌時間為20~40分鐘,攪拌時間優選30分鐘。
在去除了沉澱的濃縮液中再加入Na2CO3溶液進行沉澱反應,可以形成Li2CO3沉澱,沉澱採用陶瓷膜過濾器進行粉體洗滌,去除其中的離子,再經離心和烘乾後得到Li2CO3成品。Na2CO3溶液是經膜過濾器、精密過濾器等處理之後的,Na2CO3的純度大於99.5%。Li2CO3洗滌採用“少量、多次”洗滌方式,濃縮倍數為5~8倍,加水量為濃縮液體積的3~5倍,至陶瓷膜滲透液電導率小於100微秒/厘米。
通過陶瓷膜對沉澱(如上述的BaSO4、CaCO3、Mg(OH)2、Li2CO3)進行過濾去除中,孔徑範圍如果過小,則會導致過濾通量低,無法滿足工程所需,如果孔徑過大,則會導致一部分沉澱無法得到截留,而進入至滲透側,影響到產品的品質。壓力過小,會導致過濾通量小,壓力過大,會導致一些較小的顆粒粒子被壓過膜層,進入至滲透側。溫度過低,會導致過濾通量低,而溫度過高時,會影響到顆粒的溶解度,使一部分沉澱顆粒重新溶解,進入至滲透側。更優選的,陶瓷膜孔徑範圍是為20~200納米,優選膜孔徑為50納米,運行過程中壓力為0.1~0.5兆帕,溫度為10~50℃。
在以下實施例中採用的鹽湖滷水的離子濃度如表1所示:
基於上述的方法,可以採用的提取分離裝置如圖1和圖2所示,在圖1中,該裝置主要是由吸附解吸裝置1、除鎂裝置2、濃縮裝置3、第一沉澱槽4、第二固液分離器6依次連線而構成。吸附解吸裝置1的作用是對滷水中的鋰進行吸附和解吸,得到解吸液。
吸附解吸裝置1可以是單獨只採用如圖2中所示的結構,就是通過吸附劑填充柱20對滷水進行吸附解吸,吸附劑填充柱20中裝填的是鋰吸附劑,首先將滷水供入吸附劑填充柱20中,進行吸附的操作,排出滷水,然後再供入解吸液,將解吸液供入除鎂裝置2中,在一個實施方式中,可能在吸附劑填充柱20的出口處再連線一個過濾器21,其作用是用於去除掉解吸液中的一些固體雜質。
在另外的一個實施方式中,吸附解吸裝置1如圖1中所示,它包括有一個吸附槽7,吸附槽7的作用是存放滷水,再在其中加入鋰吸附劑,因此,在吸附槽7的上方還連線有一個吸附劑罐23,用於向吸附槽7中加入鋰吸附劑。吸附槽7的出口連線在第一固液分離器22,由於吸附槽7中主要是滷水與鋰吸附劑的混合液,將它送入第一固液分離器22中後,可以將已經吸附飽和的鋰吸附劑分離出,第一固液分離器22可以採用常規的固液分離裝置,在一個實施方式中,最好是採用陶瓷膜裝置8和板框過濾器9,如圖1中所示的這樣,陶瓷膜裝置8的入口連線於吸附槽7的出口,陶瓷膜裝置8的濃縮側與板框過濾器9的入口連線,對鋰吸附劑和滷水的混合液進行濃縮操作之後,再將濃縮液送入至板框過濾器9進行壓濾,可以得到鋰吸附劑濾餅,然後板框過濾器9的截留側的出口再連線在解吸槽10中,可以將濾餅排出,然後再在解吸槽10中加入解吸液,可以對鋰吸附劑進行解吸操作,得到了解吸液之後,再通過解吸槽10上的解吸液出口連線於除鎂裝置2的入口上。
除鎂裝置2可以採用離子交換裝置或者是納濾裝置,在一個實施方式中,除鎂裝置2包括依次連線的納濾膜11和離子交換樹脂柱12,納濾膜11的滲透側連線於離子交換樹脂柱12的入口,離子交換樹脂柱12的出口再連線於濃縮裝置3。
濃縮裝置3可以採用反滲透膜裝置、DTRO膜裝置、電滲析膜裝置、蒸發濃縮裝置中的任意一種。在一個實施方式中,可以採用如圖1中所示的依次連線的反滲透膜13和DTRO膜14,反滲透膜13的截留側的出口連線於DTRO膜14,反滲透膜13對除鎂後的滷水進行濃縮之後,由DTRO膜14對其進一步地濃縮。
DTRO膜14的出口可以直接連線於第一沉澱槽4,第一沉澱槽4是用於對濃縮液中的鋰離子進行沉澱,獲得碳酸鋰,第一沉澱槽4上連線有第一碳酸鈉罐5,其作用是向沉澱槽中加入碳酸鈉。第一沉澱槽4的出口連線在第二固液分離器6的入口,用於將獲得的碳酸鋰沉澱進行分離,第二固液分離器6可以採用陶瓷膜。
在另外的一個實施方式中,DTRO膜14的出口也可以是先連線於第二沉澱槽15上,第二沉澱槽15的出口再連線於第三固液分離器19,第二沉澱槽15上設定有氯化鋇罐16、第二碳酸鈉罐17、氫氧化鈉罐18,分別是用於向第二沉澱槽15中加入沉澱劑。第三固液分離器19可以採用陶瓷膜。
實施例1
將100克FeSO4離子篩鋰吸附劑裝入填充柱,將鹽湖滷水以3BV/小時的速度送入吸附劑床層中,2小時後達到吸附飽和,Li的濃度不再降低;用磷酸溶液進行解吸,磷酸溶液的pH控制在約為1,解吸劑的流速為2BV/小時,大約3小時後完成解吸,鋰解吸溶液再經過弱酸型陽離子交換樹脂D113去除解吸液中的少量鎂,解吸液的流量控制在5BV/小時,再用反滲透膜將處理後的解吸液中的鋰離子濃度濃縮至20克/升左右,反滲透濃縮溫度控制在30℃,操作壓力0.15兆帕,即可以通過加入碳酸鈉的方式使鋰離子轉變為碳酸鋰沉澱,共獲得碳酸鋰8.56克,純度約93%。
實施案例
實施例2
與實施例1的區別在於:吸附、解吸的過程採用的是將吸附劑混合於滷水中,再通過陶瓷膜過濾、板框過濾的方式將吸附劑脫水後再進行解吸。
具體的步驟是:將100克FeSO4離子篩吸附劑加入50升的鹽湖滷水中加熱攪拌,控制溶液溫度為40℃,攪拌60分鐘,滷水中的Li進入吸附劑中,此時溶液中Li的濃度降低至1.07克/升,FeSO4離子篩吸附劑對Li的吸附量約為40毫克/克,再用陶瓷膜對混合料液進行濃縮過濾,陶瓷膜的平均孔徑分別採用5、20、50、200、500納米,過濾壓力0.2兆帕,膜面流速3米/秒,過濾溫度50℃,反衝間隔40分鐘,反衝時間為10秒;陶瓷膜過濾濃縮液經過板框壓濾,去除濃縮液中的大部分雜質和水,得到已吸附鋰的吸附劑濾餅,將壓濾所得的吸附劑濾餅先用電導率6秒/厘米的水對吸附劑濾餅進行洗滌,去除濾餅中夾帶的鎂、鈉、鈣等雜質離子,再置於1升磷酸溶液中進行攪拌,磷酸溶液的pH控制在約為1,攪拌時間為60分鐘,控制溶液溫度為50℃,Li進入磷酸溶液中,得到鋰解吸溶液,鋰解吸溶液再經過弱酸型陽離子交換樹脂D113去除解吸液中的少量鎂,解吸液的流量控制在5BV/小時,最後使用反滲透膜進行濃縮,反滲透濃縮溫度控制在30℃,操作壓力0.15兆帕,將鋰解吸液中的鋰離子濃度濃縮至約20克/升左右時即可以通過加入碳酸鈉的方式使鋰離子轉變為碳酸鋰沉澱,沉澱經過固液分離、洗滌之後,得到碳酸鋰。試驗結果如表2。
採用將吸附劑懸浮於滷水進行吸附,再用陶瓷膜進行過濾濃縮吸附劑的方式,可以有效地提高工序效率,能夠節約樹脂的吸附時間;另外,從表中可以看出,由於在微濾的過程中,吸附劑處於微濾的錯流、分離的雙重作用效果中,滷水中的膠體、大分子雜質不易在吸附劑的表面包覆、沉積,可以防止吸附劑被污染,而且微濾過程中,這些大分子雜質是可以透過微濾膜進入至滲透側,也進一步地防止了雜質影響到吸附劑的使用壽命,使得吸附劑能夠儘可能多地吸附鋰離子,提高了鋰的收率,也避免了吸附劑上沉積雜質,提高了產品的純度。與實施例1相比可以看出,在相同的吸附劑的用量條件下,該實施例中所得到的碳酸鋰收率高、純度好。
實施例3
與實施例2的區別在於:在得到解吸液之後,通過一級納濾膜進行除鎂、鈣離子。
具體的步驟是:將100克FeSO4離子篩吸附劑加入50升的鹽湖滷水中加熱攪拌,控制溶液溫度為40℃,攪拌60分鐘,滷水中的Li進入吸附劑中,此時溶液中Li的濃度降低至1.07克/升,FeSO4離子篩吸附劑對Li的吸附量約為40毫克/克,再用陶瓷膜對混合料液進行濃縮過濾,陶瓷膜的平均孔徑分別50納米,過濾壓力0.2兆帕,膜面流速3米/秒,過濾溫度50℃,反衝間隔40分鐘,反衝時間為10秒;陶瓷膜過濾濃縮液經過板框壓濾,去除濃縮液中的大部分雜質和水,得到已吸附鋰的吸附劑濾餅,將壓濾所得的吸附劑濾餅先用電導率6秒/厘米的水對吸附劑濾餅進行洗滌,去除濾餅中夾帶的鎂、鈉、鈣等雜質離子,再置於1升磷酸溶液中進行攪拌,磷酸溶液的pH控制在約為1,攪拌時間為60分鐘,控制溶液溫度為50℃,Li進入磷酸溶液中,得到鋰解吸溶液,鋰解吸溶液再一級納濾膜去除解吸液中的少量鎂,納濾膜截留分子量300道爾頓,材質是聚醚碸,操作壓力2.0兆帕,操作溫度30℃,濃縮倍數為5倍,將納濾的透過液使用反滲透膜進行濃縮,反滲透濃縮溫度控制在30℃,操作壓力0.15兆帕,濃縮倍數達到了5倍,再通過加入碳酸鈉的方式使鋰離子轉變為碳酸鋰沉澱,沉澱經過固液分離、洗滌之後,得到碳酸鋰,共獲得碳酸鋰14.01克,純度96%。通過實施例2和實施例3可以看出,當採用納濾作為除鎂手段時相對於採用鎂離子交換樹脂進行除鎂,可以有效地提高反滲透濃縮步驟中的濃縮倍數。
對照例1
對照例1與實施例3的區別在於:未採用鋰吸附劑對滷水進行吸附操作,而是將滷水經過平均孔徑200納米的氧化鋁陶瓷膜進行預過濾之後,將陶瓷膜的滲透液送入後續的納濾除鎂、反滲透濃縮、碳酸鈉沉澱的步驟中。在本對照例中的納濾膜的濃縮倍數為3倍,少於實施例3中的濃縮倍數為5倍。由此可以看出,通過吸附法預除鎂可以顯著地提高納濾膜的濃縮倍數。
實施例4
實施例4與實施例3的區別在於:在經過一級納濾膜的除鎂、濃縮之後,將納濾透過液用離子交換樹脂進行深度除鎂,再將離子交換樹脂的透過液送入到後續的反滲透濃縮、碳酸鈉沉澱的過程中。
具體的步驟是:將100克FeSO4離子篩吸附劑加入50升的鹽湖滷水中加熱攪拌,控制溶液溫度為40℃,攪拌60分鐘,滷水中的Li進入吸附劑中,此時溶液中Li的濃度降低至1.07克/升,FeSO4離子篩吸附劑對Li的吸附量約為40毫克/克,再用陶瓷膜對混合料液進行濃縮過濾,陶瓷膜的平均孔徑分別50納米,過濾壓力0.2兆帕,膜面流速3米/秒,過濾溫度50℃,反衝間隔40分鐘,反衝時間為10秒;陶瓷膜過濾濃縮液經過板框壓濾,去除濃縮液中的大部分雜質和水,得到已吸附鋰的吸附劑濾餅,將壓濾所得的吸附劑濾餅先用電導率6秒/厘米的水對吸附劑濾餅進行洗滌,去除濾餅中夾帶的鎂、鈉、鈣等雜質離子,再置於1升磷酸溶液中進行攪拌,磷酸溶液的pH控制在約為1,攪拌時間為60分鐘,控制溶液溫度為50℃,Li進入磷酸溶液中,得到鋰解吸溶液,鋰解吸溶液再一級納濾膜去除解吸液中的少量鎂,納濾膜截留分子量300道爾頓,材質是聚醚碸,操作壓力2.0兆帕,操作溫度30℃,濃縮倍數為5倍,將納濾的透過液通過陽離子交換樹脂Lewatit MonoPlus TP208進行深度除鎂之後,離子交換樹脂的透過液使用反滲透膜進行濃縮,反滲透濃縮溫度控制在30℃,操作壓力0.15兆帕,濃縮倍數為5倍,再通過加入碳酸鈉的方式使鋰離子轉變為碳酸鋰沉澱,沉澱經過固液分離、洗滌之後,得到碳酸鋰,共獲得碳酸鋰13.95克,純度96.5%。通過實施例3和實施例4可以看出,可以採用進一步對鈉濾透過液用陽離子交換樹脂進行深度除鎂,最終可以提高碳酸鋰的純度。
實施例5
與實施例1的區別在於:吸附、解吸的過程採用的是將吸附劑混合於滷水中,再通過陶瓷膜過濾、板框過濾的方式將吸附劑脫水後再進行解吸。
具體的步驟是:將100克FeSO4離子篩吸附劑加入50升的鹽湖滷水中加熱攪拌,控制溶液溫度為50℃,攪拌50分鐘,滷水中的Li進入吸附劑中,此時溶液中Li的濃度降低至1.02克/升,FeSO4離子篩吸附劑對Li的吸附量約為40毫克/克,再用陶瓷膜對混合料液進行濃縮過濾,陶瓷膜的平均孔徑200納米,過濾壓力0.4兆帕,膜面流速分別採用0.5米/秒、1米/秒、2米/秒、3米/秒、4米/秒,過濾溫度60℃,反衝間隔30分鐘,反衝時間為30秒;陶瓷膜過濾濃縮液經過板框壓濾,去除濃縮液中的大部分雜質和水,得到已吸附鋰的吸附劑濾餅,將壓濾所得的吸附劑濾餅先用LiCl的水溶液(LiCl的濃度為0.2克/升)對吸附劑濾餅進行洗滌,去除濾餅中夾帶的鎂、鈉、鈣等雜質離子,再置於1升磷酸溶液中進行攪拌,磷酸溶液的pH控制在約為1,攪拌時間為50分鐘,控制溶液溫度為45℃,Li進入磷酸溶液中,得到鋰解吸溶液,鋰解吸溶液再經過弱酸型陽離子交換樹脂D113去除解吸液中的少量鎂,解吸液的流量控制在5BV/小時,最後使用反滲透膜進行濃縮,反滲透濃縮溫度控制在30℃,操作壓力0.15兆帕,將鋰解吸液中的鋰離子濃度濃縮至約20克/升左右時即可以通過加入碳酸鈉的方式使鋰離子轉變為碳酸鋰沉澱,沉澱經過固液分離、洗滌之後,得到碳酸鋰。試驗結果如表3。
當膜面流速為0米/秒時,即死端過濾的方式,通過對比可以看出,採用錯流過濾的濃縮模式相對於死端過濾來說,有利於不使雜質在濾餅中的聚集,可以有效地避免吸附劑的污染,它對於最終提高鋰的吸附、洗脫量是有利的,可以提高鋰的提取收率。另外,採用不同的膜面流速時,會導致吸附劑濾餅的不同污染形式,其中在採用4米/秒膜面流速時,可以有效地解決鋰離子提取收率和純度的技術問題。
實施例6
該實施例中採用鋁鹽吸附劑裝填於吸附柱中對滷水中的Li吸附,並對解吸液採用二級納濾濃縮,再對納濾的透過液進行沉澱法去除雜質鹼金屬離子。
具體的步驟是:鹽湖滷水經鋁鹽吸附劑對Li吸附後,然後再供入去離子水進行洗脫,得到解吸液,隨著解吸的過程,解吸液中的Mg含量會發生下降,當檢測到解吸液中的Mg含量分別約為0.5、2、3、4克/升時,將解吸液送入粗過濾器去除其中的吸附劑顆粒及泥沙,透過液進入一級納濾膜元件進行過濾,解吸液經過一級納濾膜元件後,得到一級納濾透過液,一級納濾膜系統操作溫度為45℃,壓力為1.5兆帕,濃縮倍數為4倍。一級納濾膜透過液進入二級納濾膜元件,得到二級納濾透過液,二級納濾膜系統操作溫度為20℃,壓力為3.5兆帕,濃縮倍數為8倍。二級納濾膜透過液進入反滲透系統濃縮,反滲透的運行壓力3.0兆帕,溫度為30℃,濃縮6倍後,反滲透濃縮液進行曬鹽以及多效蒸發後,得到多效蒸發的濃液。向多效蒸發的濃液中依次加入沉澱劑BaCl2、Na2CO3以及NaOH,加入的BaCl2的摩爾濃度比鹽滷中的SO4的摩爾濃度大1%,Na2CO3的摩爾濃度比鹽滷中的Ca的摩爾濃度大1%,NaOH的摩爾濃度比鹽滷中的Mg的摩爾濃度2倍的量再大1%,每次加入沉澱劑後都進行攪拌30分鐘,沉澱反應後,進入陶瓷膜過濾器進行過濾除雜,陶瓷膜孔徑為200納米,壓力為0.5兆帕,過濾過程中開啟反衝裝置,反衝間隔為15分鐘,反衝時間為10秒,經過陶瓷膜過濾之後,得到陶瓷膜透過液,濁度小於0.5NTU。在各組試驗中的離子濃度數據如下表所示。
通過該實施例的4組試驗,可以看出,當解吸液中的Mg離子的濃度是0.5克/升時,導致最終的鋰的收率不高,低於解吸液中Mg離子是2~3克/升的情況。當Mg離子是4克/升濃度,會影響到反滲透的濃縮倍數和分離效率,導致了最終的鋰收率也出現下降。而採用傳統的鎂離子交換樹脂-反滲透法,反滲透膜的濃縮倍數只能達到3倍左右。
實施例7
該實施例與實施例6的區別在於調整了相關的工藝參數。使陶瓷膜清液中的Li含量進一步提高,並減小了雜質鹼金屬離子的含量。
鹽湖滷水經鋁鹽吸附劑對Li吸附後,然後再供入去離子水進行洗脫,得到解吸液,當檢測到解吸液中的Mg含量約為3克/升時,將解吸液送入粗過濾器去除其中的吸附劑顆粒及泥沙,透過液進入一級納濾膜元件進行過濾,解吸液中的Ca含量為48.59毫克/升,Mg含量為3克/升,Li含量為411毫克/升。解吸液經過一級納濾膜元件後,透過液中Ca、Mg和Li的含量為29毫克/升、370毫克/升和575毫克/升。一級納濾膜系統操作溫度為25℃,壓力為3.5兆帕,濃縮倍數為5倍。一級納濾膜透過液進入二級納濾膜元件,二級納濾透過液中Ca、Mg和Li的含量為12.54毫克/升、137.5毫克/升、680毫克/升。二級納濾膜系統操作溫度為40℃,壓力為1.5兆帕,濃縮倍數為10倍。二級納濾膜透過液進入反滲透系統濃縮,反滲透的運行壓力4.0兆帕,溫度為40℃,濃縮6倍後,反滲透濃縮液進行曬鹽以及多效蒸發後,Ca、Mg和Li的含量為0.17克/升、1.21克/升、17.1克/升。向多效蒸發的濃液中依次加入沉澱劑BaCl2、Na2CO3以及NaOH,加入的BaCl2的摩爾濃度比鹽滷中的SO4的摩爾濃度大5%,Na2CO3的摩爾濃度比鹽滷中的Ca的摩爾濃度大10%,NaOH的摩爾濃度比鹽滷中的Mg的摩爾濃度2倍的量再大5%,每次加入沉澱劑後都進行攪拌30分鐘,沉澱反應後,進入陶瓷膜過濾器進行過濾除雜,陶瓷膜孔徑為20納米,壓力為0.1兆帕,過濾過程中開啟反衝裝置,反衝間隔為15分鐘,反衝時間為10秒。陶瓷膜清液濁度小於0.5NTU,Mg+Ca含量為7.5毫克/升,SO4含量為17毫克/升,Li含量為18.8克/升。而採用傳統的鎂離子交換樹脂-反滲透法,反滲透膜的濃縮倍數只能達到2.5倍左右。
實施例8
該實施例與實施例7的區別在於調整了相關的工藝參數。使陶瓷膜清液中的Li含量進一步提高,並減小了雜質鹼金屬離子的含量。
鹽湖滷水經鋁鹽吸附劑對Li吸附後,然後再供入去離子水進行洗脫,得到解吸液,當檢測到解吸液中的Mg含量約為3克/升時,將解吸液送入粗過濾器去除其中的吸附劑顆粒及泥沙,透過液進入一級納濾膜元件進行過濾,解吸液中的Ca含量為47.65毫克/升,Mg含量為3克/升,Li含量為421毫克/升。解吸液經過一級納濾膜元件後,透過液中Ca、Mg和Li的含量為24毫克/升、370毫克/升和615毫克/升。一級納濾膜系統操作溫度為30℃,壓力為3.0兆帕,濃縮倍數為5倍。一級納濾膜透過液進入二級納濾膜元件,二級納濾透過液中Ca、Mg和Li的含量為12.24毫克/升、137.5毫克/升、730毫克/升。二級納濾膜系統操作溫度為40℃,壓力為3.0兆帕,濃縮倍數為11倍。二級納濾膜透過液進入反滲透系統濃縮,反滲透的運行壓力3.5兆帕,溫度為35℃,濃縮8倍後,反滲透濃縮液進行曬鹽以及多效蒸發後,Ca、Mg和Li的含量為0.14克/升、1.01克/升、19.1克/升。向多效蒸發的濃液中依次加入沉澱劑BaCl2、Na2CO3以及NaOH,加入的BaCl2的摩爾濃度比鹽滷中的SO4的摩爾濃度大2%,Na2CO3的摩爾濃度比鹽滷中的Ca的摩爾濃度大2%,NaOH的摩爾濃度比鹽滷中的Mg的摩爾濃度2倍的量再大2%,每次加入沉澱劑後都進行攪拌30分鐘,沉澱反應後,進入陶瓷膜過濾器進行過濾除雜,陶瓷膜孔徑為50納米,壓力為0.3兆帕,過濾過程中開啟反衝裝置,反衝間隔為15分鐘,反衝時間為10秒。陶瓷膜清液濁度小於0.5NTU,Mg+Ca含量為7.3毫克/升,SO4含量為14毫克/升,Li含量為21.8克/升。而採用傳統的鎂離子交換樹脂-反滲透法,反滲透膜的濃縮倍數只能達到3.5倍左右。
實施例9
該實施例中,採用先將吸附劑混合於滷水中,待吸附完全後,通過陶瓷膜錯流過濾混合液,得到含有吸附劑的濃縮液,再將濃縮液用板框壓濾機進一步地脫水後,將脫水的鋰吸附劑濾餅裝填於吸附劑中,加入洗脫水進行解吸,得到解吸液。再將解吸液用納濾、離子交換樹脂的方法進行除鎂,再用反滲透膜進行濃縮之後,加入沉澱劑BaCl2、Na2CO3以及NaOH使Ca、Mg雜質離子沉澱,將沉澱物分離之後,再用碳酸鈉沉澱Li,得到碳酸鋰沉澱。
具體的步驟是:將100克FeSO4離子篩吸附劑加入50升的鹽湖滷水中加熱攪拌,控制溶液溫度為40℃,攪拌60分鐘,滷水中的Li進入吸附劑中,FeSO4離子篩吸附劑對Li的吸附量約為40毫克/克,再用陶瓷膜對混合料液進行濃縮過濾,陶瓷膜的平均孔徑分別50納米,過濾壓力0.2兆帕,膜面流速3米/秒,過濾溫度50℃,反衝間隔40分鐘,反衝時間為10秒;陶瓷膜過濾濃縮液經過板框壓濾,去除濃縮液中的大部分雜質和水,得到已吸附鋰的吸附劑濾餅,將壓濾所得的吸附劑濾餅先用電導率6秒/厘米的水對吸附劑濾餅進行洗滌,去除濾餅中夾帶的鎂、鈉、鈣等雜質離子,再將吸附劑濾勻填充於吸附柱中,加入去離子水進行洗脫,洗脫劑的流速是2BV/小時,噹噹檢測到解吸液中的Mg含量約為2克/升時,透過液進入一級納濾膜元件進行過濾,解吸液中的Ca含量為42.65毫克/升,Mg含量為2克/升,Li含量為450毫克/升。解吸液經過一級納濾膜元件後,透過液中Ca、Mg和Li的含量為20毫克/升、450毫克/升和556毫克/升。一級納濾膜系統操作溫度為45℃,壓力為1.5兆帕,濃縮倍數為5倍,納濾膜截留分子量300道爾頓,材質是聚醚碸。一級納濾膜透過液進入離子交換樹脂吸附塔進行深度除鎂,離子交換樹脂吸附塔透過液中,Ca、Mg和Li的含量為10毫克/升、7毫克/升和750毫克/升。離子交換樹脂透過液進入反滲透系統濃縮,反滲透的運行壓力3.0兆帕,溫度為30℃,濃縮6倍後,向濃縮液中依次加入沉澱劑BaCl2、Na2CO3以及NaOH,加入的BaCl2的摩爾濃度比鹽滷濃縮液中的SO4的摩爾濃度大2%,Na2CO3的摩爾濃度比鹽滷濃縮液中的Ca的摩爾濃度大2%,NaOH的摩爾濃度比鹽滷濃縮液中的Mg的摩爾濃度2倍的量再大2%,每次加入沉澱劑後都進行攪拌30分鐘,沉澱反應後,進入陶瓷膜過濾器進行過濾除雜,陶瓷膜孔徑為200納米,壓力為0.5兆帕。陶瓷膜清液濁度小於0.5NTU,向其中加入精製的Na2CO3溶液,進行攪拌後,進入陶瓷膜過濾器進行濃縮和洗滌,對其進行離心和烘乾後,得到Li2CO3成品,經檢測,獲得Li2CO316.44克,純度為99.5%,達到電池級Li2CO3標準。
實施例10
與實施例9的區別在於:在對解吸液用反滲透膜濃縮之後,還需要對其採用DTRO膜、MVR蒸發器進行深度濃縮,再對蒸發濃縮液中加入沉澱劑BaCl2、Na2CO3以及NaOH使Ca、Mg雜質離子沉澱。
具體的步驟是:將100克FeSO4離子篩吸附劑加入50升的鹽湖滷水中加熱攪拌,控制溶液溫度為40℃,攪拌60分鐘,滷水中的Li進入吸附劑中,FeSO4離子篩吸附劑對Li的吸附量約為40毫克/克,再用陶瓷膜對混合料液進行濃縮過濾,陶瓷膜的平均孔徑分別50納米,過濾壓力0.2兆帕,膜面流速3米/秒,過濾溫度50℃,反衝間隔40分鐘,反衝時間為10秒;陶瓷膜過濾濃縮液經過板框壓濾,去除濃縮液中的大部分雜質和水,得到已吸附鋰的吸附劑濾餅,將壓濾所得的吸附劑濾餅先用電導率6秒/厘米的水對吸附劑濾餅進行洗滌,去除濾餅中夾帶的鎂、鈉、鈣等雜質離子,再將吸附劑濾勻填充於吸附柱中,加入去離子水進行洗脫,洗脫劑的流速是2BV/小時,噹噹檢測到解吸液中的Mg含量約為2克/升時,透過液進入一級納濾膜元件進行過濾,解吸液中的Ca含量為42.65毫克/升,Mg含量為2克/升,Li含量為450毫克/升。解吸液經過一級納濾膜元件後,透過液中Ca、Mg和Li的含量為20毫克/升、450毫克/升和556毫克/升。一級納濾膜系統操作溫度為45℃,壓力為1.5兆帕,濃縮倍數為5倍,納濾膜截留分子量300道爾頓,材質是聚醚碸。一級納濾膜透過液進入離子交換樹脂吸附塔進行深度除鎂,離子交換樹脂吸附塔透過液中,Ca、Mg和Li的含量為10毫克/升、7毫克/升和750毫克/升。離子交換樹脂透過液進入反滲透系統濃縮,反滲透的運行壓力3.0兆帕,溫度為30℃,濃縮6倍後,反滲透濃縮液進入DTRO膜進行深度濃縮,濃縮4倍後進入MVR蒸發器進行蒸發,蒸發後的Ca、Mg和Li的含量為0.23克/升、0.17克/升、18克/升。向多效蒸發的濃液中依次加入沉澱劑BaCl2、Na2CO3以及NaOH,加入的BaCl2的摩爾濃度比鹽滷濃縮液中的SO4的摩爾濃度大2%,Na2CO3的摩爾濃度比鹽滷濃縮液中的Ca的摩爾濃度大2%,NaOH的摩爾濃度比鹽滷濃縮液中的Mg的摩爾濃度2倍的量再大2%,每次加入沉澱劑後都進行攪拌30分鐘,沉澱反應後,進入陶瓷膜過濾器進行過濾除雜,陶瓷膜孔徑為200納米,壓力為0.5兆帕。陶瓷膜清液濁度小於0.5NTU,向其中加入精製的Na2CO3溶液,進行攪拌後,進入陶瓷膜過濾器進行濃縮和洗滌,對其進行離心和烘乾後,得到Li2CO3成品,經檢測,獲得Li2CO321.54克,純度為99.8%,達到電池級Li2CO3標準。
實施例11
與實施例9的區別在於:在得到了多效蒸發的濃液後,加入沉澱劑的順序是依次加入NaOH、BaCl2以及Na2CO3,再進行過濾除沉澱、碳酸鋰沉澱、離心沉澱、烘乾的操作,得到Li2CO319.02克,純度為99.1%。
實施例12
將100克FeSO4離子篩吸附劑加入50升的鹽湖滷水中,再加入活性炭(濃度約3克/升)後加熱攪拌,控制溶液溫度為50℃,攪拌50分鐘,滷水中的Li進入吸附劑中,此時溶液中Li的濃度降低至1.02克/升,FeSO4離子篩吸附劑對Li的吸附約為40毫克/克,經陶瓷膜過濾濃縮過濾,陶瓷膜的平均孔徑是200納米,過濾壓力0.4兆帕,膜面流速4米/秒,過濾溫度60℃,反衝間隔40分鐘,反衝時間為30秒,濃縮倍數約52倍;清液可進入提鎂工序回收鎂,陶瓷膜過濾濃縮液經過板框壓濾,去除濃縮液中的大部分雜質和水,得到已吸附鋰的吸附濾餅,板框壓濾的濾液也進入提鎂工藝回收鎂,將壓濾所得的吸附劑濾餅先用LiCl的水溶液(LiCl的濃度為0.2克/升)對吸附劑濾餅進行洗滌,去除濾餅中夾帶的鎂、鈉、鈣等雜質離子,再置於1升磷酸溶液中進行攪拌,攪拌時間為50分鐘,控制溶液溫度為45℃,Li進入磷酸溶液中,得到鋰解吸溶液,鋰解吸溶液再經過弱酸型陽離子交換樹脂D113去除解吸液中的少量鎂,解吸液的流量控制在5BV/小時,最後使用反滲透膜進行濃縮,反滲透濃縮溫度控制在30℃,操作壓力0.15兆帕,將鋰解吸液中的鋰離子濃度濃縮至約20克/升左右時即可以通過加入碳酸鈉的方式使鋰離子轉變為碳酸鋰沉澱,共獲得碳酸鋰22.16克,純度約99%。可以看出,通過在吸附劑的體系中加入活性炭,可以有效地使吸附劑分散得更加均勻,並且活性炭可以吸附一部分有機物雜質,避免了這些雜質影響到吸附劑的使用壽命,得到的碳酸鋰的得率和純度更好。
榮譽表彰
2019年7月15日,《一種由滷水提取電池級鋰的工藝及裝置》獲第十一屆江蘇省專利項目獎優秀獎。