專利背景
愛滋病的醫學全名為“獲得性免疫缺陷綜合徵”(AcquiredImmune Deficiency Syndrome-AIDS),由人類免疫缺陷病毒(HIV,又稱愛滋病病毒)引起。HIV是一種能攻擊人體免疫系統的病毒。它把人體免疫系統中最重要的T4淋巴細胞作為攻擊目標,大量吞噬、破壞T4淋巴細胞,從而破壞人的免疫系統,最終使免疫系統崩潰,使人體因喪失對各種疾病的抵抗能力而發病並死亡,故科學家稱這種病毒為“人類免疫缺陷病毒”。愛滋病病毒在人體內的潛伏期平均為12年至13年。在發展成愛滋病病人之前外表看上去正常,他們可以沒有任何症狀地生活和工作很多年,便能夠將病毒傳染給其他人,使愛滋病病毒在人群中得以迅速傳播和蔓延。
自1981年全球發現首例愛滋病病人以來,國際社會一直在積極研究以應對這一重大傳染性疾病。2008年7月,聯合國愛滋病規劃署發表的《2008年全球愛滋病疫情報告》指出,經過國際社會多年來為防治愛滋病做出的積極努力,全球愛滋病防治在2007年首次出現了“明顯的重要進展”,愛滋病病毒新感染人數和死亡人數都有所下降。但是,全球愛滋病疫情蔓延的趨勢還沒有得到逆轉。據聯合國愛滋病規劃署統計,截至2008年11月,全球共有3320萬名愛滋病病毒感染者,其中2250萬名感染者分布在撒哈拉沙漠以南的眾多非洲國家;亞洲有近500萬名感染者;東歐和中亞地區約150萬名;拉美地區約170萬名;北美、西歐和中東歐地區約200萬名,其中美國約120萬名。中國於1985年發現首例愛滋病感染病例。在1985年至2000年底的15年間,中國累計報告的發病人數和死亡人數分別為880例和496例,。而截至2007年底,中國現存愛滋病病毒感染者和病人約70萬人,其中愛滋病病人8.5萬人。各種數據說明不論是中國還是全球其他各國在愛滋病防治領域的工作任重而道遠。
2008年11月前各國在愛滋病防治領域的研究重點主要集中在疫苗、診斷和治療這三個方面。多年來,有效的HIV疫苗研製工作仍未成功,治療HIV的特效藥雖然有了一定的成果但是仍然有待進一步研究,這使得對HIV感染的及時和準確診斷成為了愛滋病預防控制工作中的重中之重,也是控制愛滋病傳播的基礎工作和最有效的手段之一。在愛滋病診斷方面,HIV抗體篩查是HIV診斷的通用方法和重要手段。通過對各種血製品和受檢人群的血液或其他體液進行HIV抗體篩查,能有效的檢測出愛滋病病毒感染。具體的抗體篩查方法以檢測原理的不同可劃分為酶聯免疫吸附法、凝集法和層析法,它們均可對血液、唾液和尿液標本進行常規或快速檢測。
隨著醫學和生物技術的不斷發展,2008年11月前在HIV的免疫檢測中以雙抗原夾心法的套用最為廣泛。HIV雙抗原夾心法原理是:在固相支持物上麵包被第一抗原(即包被抗原),加入待檢標本,以合適的方式引入標記有特殊標記物的第二抗原(即標記抗原),假如標本中存在HIV抗體,則HIV抗體跟上述二種抗原,形成“包被抗原-HIV抗體-標記抗原”的三明治結構,然後通過標記抗原上的標記物將信號放大,得出最終的判定結果。
套用HIV雙抗原夾心法的關鍵之一在於標記抗原的質量,標記抗原的活性對免疫檢測的靈敏度有著決定性的影響。而高活性的標記抗原需要具備兩個條件:一方面,標記抗原中單位抗原上結合的標記物要儘可能多;另一方面,標記抗原中抗原的免疫學活性要儘可能高。因此,在標記物和標記方法限定的情況下,製備的標記抗原活性好壞是由抗原特點決定的,高活性的標記抗原其抗原需要具備的條件是:
1.可溶性好,摺疊構象正確。抗原的免疫學活性很大程度依賴於其空間構象,尤其是對抗原上面的構象型表位。抗原在表達時,如果作為包涵體的形式,一般來說都是沒有正確摺疊的。這種溶解性不好的抗原在標記之後一般活性不佳。
2.抗原表達量大,有利於大量生產。這一點是該領域技術人員公知的。
由於很多抗原在和標記物偶聯之後,其形成的標記抗原的活性很低。通常的解決方法就是在抗原上融合表達一段融合蛋白,形成融合蛋白-抗原的嵌合抗原的表達形式,使用該方法表達出來的重組抗原在可溶性和表達量方面均有更好的表現,從而具備優良的標記性能。2008年11月前已有技術中普遍採用的融合蛋白有TRX(由Novagen公司pET-32a載體所帶有的融合蛋白,貨號69015-3)、GST(由Phamarcia公司pGEX-4T-1載體所帶有的融合蛋白,貨號,27-4580-01)、SOD(Chiron公司,US5066591)、CKS(Abbott公司,US5124255)等融合蛋白。這些融合蛋白的運用在一定程度上有利於提高抗原在表達或標記方面的性能,但是均存在一定程度的不足。例如,CKS表達量非常大,但是大部分表達在包涵體,對抗原標記有不利;GST、SOD與HIV抗原蛋白融合表達結果也大多在包涵體,同樣不利於標記;TRX是2008年11月前實際套用中最為常用的一個,但使用中仍存在不足,例如假陽較高。
該發明提供了一種更具優勢的全新的融合蛋白(為便於描述,將此融合蛋白命名為“HT”)。將HT融合蛋白和HIV抗原融合表達,在抗原表達量和可溶性方面均具有明顯優勢。將HT-HIV融合抗原標記之後作為標記抗原套用於HIV雙抗原夾心法檢測HIV抗體,檢測的靈敏度、特異性也有了明顯提高。
此外,該發明的融合蛋白HT,還可以套用於HIV項目之外的其它蛋白的可溶性表達上面。
發明內容
名詞定義
《一種愛滋病毒重組抗原及其融合蛋白》中使用的術語除非另有說明,否則具有以下含義:
融合蛋白:該發明中使用的術語“融合蛋白”是指與目的抗原融合表達成融合抗原的蛋白。
融合抗原:該發明中使用的術語“融合抗原”為融合蛋白與目的抗原的融合表達產物。
重組抗原:該發明中使用的術語“重組抗原”為利用基因工程重組技術,將編碼抗原所對應的核酸序列插入到表達載體,形成重組質粒,然後將重組質粒導入宿主細胞並誘導表達的抗原。
標記抗原:該發明中使用的術語“標記抗原”為免疫檢測中與標記物相偶聯的抗原。
標記:該發明中使用的術語“標記”是指標記抗原跟標記物的偶聯。
標記物:該發明中使用的術語“標記物”指在免疫檢測中可被檢測到的物質,包括但不限於膠體金、辣根過氧化物酶。“標記物”也可指包含該標記物的“標記複合物”。
膠體:該發明中使用的術語“膠體”可為任何合適的膠體,包括但不限於膠體金、膠體硒、膠體銀。
膠體金:colloidalgold,也稱金溶膠goldsol,該專利可以簡稱為Au。
專利目的
《一種愛滋病毒重組抗原及其融合蛋白》的目的是為了提供一種表達量大、可溶性好、摺疊正確的HIV基因工程重組抗原,用它改善2008年11月前已有HIV抗體檢測試劑盒的靈敏度、特異性。
該發明的另外一個目的是為了提供一種可提高重組蛋白的表達量、可溶性、摺疊正確的融合蛋白,含有編碼該融合蛋白的核酸序列,以及含有上述核酸序列的質粒載體,轉化有上述質粒載體的宿主細胞轉化子。
發明詳述
《一種愛滋病毒重組抗原及其融合蛋白》發現了一種新融合蛋白HT,並提供了該融合蛋白的胺基酸序列,如SEQ ID NO:1所示。該融合蛋白,是根據大腸桿菌K-12株的測序結果所推導的某個假定基因的產物。值得進一步說明的是,該基因僅是根據測序得出的核酸序列進行理論上的分析推導而來的,故稱其為假定基因。在該發明之前,還沒有資料記載關於該基因或者該基因所編碼的蛋白的作用和及套用。
發明人通過詳細分析和實驗篩查,發現該發明中涉及到的SEQ ID NO:1的序列的親水性很好,具有成為融合蛋白的潛力。經過一系列的反覆實驗分析,得出HT融合蛋白在各方面相較2008年11月前技術中採用的融合蛋白有明顯的優勢。基於上述分析,將HT蛋白與HIVgp160蛋白質的510至681位胺基酸殘基的蛋白質片段,例如SEQ ID NO:4所示的HIV蛋白片段融合表達,根據實驗結果顯示,HT融合蛋白的套用可以提高HIV蛋白的表達量,並且使蛋白表達產物分布在上清的比例大大提高。
因此,該發明提供一種重組蛋白質,其特徵在於該重組蛋白質含有如下(A)或者(B)所述的蛋白質:(A)具有SEQ ID NO:2所示的胺基酸序列;(B)將(A)中的胺基酸序列經過一到幾個胺基酸殘基的取代、缺失或者添加而衍生的蛋白質並且不改變其親水性。
進一步,該發明提供一種重組蛋白質,其特徵在於該重組蛋白質含有如下(A)或者(B)所述的蛋白質:(A)具有SEQ ID NO:3所示的胺基酸序列;(B)將(A)中的胺基酸序列經過一到幾個胺基酸殘基的取代,缺失或者添加而衍生的蛋白質並且不改變其親水性。
進一步,該發明提供一種重組蛋白質,其特徵在於該重組蛋白質含有如下(A)或者(B)所述的蛋白質:(A)具有SEQ ID NO:1所示的胺基酸序列;(B)將(A)中的胺基酸序列經過一到幾個胺基酸殘基的取代、缺失或者添加而衍生的蛋白質並且不改變其親水性。
此外,通過融合表達該發明的HT蛋白和HIVenv基因編碼的gp41蛋白(如SEQ ID NO:4所示),可顯著增大整個蛋白的的表達量,提高整個重組抗原的可溶性;尤其在經過標記之後,將該重組抗原套用於HIV雙抗原夾心法檢測,具有靈敏度高、特異性好的突出特點。
因此,該發明提供一種重組蛋白質,該基因工程重組蛋白質裡面不僅包含有SEQ ID NO:1或2或3所代表的蛋白質序列,還嵌合有含有HIVgp160蛋白質的510至681位胺基酸殘基的蛋白質片段。
進一步,該發明還提供一種重組蛋白質,該基因工程重組蛋白質裡面不僅包含有SEQ ID NO:1或2或3所代表的蛋白質序列,還嵌合有含有如SQEIDNO:4所示的HIVgp41蛋白質片段。
進一步,該發明還提供上述的重組蛋白質製備的HIV抗體檢測試劑盒。
在另一方面,該發明還提供編碼所述重組蛋白的核酸序列的載體和該載體所轉化的宿主細胞。
在另一方面,該發明還提供上述重組蛋白的製備方法,包括:
(a)將編碼含有SEQ ID NO:1或2或3蛋白質片段的核苷酸序列連於質粒載體,形成重組質粒;
(b)將步驟(a)中的重組質粒轉入宿主細胞,形成轉化子細胞;
(c)在適合的條件下,培養步驟(b)中的轉化子細胞,表達該重組蛋白質;
(d)分離純化出該重組蛋白質。
技術方案
《一種愛滋病毒重組抗原及其融合蛋白》涉及的一個基因工程重組蛋白(即HT)的核酸序列是從大腸桿菌K-12株的基因組序列中獲取的。其獲取方法為:提取大腸桿菌K-12株的基因組,以大腸桿菌K-12株的基因組序列為模版,合成兩條引物A1和B1,其中A1為正向引物,B1為反向引物,引物兩端帶有合適的酶切位點,選擇適當的溫度和過程PCR出HT的DNA片段。將PCR產物通過瓊脂糖凝膠電泳確定大小和濃度後,經過酶切、連線,將該HT蛋白的基因構建到一個不帶有融合蛋白基因的載體中。HT載體構建好後,通過轉化宿主菌,選取單克隆菌株培養,誘導目的蛋白表達,進行SDS-PAGE電泳、酶切電泳鑑定陽性菌株。選取合適的宿主蛋白,培養表達並純化相應的基因工程重組蛋白HT。
該發明中涉及到的一個重組蛋白,即重組蛋白HT與HIVgp41蛋白融合的重組抗原的獲取方法。以構建好的HT載體為模板,選擇合適的酶切位點,同時擴增SQEIDNO:4所示的HIVgp41基因片段,並且該片段帶有跟HT載體能夠連線到一起的酶切位點,按照通用的分子克隆過程構建載體。載體構建好後,通過轉化,菌株培養,獲取相應的質粒。選取合適的宿主菌株,培養表達並純化相應的蛋白。
該發明涉及的重組抗原即HT與愛滋病毒gp41蛋白融合表達的套用僅為該基因工程重組蛋白HT作為融合蛋白在免疫抗原方面的一個具體套用,但不僅僅局限於愛滋病蛋白,還可以與其他蛋白融合套用,並套用於除免疫檢測以外的其他方面。
有益效果
根據以上《一種愛滋病毒重組抗原及其融合蛋白》的描述,該發明的重組蛋白作為融合蛋白與其他目的蛋白融合表達後,能增強目的蛋白親水性,有利於目的蛋白表達在上清部分,從而使目的抗原的空間構象摺疊的更加接近天然抗原。根據以上特點,採用此重組蛋白HT作為融合蛋白與目的蛋白融合表達出來的重組抗原具有很高活性,尤其是用在免疫檢測中的酶標記或者膠體標記的標記抗原時,靈敏度、特異性等均顯著優於2008年11月前常用的其他方式所表達的抗原。
該發明的目的、特徵及優點將結合實施例,參照附圖作進一步詳細闡述。應當理解,這些實施例僅用於說明該發明而不用於限定該發明的範圍。下列實施例中未註明具體條件的實驗方法,通常按照常規條件,例如Sambrook等人,分子克隆實驗室手冊(NewYork:Cold Spring Harbor Laboratory Press,0989)中所述的條件,或者試劑盒生產廠家推薦的方法。
附圖說明
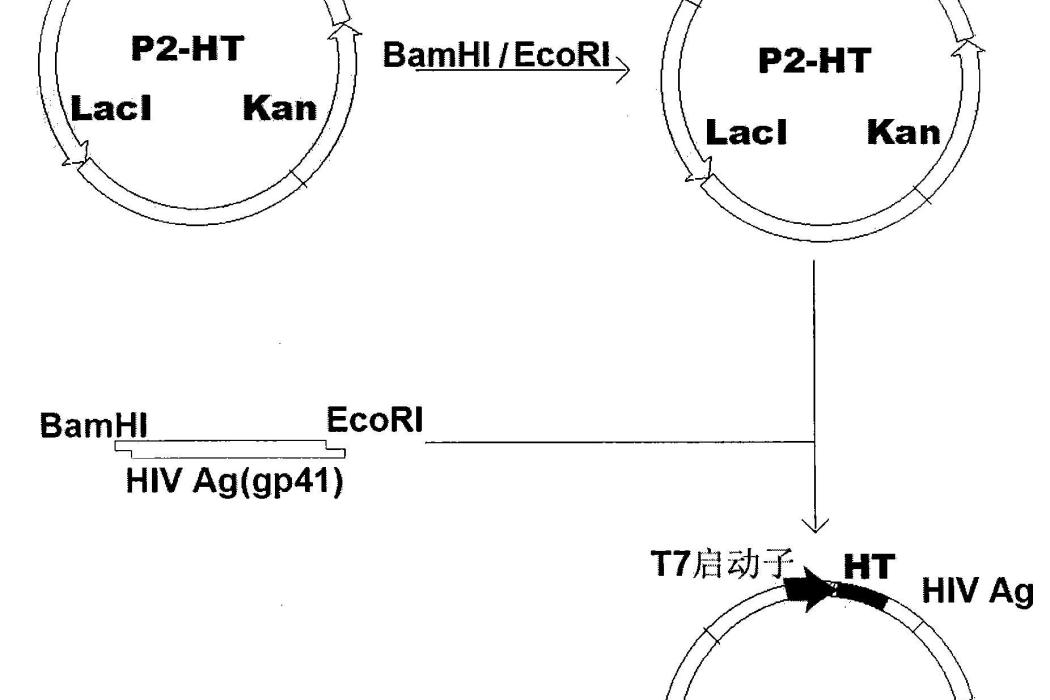
圖1:P2-HT載體的構建過程;
圖2:P2-HT-HIV表達質粒的構建過程。
技術領域
《一種愛滋病毒重組抗原及其融合蛋白》屬於免疫檢測領域,具體地說,該發明涉及一種新的融合蛋白,含有編碼該融合蛋白的核酸序列,以及含有上述核酸序列的質粒載體,轉化有上述質粒載體的宿主細胞轉化子,還涉及一種利用該融合蛋白構建的HIV重組抗原,以及該重組抗原製備的HIV抗體檢測試劑盒。
權利要求
1.一種重組蛋白質,其特徵在於該重組蛋白質由SEQ ID NO:2所示的胺基酸序列與SQEIDNO:4所示的HIVgp41蛋白質片段融合表達而成。
2.一種重組蛋白質,其特徵在於該重組蛋白質由SEQ ID NO:3所示的胺基酸序列與SQEIDNO:4所示的HIVgp41蛋白質片段融合表達而成。
3.一種重組蛋白質,其特徵在於該重組蛋白質由SEQ ID NO:1所示的胺基酸序列與SQEIDNO:4所示的HIVgp41蛋白質片段融合表達而成。
4.一種質粒載體,其特徵在於該質粒載體含有能夠編碼權利要求1-3所述的重組蛋白質的核苷酸序列。
5.一種採用權利要求6所述質粒載體轉化的宿主細胞。
6.一種生產權利要求1-3所述的重組蛋白質的方法,包括:
(a)將編碼具有權利要求1-3的核苷酸序列連於質粒載體,形成重組質粒;
(b)將步驟(a)中的重組質粒轉入宿主細胞,形成轉化子細胞;
(c)在適合的條件下,培養步驟(b)中的轉化子細胞,表達該重組蛋白質;
(d)分離純化出該重組蛋白質。
7.含有權利要求1-3所述的重組蛋白質的HIV抗體檢測試劑盒。
實施方式
實施例1 構建帶有HT融合蛋白的載體
該發明參考專利FPCH04160045P構建了表達質粒P2,也就是該發明所使用的克隆載體,在實施該發明的過程中P2並不是必須表達載體,其上游的增強子該該發明中也不起實質作用,構建此載體只是為了克隆方便,其它許多表達載體如pET-24a(+)(美國Novagen公司,貨號69749-3)均可用於實施該發明。
用Oligo軟體計算機輔助設計該SEQ ID NO:1區段的引物,引物序列為:上游引物A15’-GGC AGA TCT CAC CAC CAC CAC CAC CAC GAA GCG GAA CAG CAA GG-3’,5’端帶有BglII酶切位點和三個保護鹼基,以及6個His的標籤,下游引物B15’-GGC GAA TTC TTA GGA TCC ATT AAA CCA GCT GTC CGA TT-3’,5’端帶有BamHI、EcoRI酶切位點,兩個酶切位點之間加入一個終止密碼子,最末端帶有三個保護鹼基。同原理,用Oligo軟體計算機輔助設計分別設計SEQ ID NO:2和SEQ ID NO:3區段的引物,其中SEQ ID NO:2的兩條引物分別為A25’-GGC AGA TCT CAC CAC CAC CAC CAC CAC GAC AAA AAA CGC-3’,B25’-GGC GAA TTC TTA GGA TCC CTT TGT GCT TCA GTT-3’;SEQ ID NO:3的兩條引物分別為A35’-GGC AGA TCT CAC CAC CAC CAC CAC CAC AAG AAA GCT CGT C-3’,B35’-GGC GAA TTC TTA GGA TCC CTT TGT GCT TCA GTT-3’。
在裝有5毫升LB培養基的試管內,接種大腸桿菌ER2566菌株(美國New England Biolabs公司),37℃搖床培養至OD=1,收集菌液,12000轉/分離心,去掉上清,菌體用基因組提取試劑盒(該發明所使用的分子生物學提取和回收試劑盒均購自上海華舜生物工程有限公司)提取其全基因組。
以上面提取的ER2566基因組作為模板,用上面設計的三對引物分別PCR擴增HT基因。PCR條件為:94℃,5分鐘×1個循環,(94℃,30秒鐘,55℃,40秒鐘,72℃,40秒鐘)×30個循環,72℃,10分鐘×1個循環。為了方便描述,得到的SEQ ID NO:1,2和3三段PCR產物分別對應命名為HT1,HT2和HT3。將上述PCR產物回收之後,分別用BglII和EcoRI酶(該發明所採用的各種分子生物學用酶均購自大連寶生物工程有限公司)同時酶切,之後回收各自的酶切產物,分別連線到用BamHI和EcoRI酶切之後的P2載體上,經過轉化,PCR鑑定重組子,得到陽性轉化子,提質粒,就得到了改造好的載體P2-HT1,P2-HT2,P2-HT3。該步驟可參見圖1。
實施例2 構建含有HIV融合抗原基因的表達質粒
PCR擴增HIV的env基因gp41中SEQ ID NO:4區段所對應的DNA片段,其上游引物帶有BamHI位點,下游引物帶有EcoRI位點且EcoRI位點之前帶有終止密碼TAA。PCR的片段經過回收和酶切之後,分別連線到經過BamHI和EcoRI酶切之後的P2-HT1,P2-HT2,P2-HT3載體,經過轉化,PCR鑑定重組子,得到的陽性克隆P2-HT1-HIV,P2-HT2-HIV,P2-HT3-HIV。該步驟可參見圖2。
實施例3 含有HIV融合抗原的表達和純化
將P2-HT1-HIV,P2-HT2-HIV,P2-HT3-HIV質粒分別轉化大腸桿菌ER2566,塗布於含100微升微克/毫升硫酸卡那黴素(上海生工生物工程技術服務有限公司,以下簡稱生工,貨號KB0286)的LB平板上,37℃過夜培養,挑取單克隆,用含同一濃度卡那黴素的500毫升LB培養基37℃振盪培養至OD6001.0左右,用終濃度為0.5毫摩爾/升的IPTG(生工,貨號IB0168)進行誘導,誘導條件為:37℃,200轉/分,4小時。4℃5000轉/分離心20分鐘收集菌體,每升菌液的菌體用10毫升裂解緩衝液(50毫摩爾/升Tirs-HCl,pH8.0,1毫摩爾/升EDTA,100毫摩爾/升NaCl)重懸,超聲破碎,4℃12000轉/分離心20分鐘,經SDS-PAGE電泳鑑定後,三種表達產物均有90%以上的目的蛋白分布在裂解上清液中。
為進一步證明該發明中的融合蛋白具有表達量大,上清分布比例大的優勢,故將上述HIV的env基因gp41中SEQ ID NO:4區段所對應的片斷分別與其他載體P2(不加任何融合蛋白)、P2-TRX、P2-GST、P2-SOD、P2-CKS進行融合表達,並將其結果作對比實驗,來進行關於HT融合蛋白優越性說明。即將P2-HT1-HIV,P2-HT2-HIV,P2-HT3-HIV、P2-HIV、P2-TRX-HIV、P2-GST-HIV、P2-SOD-HIV、P2-CKS-HIV(這幾個克隆的製備過程,和P2-HT1-HIV類似,該領域的技術人員應該熟知,在此不再贅述)在同一條件下的誘導表達結果作比較。對比實驗步驟:各取P2-HT1-HIV,P2-HT2-HIV,P2-HT3-HIV、P2-HIV、P2-TRX-HIV、P2-GST-HIV、P2-SOD-HIV、P2-CKS-HIV質粒0.2微升轉化大腸桿菌ER2566感受態細胞,塗布於含100微升微克/毫升卡那黴素的LB平板上,37℃過夜培養。各挑取P2-HT1-HIV,P2-HT2-HIV,P2-HT3-HIV、P2-HIV、P2-TRX-HIV、P2-GST-HIV、P2-SOD-HIV、P2-CKS-HIV的單克隆10個,分別用含同一濃度卡那黴素的500毫升LB培養基37℃振盪培養至OD600=1.0,用終濃度為0.5毫摩爾/升的IPTG(生工,貨號IB0168)進行誘導,誘導條件為:37℃,200轉/分,4小時。4℃5000轉/分離心20分鐘收集菌體,每升菌液的菌體用10毫升裂解緩衝液(50毫摩爾/升Tirs-HCl,pH8.0,1毫摩爾/升EDTA,100毫摩爾/升NaCl)重懸,超聲破碎,4℃12000轉/分離心20分鐘,收集上清和沉澱部分,分別取相同初始菌體積的蛋白成分,上SDS-PAGE電泳,通過Dolphin-1D軟體分析凝膠,得出各自表達量(目的蛋白占總蛋白的百分比)和溶解性(上清目的蛋白占總目的蛋白的百分比)的平均值,結果如下:
表1:Dolphin-1D分析凝膠對P2-HT1-HIV、P2-HT2-HIV、P2-HT3-HIV、P2-HIV、P2-TRX-HIV、P2-GST-HIV、P2-SOD-HIV、P2-CKS-HIV表達結果的分析比對 |
| | |
| | |
| | |
| | |
| | |
| | |
| | |
| | |
| | |
從上述結果可以看到,P2-HT1-HIV,P2-HT2-HIV,P2-HT3-HIV的表達量和溶解性要好於其它幾種抗原。
收集P2-HT1-HIVAg上清,加入0.5倍上清體積的飽和硫酸銨溶液,4℃12000轉/分離心20分鐘,收集沉澱,用10毫昇平衡緩衝液(10毫摩爾/升Na2HPO4,1.8毫摩爾/升KH2PO4,140毫摩爾/升NaCl,2.7毫摩爾/升KCl,5毫摩爾/升咪唑(美國Sigma-Aldrich公司,貨號I5513),pH8.0)溶解,用10倍柱床體積的平衡緩衝液平衡Ni-NTA親和柱(Qiagen公司,貨號30210)之後,加入蛋白樣,用10倍介質體積的平衡緩衝液洗去未結合的蛋白,再用5倍體積洗脫緩衝液(50毫摩爾/升NaH2PO4,300毫摩爾/升NaCl,500毫摩爾/升咪唑,pH8.0),洗脫目的蛋白,測定蛋白濃度,-20℃保存備用。P2-HT1-HIV質粒表達純化之後的融合抗原在下文簡寫為P2-HT1-HIVAg。其它表達在上清中的目的蛋白,純化方式類似。
P2-HIV、P2-GST-HIV、P2-CKS-HIV、P2-SOD-HIV包涵體的純化方式:經SDS-PAGE電泳鑑定後,部分目的蛋白分布在裂解液沉澱。每升菌液的菌體用10毫升裂解緩衝液(50毫摩爾/升Tirs-HCl,pH8.0,1毫摩爾/升EDTA,100毫摩爾/升NaCl)重懸,超聲破碎,4℃12000轉/分離心20分鐘收集包涵體,用含2%TritonX-100(生工貨號T0694)的溶液I(20毫摩爾/升Tirs-HCl,pH8.5,5毫摩爾/升EDTA,100毫摩爾/升NaCl)重懸,4℃12000轉/分離心20分鐘收集包涵體,用溶液I配製的8摩爾/升尿素溶解後對100倍體積的PB緩衝液(pH7.0,20毫摩爾/升)透析,換液3次,4℃12000轉/分離心20分鐘去除沉澱後製成粗抗原,用10毫昇平衡緩衝液(10毫摩爾/升Na
2HPO
4,1.8毫摩爾/升KH
2PO
4,140毫摩爾/升NaCl,2.7毫摩爾/升KCl,25毫摩爾/升咪唑(美國Sigma-Aldrich公司,貨號I5513),pH8.0)溶解。用10倍柱床體積的平衡緩衝液平衡Ni-NTA親和柱(Qiagen公司,貨號30210)之後,加入蛋白樣,用10倍介質體積的平衡緩衝液洗去未結合的蛋白,再用5倍體積洗脫緩衝液(20毫摩爾/升Na
2HPO
4,300毫摩爾/升NaCl,250毫摩爾/升
咪唑,pH8.0),洗脫目的蛋白。
純化之後的目的蛋白分別命名為P2-HT1-HIVAg、P2-HT2-HIVAg、P2-HT3-HIVAg、P2-HIVAg、P2-TRX-HIVAg、P2-GST-HIVAg、P2-SOD-HIVAg、P2-CKS-HIVAg。
實施例4 融合抗原和HRP的偶聯
融合抗原和HRP的偶聯採用NaIO4氧化法。稱取10毫克辣根過氧化物酶(HRP,美國SIGMA公司,貨號P8375)溶解於1毫升超純水中,再緩慢滴加1毫升超純水新鮮配製的5毫克/毫升NaIO4(生工,貨號ST1244)溶液,室溫下避光輕柔攪拌40分鐘後加入20%乙二醇(生工,貨號E0582)溶液0.05毫升,室溫下避光攪拌40分鐘。然後立即加入事先對100毫摩爾/升,pH9.51碳酸鹽緩衝液透析2小時,2.5毫克/毫升的純化好的P2-HT1-HIVAg抗原1毫升,4℃避光對100毫摩爾/升,pH9.51碳酸鹽緩衝液透析過夜。次日,向混合物中滴加0.1毫升新鮮配製的4毫克/毫升NaBH4(生工,貨號ST1268)溶液,混勻,4℃靜置2小時。將上述溶液裝入透析袋中,對PBS緩衝液(150毫摩爾/升,pH7.4)透析,4℃過夜。加入酶保護劑及終濃度50%的甘油混勻後-20℃避光保存備用。P2-HT1-HIVAg融合抗原標記HRP之後的標記抗原在以下的文字中稱為P2-HT1-HIVAg-HRP,其它抗原製備標記抗原的名稱和製備方法均以此類推。
實施例5 含有HRP的HIV重組抗原用於雙抗原夾心法ELISA檢測HIV抗體
將P2-HIVAg抗原以一定比例用碳酸鹽緩衝液(50毫摩爾/升,pH9.51)稀釋,100微升/孔加入酶標板(深圳金燦華實業有限公司輻照酶標板),4℃包被24小時,次日用PBST(10毫摩爾/升PB,150毫摩爾/升NaCl,0.05%Tween-20,pH7.4)洗滌液洗板二次,拍乾,120微升/孔加入含30%新生牛血清(北京元亨聖馬生物技術研究所),8%蔗糖,5‰酪蛋白(美國Sigma-Aldrich公司,貨號C-8645),1‰β-巰基乙醇(生工,貨號M0482),150毫摩爾/升NaCl的pH7.4,10毫摩爾/升PB封閉液,37℃封閉2小時,甩掉孔內液體,拍乾,置室溫20-25℃、濕度55%-65%、有通風設備的房間內風乾。封裝於加有乾燥劑的鋁膜袋中,包被完畢。
在包被酶標板中先加入100微升待測樣品、陰性參照樣品(正常人陰性血清)、陽性參照樣品(HIV-1型抗體陽性血清)對照,37℃溫育30分鐘;用PBST洗滌液洗板五次,拍乾。再100微升/孔加入含有20%新生牛血清,以一定比例稀釋的P2-HT1-HIVAg-HRP綴合物的pH7.4的20毫摩爾/升PB緩衝液,37℃溫育30分鐘;用PBST洗滌液洗板五次,拍乾。(P2-HT2-HIVAg-HRP,P2-HT3-HIVAg-HRP的實驗方法同P2-HT1-HIVAg-HRP)
每孔加入含0.5‰過氧化氫尿素(生工,貨號UB1753)、4.76‰三水合乙酸鈉、0.9‰冰醋酸的顯色劑A及含0.32‰TMB(生工,貨號TB0514)、5毫摩爾/升檸檬酸、0.5毫摩爾/升EDTA-2Na、5%甲醇、2‰二甲基甲醯胺的顯色劑B各50微升,37℃避光顯色10分鐘。每孔加50微升,含2摩爾/升硫酸的終止液終止反應,酶標儀450nm波長(參考波長630nm)空白孔校零後讀取OD值。
截值(CutoffValue(COV))計算:COV=陰性對照平均OD值×2.0(陰性對照OD值低於0.075按0.075計算,高於0.075按實際OD值計算),待測樣品OD值≥COV為陽性,待測樣品OD值<COV為陰性。
該發明的融合蛋白HT(包括HT1,HT2,HT3)連線HIV目的蛋白之後表達的重組抗原,標記HRP之後用於雙抗原夾心法ELISA檢測HIV抗體,靈敏度、特異性、準確性等指標均優於P2、P2-TRX、P2-GST、P2-SOD、P2-CKS等表達載體表達的HIV抗原標記HRP之後的綴合物。
(1)靈敏度
用同樣的方法選擇最佳的標記條件,將P2-HT1-HIVAg,P2-HT2-HIVAg,P2-HT3-HIVAg、P2-HIVAg、P2-TRX-HIVAg、P2-GST-HIVAg、P2-SOD-HIVAg、P2-CKS-HIVAg分別標記上HRP,並用同樣的方法選擇各自的最佳使用比例,再用二步夾心法在同一環境統一的試劑的條件在對100份的系列稀釋比例的HIV-1型抗體陽性血清進行檢測,得到了表2的結果,結果表明該發明融合蛋白連線HIV基因並標記後和P2、P2-TRX、P2-GST、P2-SOD、P2-CKS等表達載體連線HIV抗原並標記後對各稀釋度血清反應的靈敏度差異均具有統計意義(P<0.05)。由此可見,該發明融合蛋白連線HIV型抗原並標記後的靈敏度有較大的提高。
表2:該發明融合蛋白HT連線HIV抗原表達的融合抗原製備的HRP綴合物在用於雙抗原夾心法ELISA檢測HIV抗體時的靈敏度比較 |
| |
| | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
(2)特異性
用P2-HIVAg包被96孔板,用P2-HT1-HIVAg-HRP,P2-HT2-HIVAg-HRP,P2-HT3-HIVAg-HRP、P2-HIVAg-HRP、P2-TRX-HIVAg-HRP、P2-GST-HIVAg-HRP、P2-SOD-HIVAg-HRP、P2-CKS-HIVAg-HRP綴合物作為酶標記物分別組成試劑盒,用二步夾心法在相同條件下分別分別檢測了3000份臨床陰性血清,P2-HT1-HIVAg-HRP,P2-HT2-HIVAg-HRP,P2-HT3-HIVAg-HRP假陽性率為0.033%,P2-HIVAg-HRP、P2-CKS-HIVAg-HRP假陽性率為0.066%,P2-GST-HIVAg-HRP、P2-SOD-HIVAg-HRP的假陽性率為0.1%、P2-TRX-HIVAg-HRP假陽性率為0.133%。
(3)重複性
對陰、陽性待測樣品各240份,採用不同時不同批次不同操作者進行多次檢測,考查P2-HT1-HIVAg-HRP,P2-HT2-HIVAg-HRP,P2-HT3-HIVAg-HRP分別用於組成試劑盒後判定結果的重複性,結果顯示該發明P2-HT1-HIVAg-HRP,P2-HT2-HIVAg-HRP,P2-HT3-HIVAg-HRP用於組成的試劑盒對陰、陽性判定結果的重複性均為100%。這表明該融合蛋白用於基因克隆及HRP標記的再現性好,重複性高。
(4)穩定性
將該發明的融合蛋白連線抗原後表達的蛋白P2-HT1-HIVAg,P2-HT2-HIVAg,P2-HT3-HIVAg以及標記HRP的抗原P2-HT1-HIVAg-HRP,P2-HT2-HIVAg-HRP,P2-HT3-HIVAg-HRP分別37℃考核144小時,取出後與同時4℃存放的抗原和抗原酶在同一條件下檢測相同的陰、陽性質控血清,抗原包被後間接法檢測,抗原酶稀釋成工作液後二步夾心法檢測,其結果見表3和表4。實驗表明,該發明融合蛋白用來表達的抗原和表達抗原標記後的穩定性好。
表3:P2-HT1-HIVAg,P2-HT2-HIVAg,P2-HT3-HIVAg抗原穩定性實驗結果 |
| | | | | | |
| | | | | | |
| | | | |
| | | | | | |
| | | | |
| | | | | | |
| | | | |
表4:P2-HT1-HIVAg-HRP,P2-HT2-HIVAg-HRP,P2-HT3-HIVAg-HRP抗原酶穩定性實驗結果 |
| | | | | | |
| | | | | | |
| | | | |
| | | | | | |
| | | | |
| | | | | | |
| | | | |
在用P2-HIVAg包被的同一反應板上對同一份已知陽性標本,多次平行做大於等於10孔重複間接法檢測,得到各孔的檢測OD值,計算其CV值均低於15%;在同一反應板上對同一份已知陽性標本,用P2-HT1-HIVAg-HRP、P2-HT2-HIVAg-HRP、P2-HT3-HIVAg-HRP稀釋的酶當作酶工作液多次平行做大於等於10孔重複二步夾心法檢測,得到各孔的檢測OD值,計算其CV值均低於10%,說明該試劑盒精密性較好。
實施例6 含有膠體金的的HIV重組抗原的製備
取100毫升超純水於500毫升圓底燒瓶中,放到加熱攪拌器上加熱至沸騰,加入1毫升1%氯金酸(美國Sigma-Aldrich公司)的水溶液,沸騰後加入1毫升1%的檸檬酸鈉(美國Sigma-Aldrich公司),繼續加熱10分鐘後放置自然冷卻。取10毫升P2-HT1-HIVAg抗原裝入透析袋中,對10毫摩爾/升PBSPH7.4緩衝液透析8小時,其間每1小時換一次緩衝液。取10毫升膠體金,用0.2摩爾/升K2CO3溶液調節膠體金的pH至6~7,加入200微升微克P2-HT1-HIVAg抗原,繼續攪拌5~10分鐘。在上述混合液中加入0.5毫升2%BSA溶液,繼續攪拌5分鐘。將上述混合液裝入合適的離心管中。5000轉/分離心10分鐘,吸出上清,將沉澱收集至一合適容器;對上清再用10000轉/分離心15分鐘,重複第一次離心的操作;對上清再用12000轉/分離心30分鐘,棄掉上清,將三次離心的沉澱收集到同一離心管中,用膠體金稀釋液定容至1毫升。將上述沉澱於-4℃冰櫃中保存。金標記好的P2-HT1-HIVAg抗原命名為P2-HT1-HIVAg-AU,其它抗原製備標記抗原的名稱和製備方法均以此類推。採用如下方式確定最佳使用效價:將P2-HT1-HIVAg-AU用膠體金稀釋液稀釋x個稀釋度,每個稀釋度不少於1毫升,即稀釋好的HIV金標工作液,浸泡合適大小的固相載體(如玻璃纖維、聚酯膜、無紡布等),用已知檢定合格的HIV包被抗原包被硝酸纖維素膜(Milipore公司),用夾心法做膠體金免疫試驗,從x個條件中選擇靈敏度最高,特異性最好的條件,即P2-HT1-HIVAg-AU的最佳比例。該領域技術人員應領會,x為相對有限的數目,並且大於等於試驗次數。
實施例7 該發明融合蛋白連線HIV抗原後標記膠體金的綴合物用於雙抗原夾心法金標檢測HIV抗體
該發明融合蛋白連線HIV抗原後標記膠體金的綴合物用於雙抗原夾心法金標檢測HIV抗體,其靈敏度、特異性、準確性等指標均優於P2、P2-TRX、P2-GST、P2-SOD、P2-CKS等表達載體連線HIV抗原後標記綴合物的對應性能。
(1)靈敏度
用同樣的方法選擇最佳的標記條件,將P2-HT1-HIVAg,P2-HT2-HIVAg,P2-HT3-HIVAg、P2-HIVAg、P2-TRX-HIVAg、P2-GST-HIVAg、P2-SOD-HIVAg、P2-CKS-HIVAg分別標記,並用同樣的方法選擇各自的最佳使用濃度,製成膠體金試紙條在同樣的條件下對100份的系列稀釋比例的HIV-1型抗體陽性血清進行檢測,得到了表5的結果,結果表明該發明融合蛋白連線HIV抗原並標記膠體金後和P2、P2-TRX、P2-GST、P2-SOD、P2-CKS等表達載體連線HIV抗原並標記膠體金後對各稀釋度血清反應的靈敏度差異均具有統計意義(P<0.05)。由此可見,該發明融合蛋白連線HIV抗原並標記後的靈敏度有較大的提高。
表5:該發明融合蛋白HT連線HIV基因表達的融合抗原製備的膠體金綴合物在用於膠體金檢測HIV陽性血清的HIV抗體時的靈敏度比較 |
| |
| | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
(2)特異性
該發明的融合蛋白HT連線HIV抗原後,使HIV抗原可溶性明顯增加,利於純化,且更利於膠體金的標記,與其他融合蛋白比特異性明顯改善。用P2-HT1-HIVAg-AU,P2-HT2-HIVAg-AU,P2-HT3-HIVAg-AU、P2-HIVAg-AU、P2-TRX-HIVAg-AU、P2-GST-HIVAg-AU、P2-SOD-HIVAg-AU、P2-CKS-HIVAg-AU用相同的包被硝酸纖維素膜組裝成膠體金試紙條,用雙抗原膠體金夾心法在同條件下分別分別檢測了2000份臨床陰性血清,P2-HT1-HIVAg-AU,P2-HT2-HIVAg-AU,P2-HT3-HIVAg-AU假陽性率均為0.35%,P2-HIVAg-AU假陽性率為0.9%、P2-SOD-HIVAg-AU假陽性率為0.75%、P2-TRX-HIVAg-AU假陽性率為0.8%、P2-GST-HIVAg-AU假陽性率為0.6%、P2-CKS-HIVAg-AU假陽性率為0.85%。
(3)重複性
對陰、陽性待測樣品各200份,採用不同時不同批次不同操作者進行多次檢測,考查P2-HT1-HIVAg-AU,P2-HT2-HIVAg-AU,P2-HT3-HIVAg-AU組裝成的試紙條後判定結果的重複性,結果顯示該發明P2-HT1-HIVAg-AU,P2-HT2-HIVAg-AU,P2-HT3-HIVAg-AU組裝成的試紙條對陰、陽性判定結果的重複性為100%。這表明該融合蛋白用於基因克隆及膠體金標記的再現性好,重複性高。
(4)穩定性
將該發明的融合蛋白連線抗原後表達的蛋白P2-HT1-HIVAg,P2-HT2-HIVAg,P2-HT3-HIVAg以及膠體金標記的P2-HT1-HIVAg-AU,P2-HT2-HIVAg-AU,P2-HT3-HIVAg-AU分別37℃考核7天,取出後與同時4℃存放的抗原和抗原金標複合物在同一條件下檢測相同的陰、陽性質控血清,抗原用同樣方法標記,與抗原金標複合物分別稀釋成工作液後製成膠體金成品條檢測,其結果見表6和表7。實驗表明,該發明融合蛋白用來表達的抗原和表達抗原標記後的穩定性好。
表6:P2-HT1-HIVAg,P2-HT2-HIVAg,P2-HT3-HIVAg抗原穩定性實驗結果 |
| | | | | | |
| | | | | | |
| | | | |
| | | | | | |
| | | | |
| | | | | | |
| | | | |
註:表6中信號強度+代表弱陽,++代表中陽,+++代表強陽。 |
表7:P2-HT1-HIVAg-AU,P2-HT2-HIVAg-AU,P2-HT3-HIVAg-AU抗原金標複合物穩定性實驗結果 |
| | | | | | |
| | | | | | |
| | | | |
| | | | | | |
| | | | |
| | | | | | |
| | | | |
註:表7中信號強度+代表弱陽,++代表中陽,+++代表強陽。 |
(5)精密性
在用P2-HT1-HIVAg-AU,P2-HT2-HIVAg-AU,P2-HT3-HIVAg-AU稀釋成工作液後製成膠體金成品條檢測同一份已知陽性標本,多次平行做10次重複檢測,得到各檢測條的結果均為陽性,且各檢測條的顯色程度也無顯著差異,說明本試劑條精密性較好。
榮譽表彰
2018年12月20日,《一種愛滋病毒重組抗原及其融合蛋白》獲得第二十屆中國專利銀獎。